热门推荐
- 精 缓解超2年!CAR-T疗法横扫多发性骨髓瘤、B细胞淋巴瘤,缓解率实现惊人的100%!
- 精 实至名归!CAR-T先驱获2024年沃伦·阿尔珀特奖!CAR-T细胞疗法重击淋巴细胞白血病!
- 精 靶向GPC3的CAR-T疗法联合药物获得了完全缓解和长期生存,肝细胞癌患者的福音
- 精 CAR-T细胞产品-CT071获批,血液系统肿瘤患者又增新的治疗选择
- 精 GRP78 CAR-T的研究让肿瘤治疗更上一层楼
- 精 CAR-T产品-纳基奥仑赛价格跌破百万,肿瘤患者的福音
- 精 PD-1免疫抑制剂与CAR-T细胞疗法让肿瘤无处躲藏
- 精 CAR-T细胞疗法在骨髓瘤,白血病以及淋巴瘤中大展身手!
- 精 CAR-T在多种实体瘤和血液瘤中全面开花!
- 精 与时间赛跑,CAR-T疗法让淋巴瘤患者重获新生!
- 精 攻克癌症有方法——CAR-T,TILS各显神通
- 精 白血病并不是不治之症CAR-T细胞疗法在血液肿瘤大放光彩
- 精 “抗癌神药”CAR-T疗法到底是班门弄斧还是真有奇效?免疫管家与你揭开谜底。
- 精 解密CAR-T疗法真实治疗流程,细胞治疗到底需要多久呢?
- 精 CAR-T疗法再传捷报!卵巢癌,结肠癌再创佳绩!攻克实体瘤火力全开!!
- 精 120万一支,天价抗癌药,到底值不值?
资讯列表
2026年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)在1 月 8 日至 10 日于美国旧金山举办。此次会议上,易慕峰生物展示了其自主研发的靶向Claudin18.2(CLDN18.2)的自体CAR-T细胞治疗产品IMC002在晚期胃癌/胃食管结合部癌(GC/GEJ)患者中的 I/IIa 期 临床研究结果。
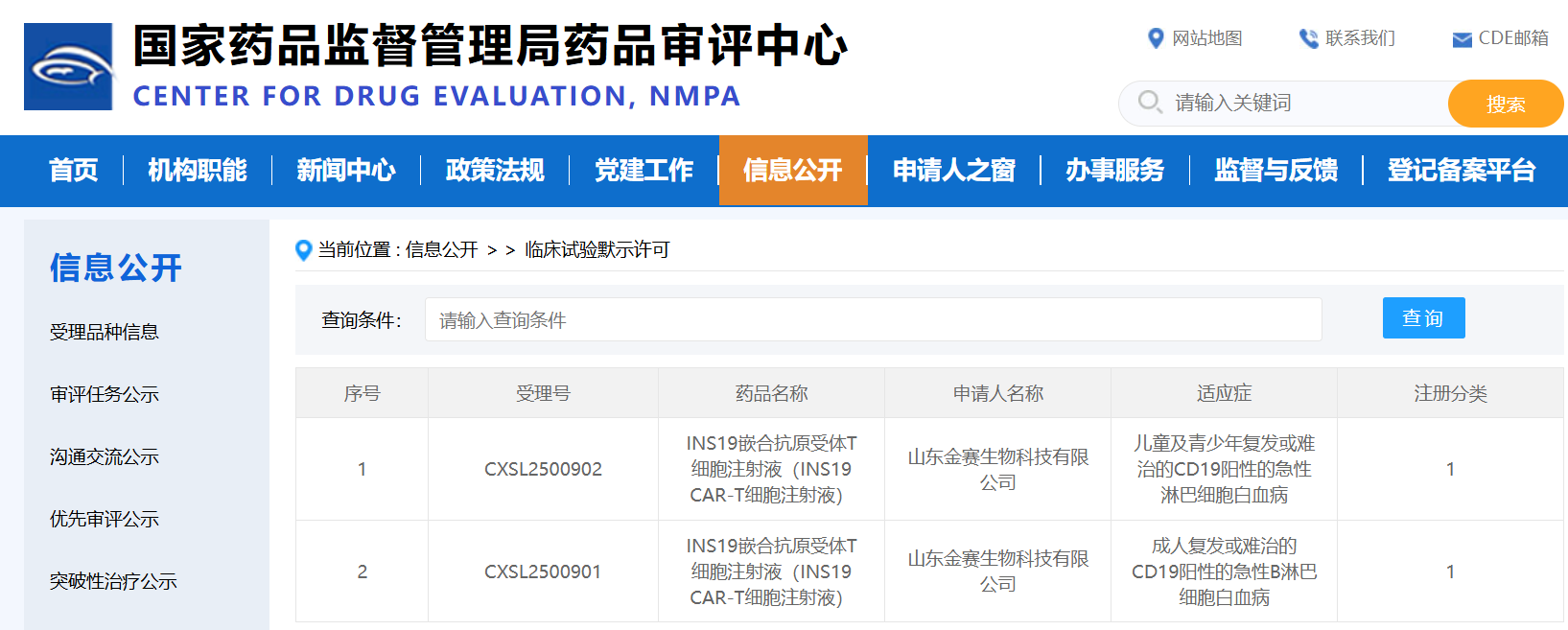
1月9日,国家药品监督管理局药品审评中心(CDE)显示:艺妙神州自主研发的CAR-T细胞候选药物INS19临床试验申请获批,分别用于治疗儿童及青少年复发或难治的CD19阳性的急性淋巴细胞白血病和成人复发或难治的CD19阳性的急性B淋巴细胞白血病(r/r B-ALL)。
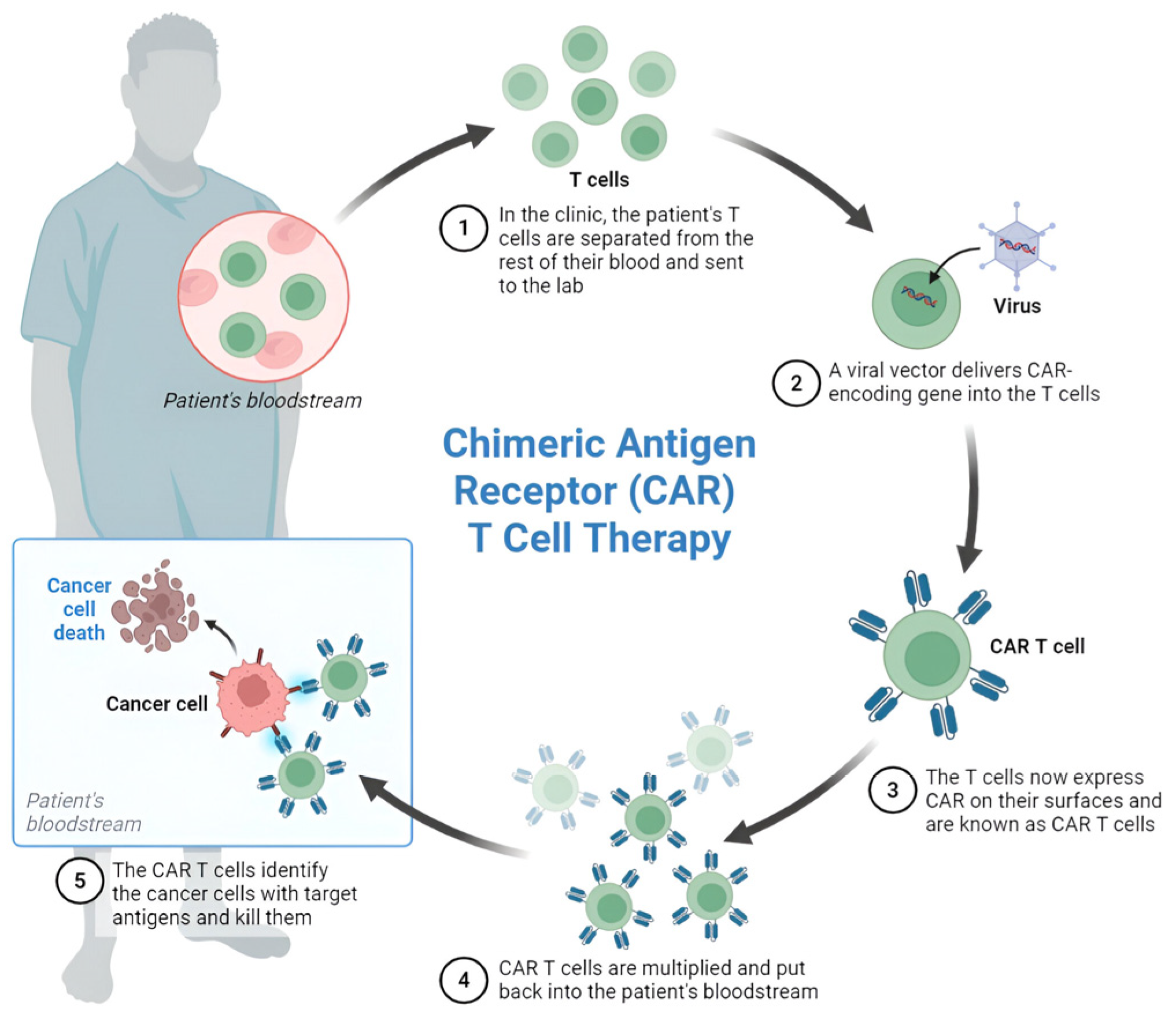
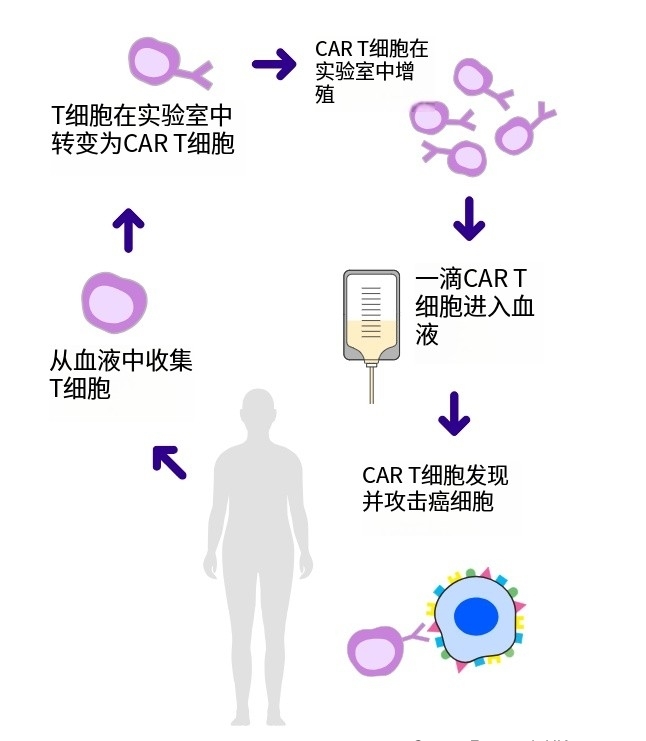
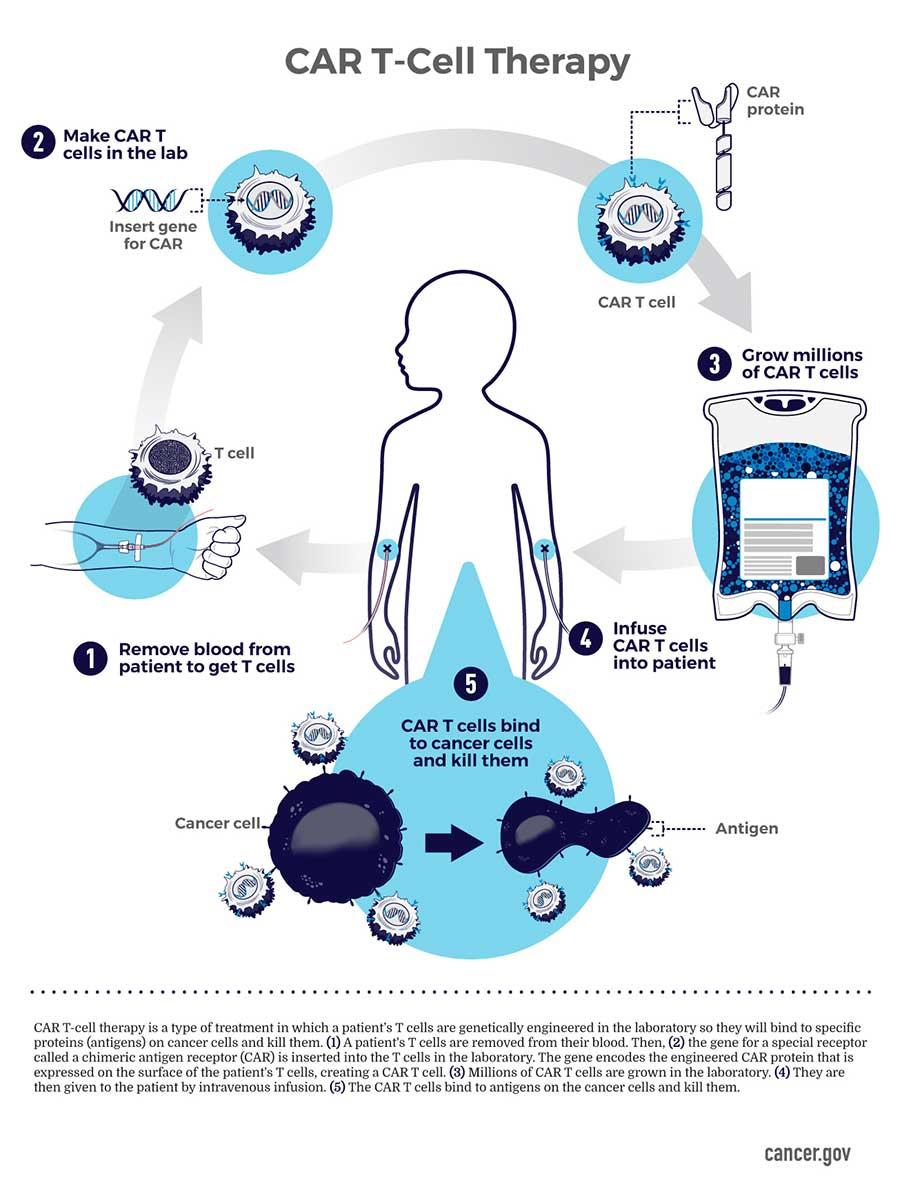
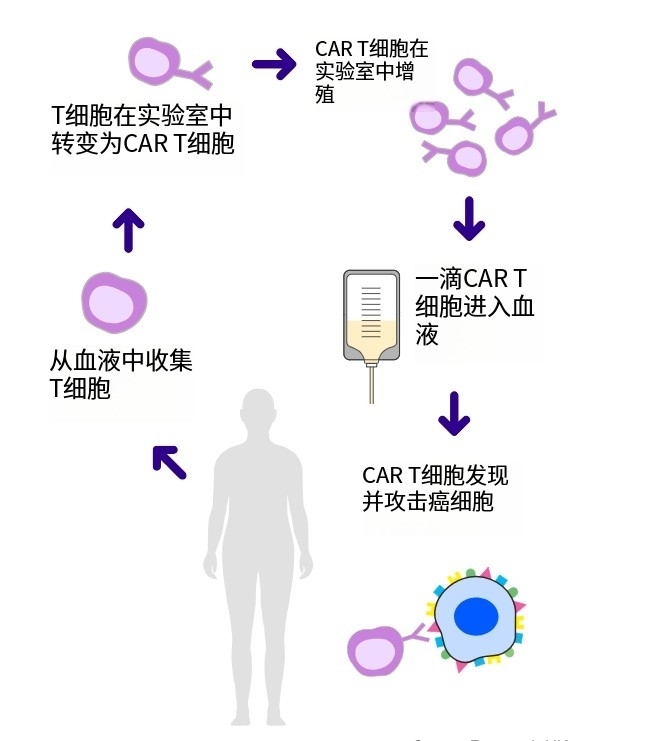
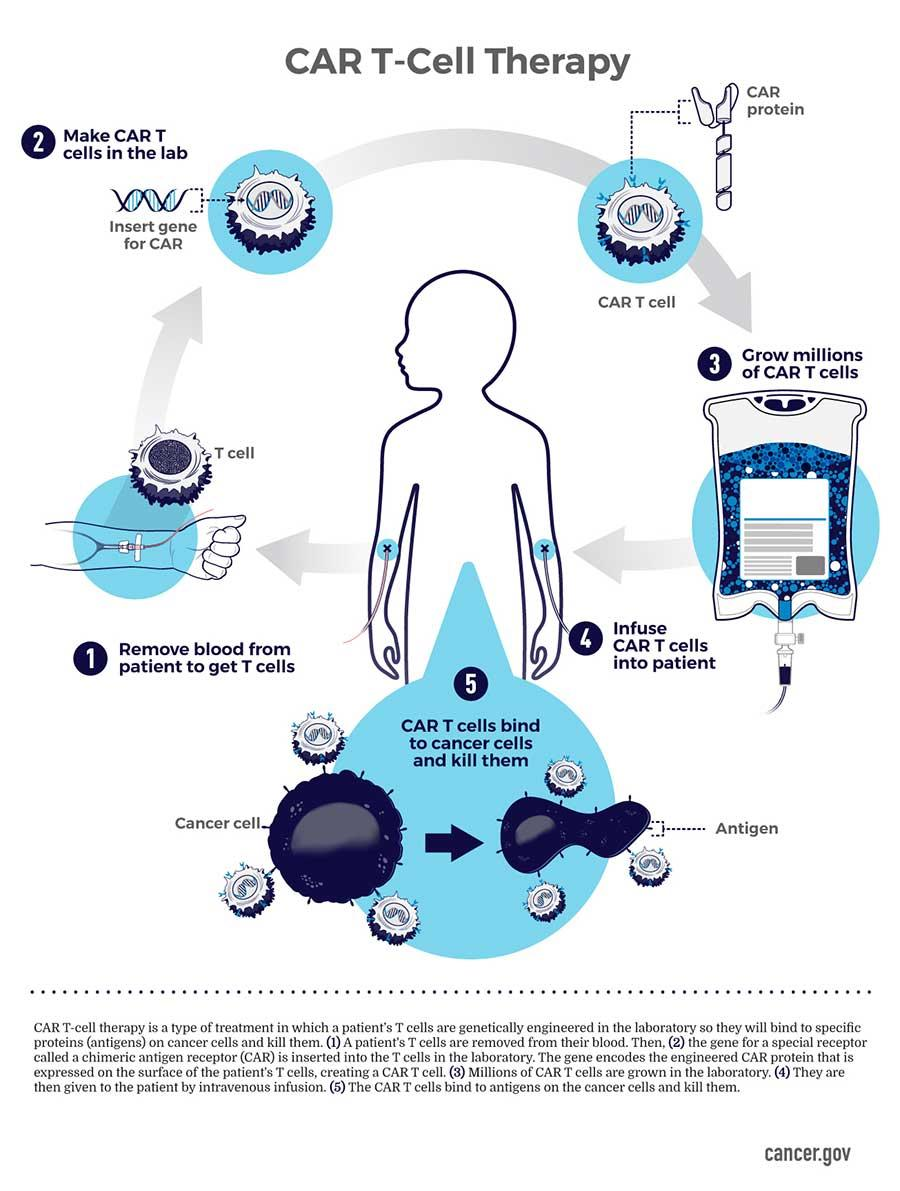
从患者体内提取的T细胞在实验室经过改造,可以精准识别并摧毁癌细胞,这正是CAR-T细胞疗法的魅力,但值得注意的是,CAR-T并非万能神药。
2021年,一款价值120万元的“抗癌神药”引发全民关注。“一针清除癌细胞”的案例在网络上迅速传播,让无数人看到了癌症治愈的新希望。
1月8日,艺妙神州宣布其自主研发的CAR-T细胞治疗产品赛泊华®(通用名:泊基奥仑赛注射液,研发代号:IM19)针对非霍奇金淋巴瘤(NHL)的二线治疗临床试验申请获得批准。此次获批标志着赛泊华®在适应症拓展上取得关键进展,未来有望为更多非霍奇金淋巴瘤患者提供更早线的治疗选择,同时这也是艺妙生物在全球范围内获批的第10个...
自2017年美国食品药品监督管理局(FDA)批准首款CAR-T细胞产品上市短短几年的时间,这款曾经高达120万元一针的抗癌药在国内发展速度令人瞩目。截至目前,国内已经上市八款CAR-T细胞治疗产品,基因细胞药物的临床试验数量和治疗的患者人数众多,稳居世界前端。
“上百万元,用不起”这是CAR-T细胞疗法在国内患者眼中的真实写照。作为肿瘤治疗领域的突破性进展,CAR-T疗法为血液肿瘤患者带来了希望,然而动辄百万元的治疗费用却让大多数家庭望而却步。
12月22日,茂行生物宣布其自主研发的靶向B7H3的通用型CAR-T细胞疗法MT027已获得美国食品药品监督管理局(FDA)批准开展Ⅱ期临床研究,用于治疗复发性胶质母细胞瘤(rGBM)。
12月22日,茂行生物宣布其自主研发的靶向B7H3的通用型CAR-T细胞疗法MT027,已获得美国食品药品监督管理局(FDA)批准开展Ⅱ期临床研究,用于治疗复发性胶质母细胞瘤(rGBM)。