相关推荐

不出国门,就能享受国际前沿治疗!BNCT在中国启航,海南已落地!复发头颈部肿瘤患者迎来春天
近期,一项发表于《Critical Reviews in Oncology/Hematology》的Meta分析,系统评估了硼中子俘获疗法(BNCT)治疗局部复发性头颈癌(LRHNC)的疗效与安全性。
免疫管家 2026-03-12

揭开“临床试验”真相:不是盲目冒险,不是“当小白鼠”,而是走在科学前沿的治疗
很多人一听到“试药”就害怕,认为风险太大。但实际上,即使是已经上市的药物也有风险。临床试验则由更严格的医疗团队保驾护航。
免疫管家 2026-01-05

克利夫兰诊所真实案例!多次复发、治疗无效…直到她尝试了这项前沿异体CAR-T疗法,5年后癌症仍未复发
在癌症治疗的漫长征程中,每一次突破都如同黑暗中的明灯,为患者带来生的希望。12月15日,美国克利夫兰诊所分享了一名难治性多发性骨髓瘤患者通过前沿CAR-T细胞治疗实现5年长期无病生存的病例报告。
免疫管家 2025-12-18

晚期卵巢癌新希望 | 新型TIL疗法GC203临床试验招募,符合条件者可免费入组用药
2023年初,H女士(化名)腹股沟和腰部偶发疼痛,入院检查发现腹膜后、腹股沟等多处的淋巴结肿大,被确诊为IVB期卵巢高级别浆液性癌。一年多来,H女士先后进行了新辅助化疗、妇科晚期肿瘤减瘤手术,一线化疗联合抗血管生成药物以及免疫治疗,后期使用PARP抑制剂维持。但是各种抗癌手段仍然无法阻止癌症复发。
免疫管家 2025-12-16
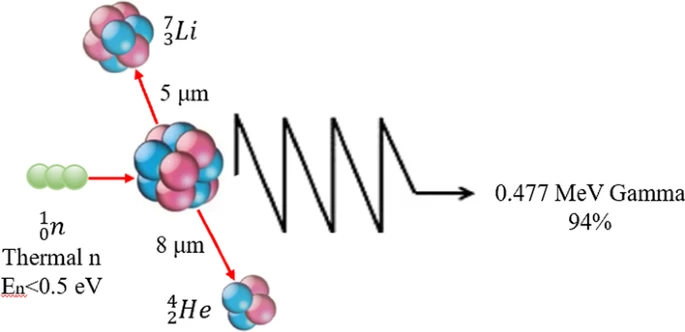
日本已上市,中国患者可赴日治疗!硼中子俘获疗法(BNCT)实现80.5%的客观缓解率,头颈癌新希望
癌症作为一种复杂的疾病,严重威胁人类健康。传统的手术、放疗和化疗常常显得力不从心,甚至可能因严重的副作用而耗尽患者最后的体力。而硼中子俘获治疗(BNCT)作为一种新兴的肿瘤治疗技术,正逐渐展现出其独特的优势和巨大的潜力,为肿瘤患者带来了新的希望。 近日,中国核技术网宣布我国硼中子俘获治疗(BNCT)技术取得重要进...
免疫管家 2025-11-28

临床试验 = 当“小白鼠”?当治疗陷入困境时:临床试验,一个不容错过的治疗新选择与免费机会
“临床试验”很多人都不陌生,有的人认为参加临床试验就是当“小白鼠”,有的人认为这是一种无私奉献的行为,还有的人认为这是一种接触前沿治疗的选择方式。那么哪种想法才是对的?接下来,康和源免疫之家(400-880-3716)就“临床试验”来与大家进行深入探讨,希望能够以一个更加全面的视角来让更多的癌症患者了解临床试验。
免疫管家 2025-11-26

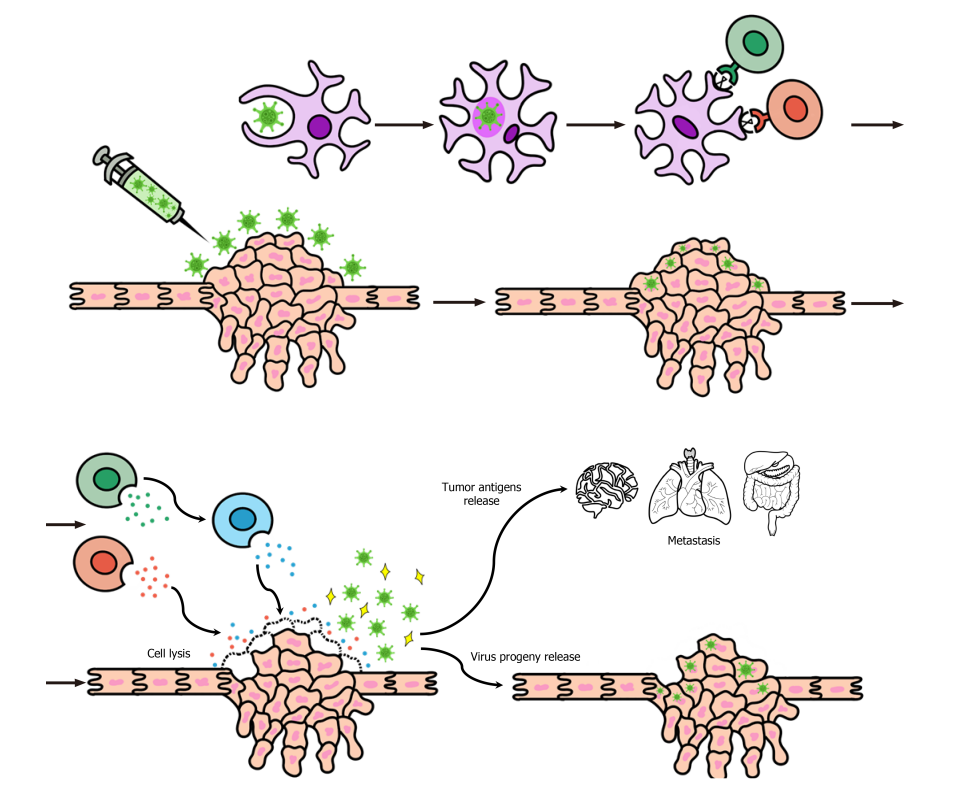
近四年病情稳定!溶瘤病毒疗法为晚期癌症患者带来新生机,一款能精准杀伤肿瘤的病毒疗法正在招募
近年来,全球癌症发病率不断上升,癌症仍然是人类健康的威胁。癌症治疗的最新发展使人们认识到病毒在癌症治疗中具有很高的潜力,使用溶瘤病毒(OVs)是治疗恶性肿瘤的一种很有前途的方法。
免疫管家 2025-11-13

华赛伯曼TIL细胞产品I期临床试验数据持续更新
11月5日,华赛伯曼宣布FAST-TIL注册I期临床试验数据在持续的随访中得到更新,1例PR和1例SD受试者转化为CR和PR疗效,CRR20%,ORR达到50%!中位随访已超过5.5个月,mPFS仍未达到!更高的深度缓解率显示出FAST-TIL强劲的体内持续杀伤肿瘤能力。
免疫管家 2025-11-05

七年无癌!美国顶级癌症中心报道:CAR-NK疗法为晚期淋巴瘤患者带来“完美”缓解
首先我们先来认识人体内的自然杀手-NK细胞。自然杀伤(NK)细胞是与细胞毒性T淋巴细胞类似的效应细胞。而与T细胞需要“训练”才能识别特定目标不同,NK细胞是免疫系统中的“快速反应部队”,天生就能识别并清除异常细胞,包括癌细胞。 传统自体CAR-T疗法存在若干局限性,采集、改造并回输患者自身T细胞需要个体化定制生产...
免疫管家 2025-11-05