相关推荐

CAR-T产品FKC889药品注册申请获国家药监局受理
9月24日,国家药品监督管理局药品审评中心(CDE)显示:复星凯瑞的第二款CAR-T产品布瑞基奥仑赛注射液(项目代号FKC889)的药品注册申请获受理,本次申报适应症为复发或难治性前体B细胞急性淋巴细胞白血病(ALL)成人患者。
免疫管家 2025-09-25

超90%的患者肿瘤缩小!CAR-T疗法不仅治血癌,卵巢癌也有效!晚期患者也能实现肿瘤消失
自2017年美国食品药品监督管理局(FDA)批准首个嵌合抗原受体T细胞(CAR-T)疗法以来,CAR-T治疗对于白血病、淋巴瘤和骨髓瘤等某些血癌具有革命性意义。
免疫管家 2025-08-26

纳基奥仑赛注射液纳入突破性治疗
8月12日,国家药品监督管理局药品审评中心(CDE)显示:合源生物自主研发的源瑞达®(纳基奥仑赛注射液,曾用名:赫基仑赛注射液)纳入突破性治疗,用于治疗儿童复发或难治性B细胞急性淋巴细胞白血病(r/r B-ALL)。
免疫管家 2025-08-21
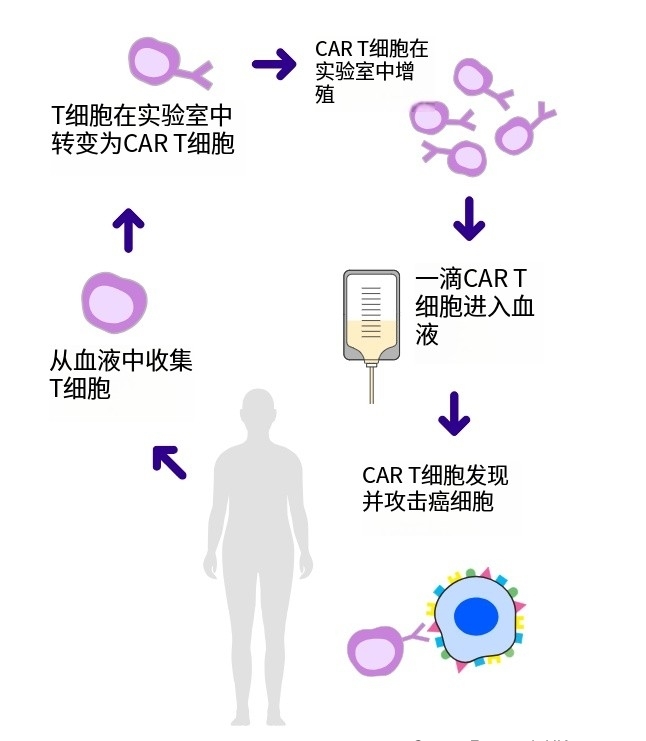
CAR-T细胞疗法KTE-X19(Brexu-cel)中国研究在2025 EHA公布
2025年欧洲血液学协会年会(EHA)年会于2025年6月12日至15日在意大利米兰盛大举行。EHA是欧洲乃至全球血液学领域最具影响力的学术会议之一,每年都会吸引来自世界各地的血液学专家、研究人员、临床医生和行业代表参加。会议内容包括最新的血液学研究进展、临床试验结果、治疗指南更新、技术创新等,是血液学领域交流和展示前...
免疫管家 2025-06-18

惊爆!国内外CAR-T细胞疗法在癌症治疗领域“狂飙”,骨髓瘤、白血病、淋巴瘤患者的“救命稻草”!
近日,科济药业开发的通用型BCMA CAR-T实现首例入组多发性骨髓瘤患者达到严格意义上的完全缓解(sCR)和微小残留病(MRD)阴性。
免疫管家 2025-03-04

永泰瑞科CAR-T-19注射液拟纳入突破性治疗品种
12月3日,国家药品监督管理局药品审评中心(CDE)显示:永泰瑞科申请的抗CD19单链抗体嵌合抗原受体T细胞注射液拟纳入突破性治疗品种,拟定适应症为25岁(含)以下CD19阳性复发/难治B细胞急性淋巴细胞白血病。
免疫管家 2024-12-04

重磅!新一代CAR-T疗法剑指白血病,白血病患者迎来“生命之光”?
11月8日,美国食品药品监督管理局(FDA)批准新一代CAR-T细胞疗法obecabtagene autoleucel(Aucatzyl,obe-cel)用于治疗复发或难治性B细胞急性淋巴细胞白血病(ALL)成人患者。Aucatzyl是Autolus Therapeutics研发的靶向CD19的CAR-T细胞疗法,据介...
免疫管家 2024-11-12

又一款CAR-T细胞疗法获批!B细胞急性淋巴细胞白血病患者获益
11月8日,美国食品药品监督管理局(FDA)批准新一代 CAR-T 疗法obecabtagene autoleucel(Aucatzyl,obe-cel )用于治疗复发或难治性 B 细胞急性淋巴细胞白血病 (ALL) 成人患者。据介绍,Aucatzyl是获美国FDA批准的首个无需风险评估缓解策略计划(REMS)的CAR...
免疫管家 2024-11-11

CAR-T疗法成功挽救淋巴瘤患者生命,并助力其考上大学!血液系统肿瘤的“救星”
近期,广州医科大学附属第五医院血液科收到了1位伯基特淋巴瘤患者送来的鲜花和锦旗以此来感谢医护人员挽救自己的生命,同时也分享了自己成功收到大学录取通知书圆了大学梦的喜悦。
免疫管家 2024-09-05

93%的儿童肿瘤消失!CAR-T疗法在血液肿瘤领域闪闪发光
近日,Orgenesis宣布靶向CD19的CAR-T疗法ORG-101在CD19阳性的B细胞急性淋巴细胞白血病(B-ALL)患者中的真实世界研究取得积极临床试验结果。
免疫管家 2024-09-03