相关推荐
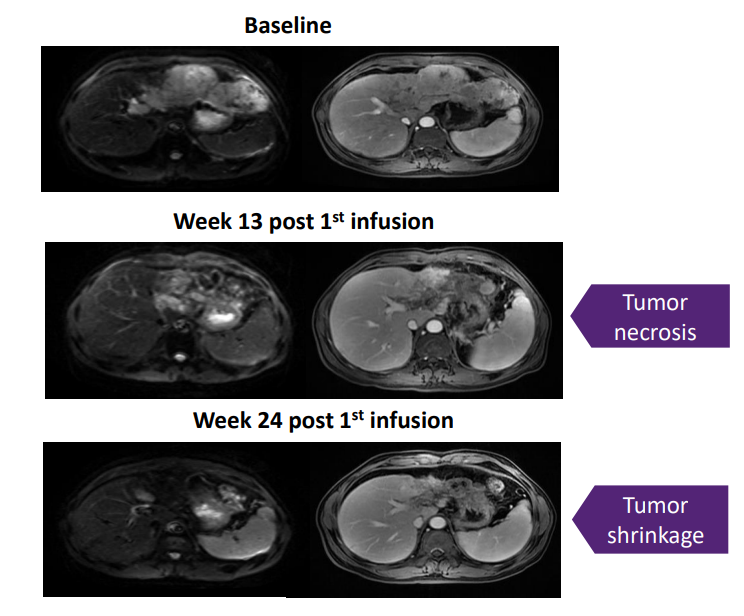
44周完全缓解!国产CAR-T疗法在胃癌、胰腺癌领域连传捷报,为实体瘤患者带来治愈曙光
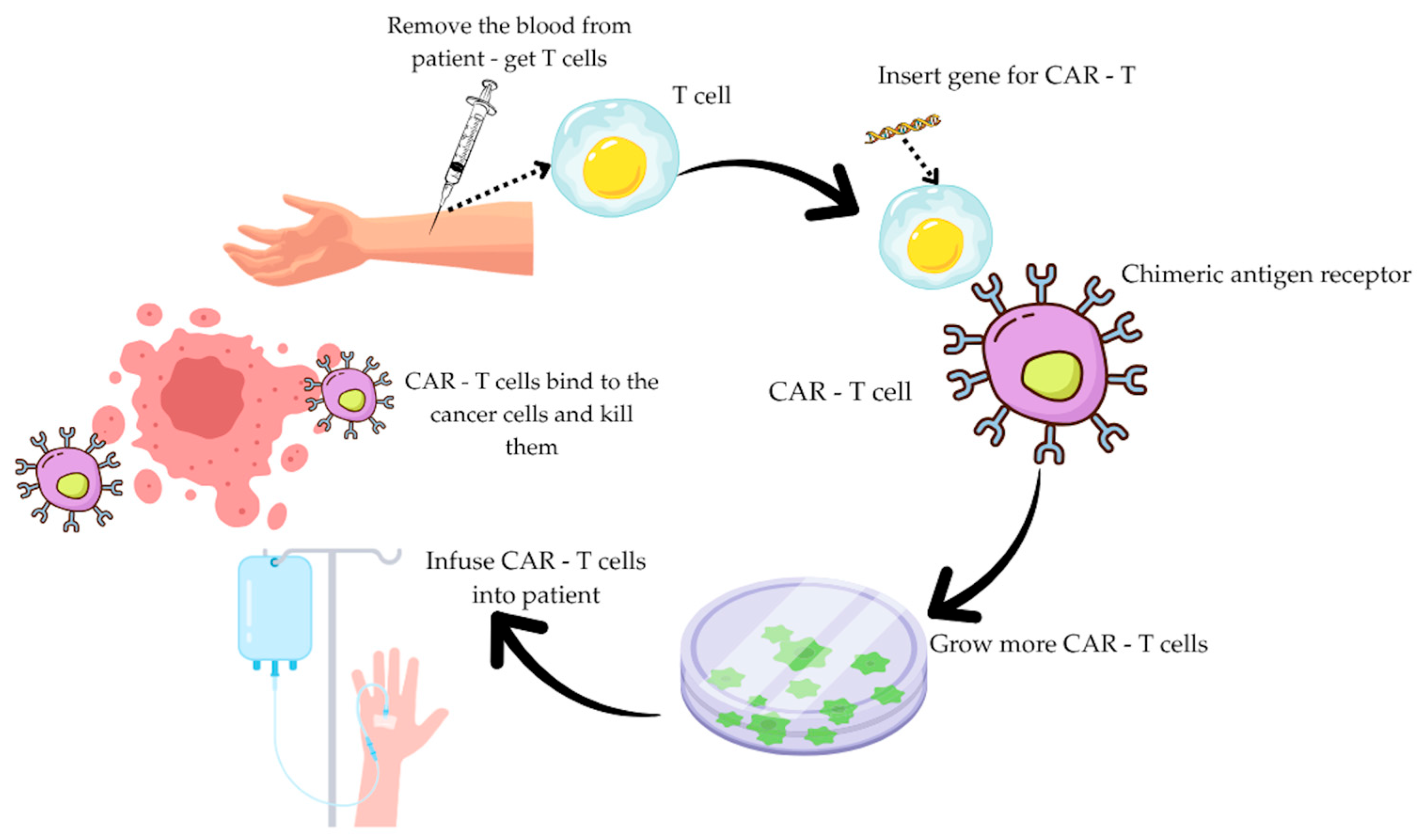
CAR-T细胞治疗是一种使用患者自身T细胞来对抗癌症的免疫疗法。T细胞在免疫系统中发挥着至关重要的作用,是人体抵御感染和疾病的防御手段。
免疫管家 2025-09-30

CAR-T产品FKC889药品注册申请获国家药监局受理
9月24日,国家药品监督管理局药品审评中心(CDE)显示:复星凯瑞的第二款CAR-T产品布瑞基奥仑赛注射液(项目代号FKC889)的药品注册申请获受理,本次申报适应症为复发或难治性前体B细胞急性淋巴细胞白血病(ALL)成人患者。
免疫管家 2025-09-25
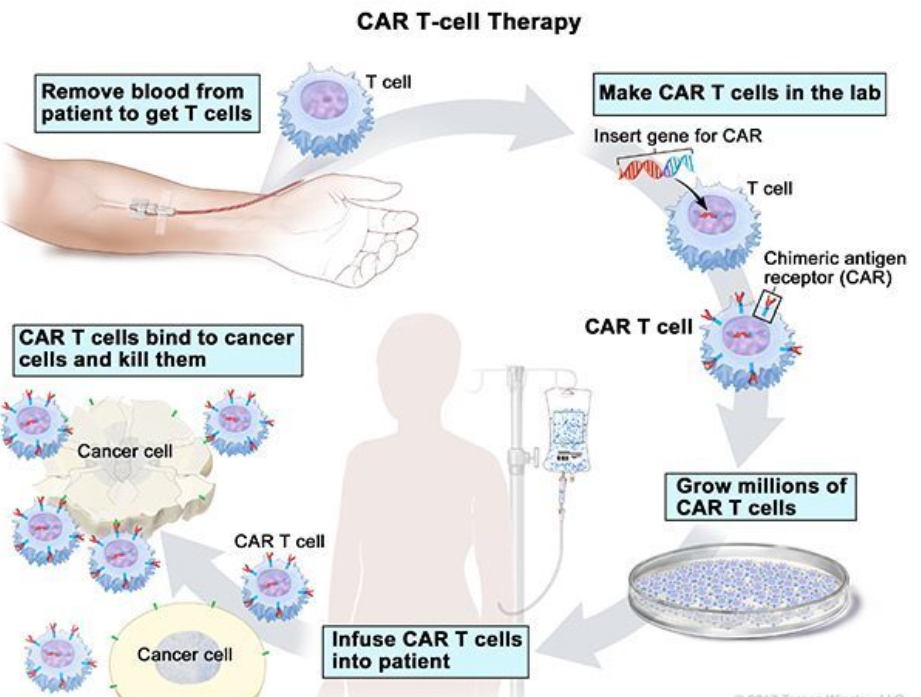
CAR-T产品IMC002 III期确证性临床研究全国启动
近日,由易慕峰生物主办的“一项在既往接受过至少二线治疗的CLDN18.2表达阳性的不可手术局部晚期或转移性胃或胃食管结合部腺癌成人受试者中比较IMC002与研究者选择的治疗的疗效和安全性的多中心、随机、对照、开放性III期确证性临床研究”全国研究者会成功召开。
免疫管家 2025-09-25

无癌生存超5年、100%缓解!CAR-T疗法交出惊人答卷,为癌症患者带来长期生存希望
当首位接受CAR-T细胞治疗的白血病儿童艾米莉·怀特(Emily Whitehead)成功实现完全缓解(CR)时,CAR-T细胞治疗以前所未有的革命性姿态宣布了癌症治疗新时代的到来,这一成功进一步加速了2017年全球首款CAR-T药物Kymriah的获批上市,开启了癌症免疫治疗的新时代。
免疫管家 2025-09-23

75个月无复发生存!癌症疫苗迎来高光时刻:晚期癌症患者实现长期存活,最长已超6年
近年来,免疫疗法发展迅速,为癌症治疗提供了超越手术,传统化疗和放疗的新方法,开创了癌症治疗的新时代。免疫检查点抑制剂和细胞免疫治疗是近年来的研究热点。癌症疫苗作为一种研究中的免疫疗法,在临床试验中也得到了广泛的研究,并显示出广阔的应用前景。
免疫管家 2025-09-22

泽沃基奥仑赛注射液用于多发性骨髓瘤的长期随访更新结果亮相2025年IMS年会
9月18日,科济药业宣布,赛恺泽®(泽沃基奥仑赛注射液)用于复发/难治性多发性骨髓瘤患者的I期临床试验的长期随访更新结果,已在第22届国际骨髓瘤学会(IMS)年会上展示。
免疫管家 2025-09-18
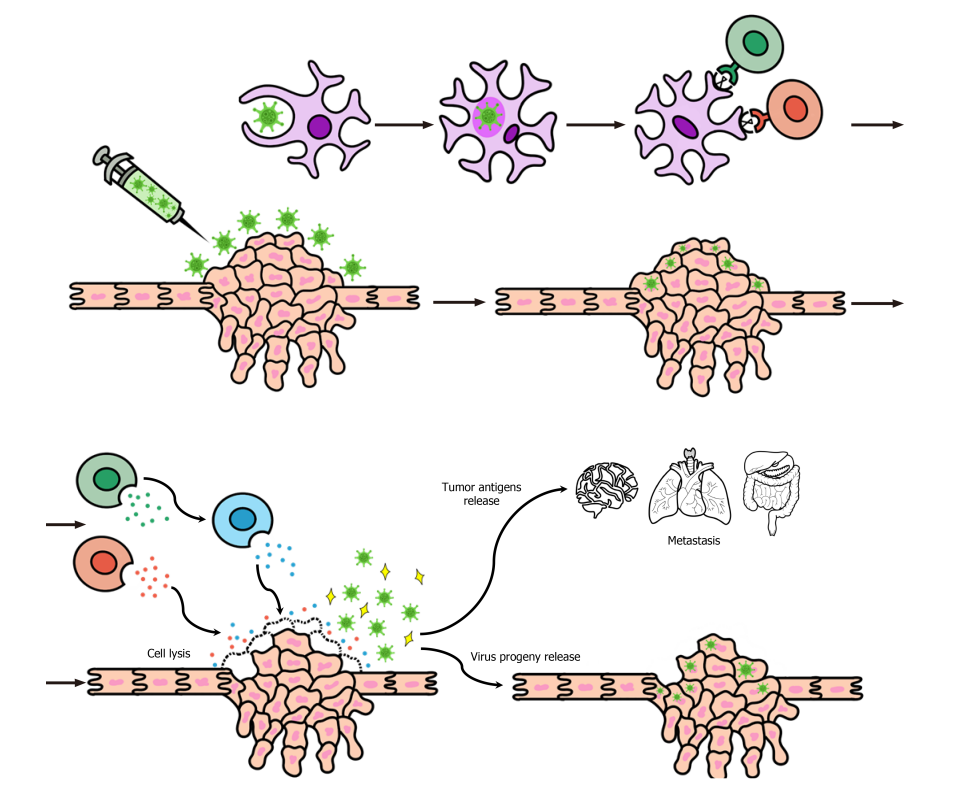
生存期超3年!国内研究登顶国际期刊:新型溶瘤病毒为晚期肝癌患者带来生存曙光
近日,中山大学附属第三医院研究人员在《Clinical Cancer Research》发表了M1-c6v1溶瘤病毒联合卡瑞利珠单抗和阿帕替尼在晚期肝细胞癌(HCC)患者中的临床疗效(NCT04665362)。
免疫管家 2025-09-18

中国原研CAR-T疗法首例患者无癌生存突破5年
2025年9月17日,上海邦耀生物(BRL Biotech)发布重大临床里程碑:其自主研发的全球新一代CD19靶向PD1-CAR-T产品BRL-201(全球首款非病毒定点整合CAR-T疗法),在治疗复发难治性恶性淋巴瘤领域取得突破性成果——首位接受治疗的患者孙先生已保持无癌状态超过5年,且最新随访显示其仍处于完全缓解(...
免疫管家 2025-09-17
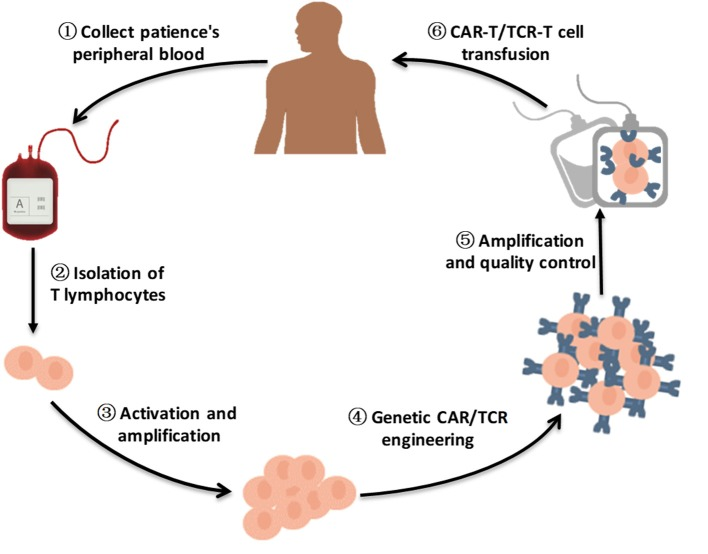
中位生存期近3年!TCR-T疗法为肝癌、肉瘤等患者打开生命新大门!,癌细胞无处可逃
近年来,癌症治疗取得了很大进展。免疫疗法是发展迅速、引人注目的领域它为患有各种实体瘤和血液系统癌症的患者提供了新的治疗选择。其中,TCR-T细胞疗法作为一种新型的过继性细胞免疫疗法,显示出巨大的应用潜力。
免疫管家 2025-09-17

生存期超4.5年!CAR-T疗法为骨髓瘤患者带来深度缓解与长期生存希望,92%患者肿瘤缩小或消失!
长期以来,癌症一直是人类健康的重大威胁,给无数患者及其家庭带来了沉重的打击。然而,医学的进步从未停止,嵌合抗原受体T细胞(CAR-T)疗法的出现为癌症患者带来了新的希望。
免疫管家 2025-09-16