相关推荐
最长缓解4年!NTRK融合肿瘤儿童迎来长期生存机会,有机会接受前沿治疗
近日,《Frontiers in Oncology》发表了拉罗替尼治疗NTRK融合肿瘤儿童的病例报告。
免疫管家 2025-09-30

震惊!NTRK融合基因“风暴”来袭,拉罗替尼、恩曲替尼如何改写肿瘤治疗版图
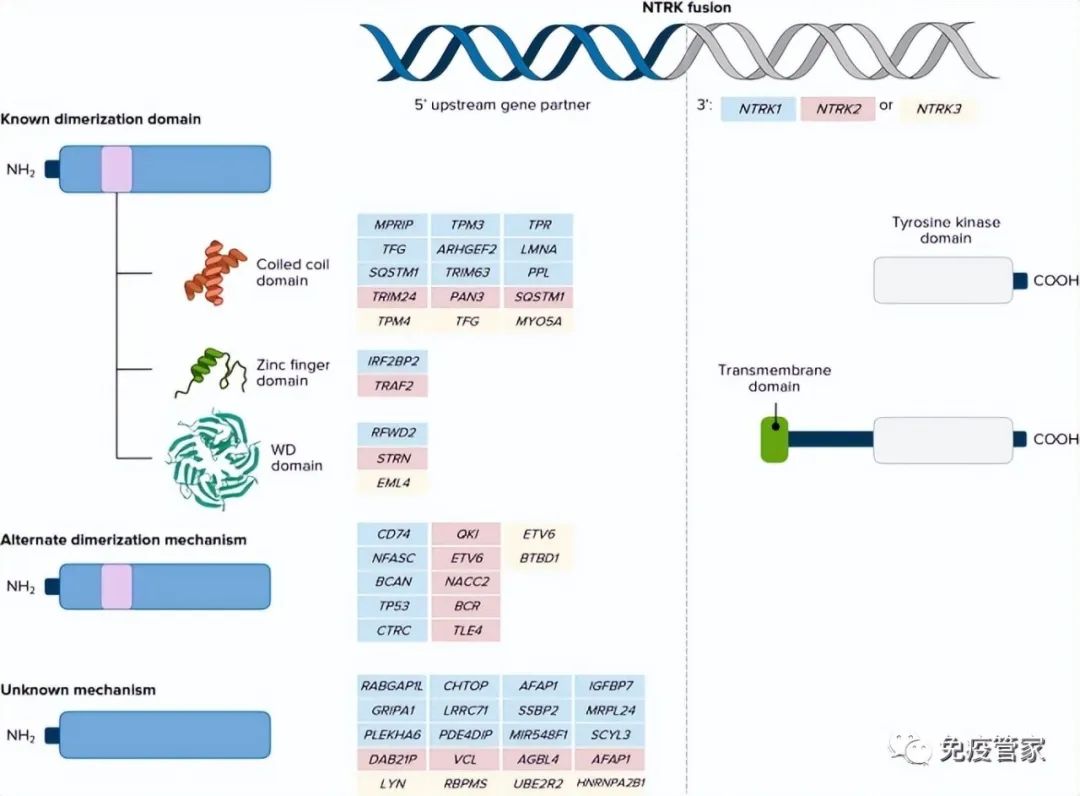
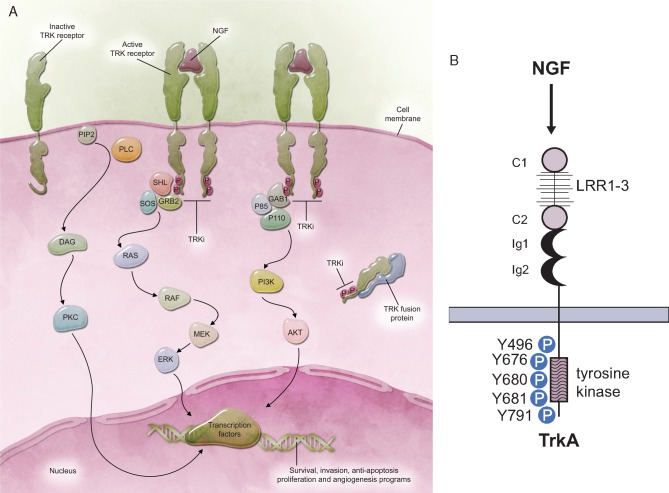
神经营养原肌球蛋白激酶受体(NTRK)是近年来肿瘤研究领域的热点之一,包含NTRK1、NTRK2 和 NTRK3,分别编码原肌球蛋白受体激酶(TRK)家族TRKA、TRKB 和 TRKC 三种蛋白。任何一个基因如果和其他的基因发生了融合突变,那么就会导致癌细胞异常活性,驱动肿瘤的发生。
免疫管家 2025-03-25

半年时间肿瘤缓解54%!瑞普替尼获批用于NTRK融合患者,疾病控制率高达83%!
6月13日,瑞普替尼(repotrectinib)获美国食品药品监督管理局(FDA)批准用于治疗12岁及以上具有神经营养性酪氨酸受体激酶(NTRK)基因融合的局部晚期、转移性或手术切除可能导致严重疾病、治疗后病情进展或没有令人满意的替代疗法的成人和儿童实体瘤患者。
免疫管家 2024-06-18