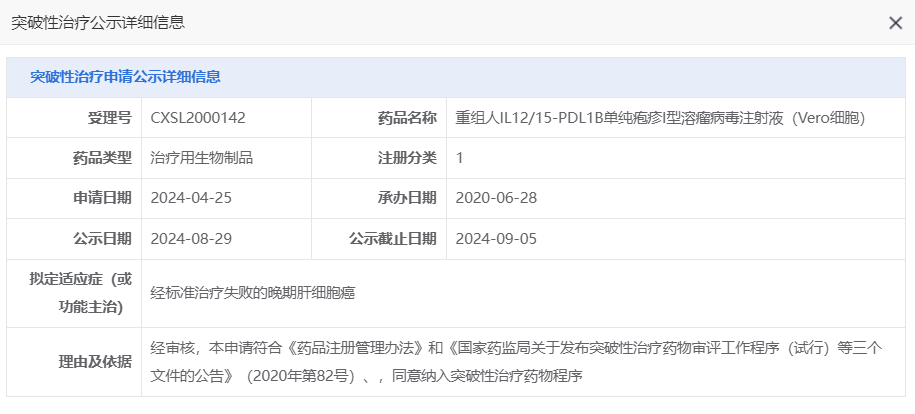
8月29日,国家药品监督管理局药品审评中心(CDE)公示:中生复诺健生物申报的重组人IL12/15-PDL1B单纯疱疹I型溶瘤病毒注射液(Vero细胞)VG161拟纳入突破性治疗品种,拟用于治疗经标准治疗失败的晚期肝细胞癌。
VG161是中生复诺健生物原创开发的一种重组人IL12/15-PDL1B单纯疱疹I型溶瘤病毒注射液(Vero细胞),是一种单纯疱疹病毒1型病毒(HSV-1)。
2024年美国肿瘤学会年会(ASCO)报告了VG161在既往接受过包括检查点抑制剂在内的二线治疗失败的肝细胞癌(HCC)患者中的临床数据。

该试验共纳入40例肝细胞癌患者,结果显示:疾病控制率(DCR)为 60%,既往至少接受3个月接受检查点抑制剂的患者,中位总生存期(OS)为17.30个月。数据表明,VG161单药治疗肝细胞癌具有显著的临床效果。
2024年4月3日,《Oncology Letters》报告了VG161治疗肉瘤的临床病例。

患者1于 2019 年 11 月确诊为软骨肉瘤伴肺转移,患者接受手术以及放射治疗,但病情进展,于是患者接受VG161治疗,治疗后患者病情稳定,目标病灶相比于基线最大缩小17.96%,无进展生存近1年。

患者2于2011年8月诊断为血管外皮瘤,既往接受了手术、放疗、靶向治疗以及溶瘤病毒T3011治疗等,遗憾的是,患者病情仍旧疾病进展,并观察到五个分别位于右腋窝、右锁骨上、右大腿后部、右膈肌和前纵隔淋巴结的靶病变,于是患者接受VG161治疗。治疗后患者病情稳定,无进展生存超11.9个月。
这两个病例表明,VG161可有望成为治疗肉瘤的有效药物。
目前溶瘤病毒针对实体瘤的临床试验正在全国范围内寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
项目名称:重组人IL-21溶瘤痘病毒注射液(hV01)治疗晚期恶性实体瘤的I期临床研究
部分入选标准:
1.年龄18~75周岁;
2.晚期恶性实体瘤患者;
3.预计生存期≥3个月;
4.体力状态评分(ECOG)0-1分。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。

相关推荐
随便看看
- “敌人变朋友?”溶瘤病毒疗法势不可挡,在不伤害健康组织的情况下杀伤癌细胞
- 溶瘤痘苗病毒Olvi-Vec治疗广泛小细胞肺癌患者的1b期/2期临床试验取得积极数据
- 溶瘤病毒联合治疗方案实现一名50岁直肠癌患者病理完全缓解
- 溶瘤病毒Ad-TD-nsIL12实现复发性高级别胶质瘤患者肿瘤完全消失
- 病毒也能抗癌?溶瘤病毒多癌种齐开花,胰腺癌控制率94%、膀胱癌完全缓解率83.7%……
- 溶瘤病毒爆发惊人力量:前列腺癌、胰腺癌、肺癌、肉瘤、黑色素瘤迎突破!
- 头颈癌、黑色素瘤、肝癌……看溶瘤病毒如何挑战难治性肿瘤,实现肿瘤显著缩小甚至消失!
- CAN-3110 治疗黑色素瘤的临床前数据即将亮相SITC年会
- 将病毒转化成“合格的士兵”!溶瘤病毒疗法让她重获新生,获得长达14年生存期!
- 71%疾病控制率!这种向病毒“借力”的溶瘤病毒新疗法,正在成为击碎难治性癌症的“破局者”











