11月21日,Replimune Group宣布已向美国食品药品监督管理局(FDA)提交RP1(vusolimogene oderparepvec)的生物制品许可申请(BLA),联合PD-1抑制剂nivolumab用于治疗既往接受过PD-1靶向疗法治疗的晚期黑色素瘤成年患者。

RP1(vusolimogene oderparepvec)是Replimune的主要候选产品,基于一种专有的单纯疱疹病毒株,该毒株经过工程改造和基因武装,具有融合蛋白 (GALV-GP R-)和GM-CSF,旨在最大限度地提高肿瘤杀伤效力、肿瘤细胞死亡的免疫原性以及全身抗肿瘤免疫反应的激活。
第 39 届癌症免疫治疗学会年会(SITC 2024)上报告了 RP1 与纳武利尤单抗联合使用治疗进展或不适合抗 CTLA-4 治疗的晚期黑色素瘤患者的III期IGNYTE-3试验。
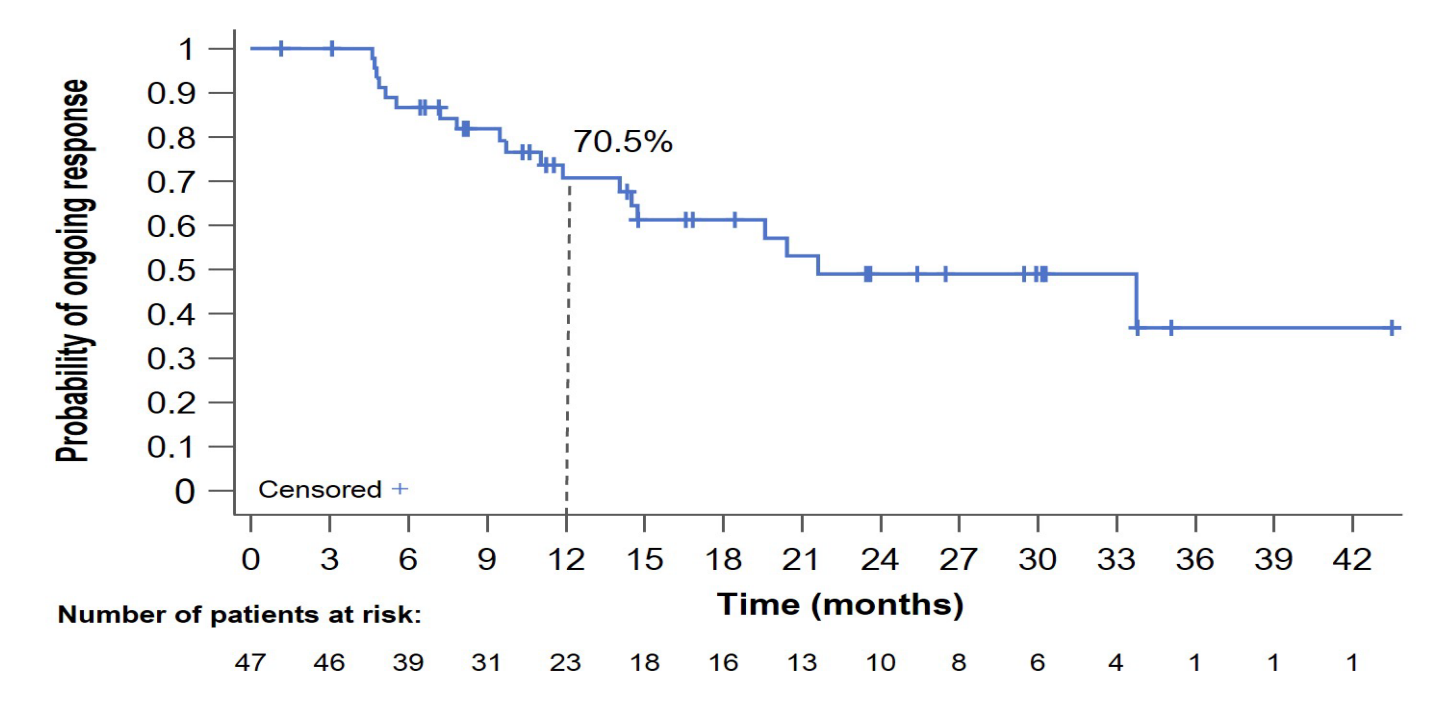
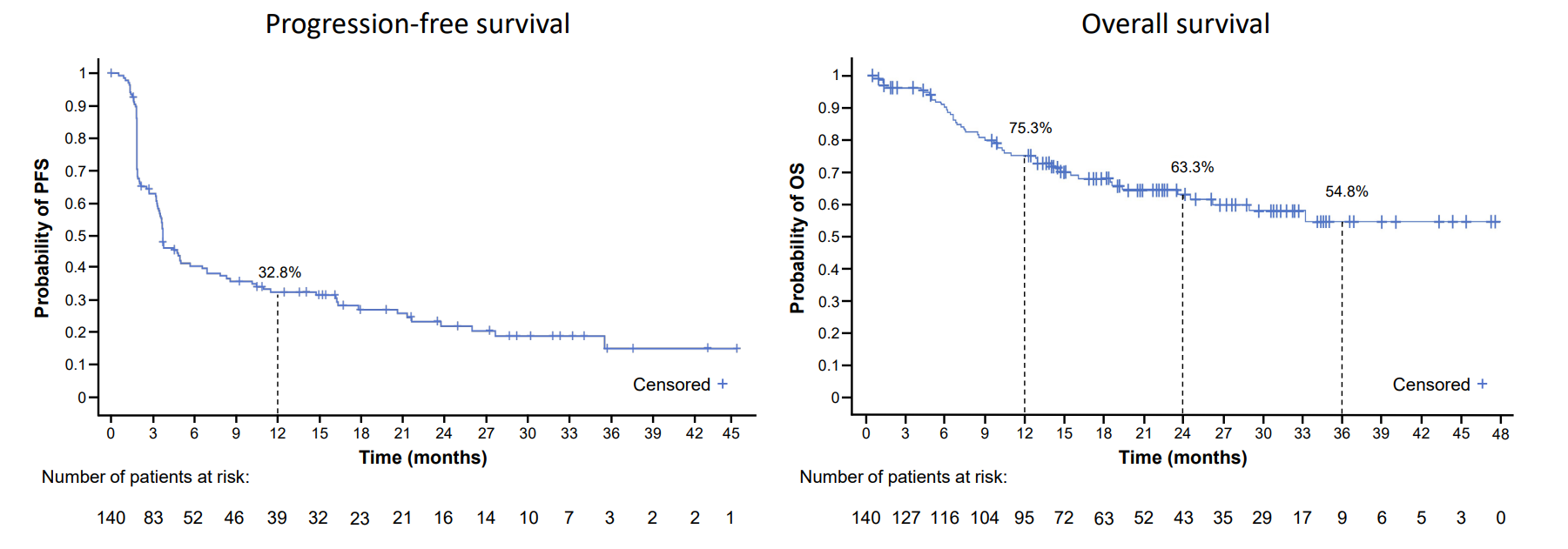
结果显示:总缓解率 (ORR) 为 33.6%,其中21例患者达到完全缓解(CR),26例患者达到部分缓解(PR),41例患者病情稳定(SD),中位反应持续时间为 21.6 个月。中位总生存期尚未达到,但 1 年、2 年和 3 年生存率分别为 75.3%、63.3% 和 54.8%。12 个月无进展生存期 (PFS) 为 32.8%,中位 PFS 为 3.7 个月。
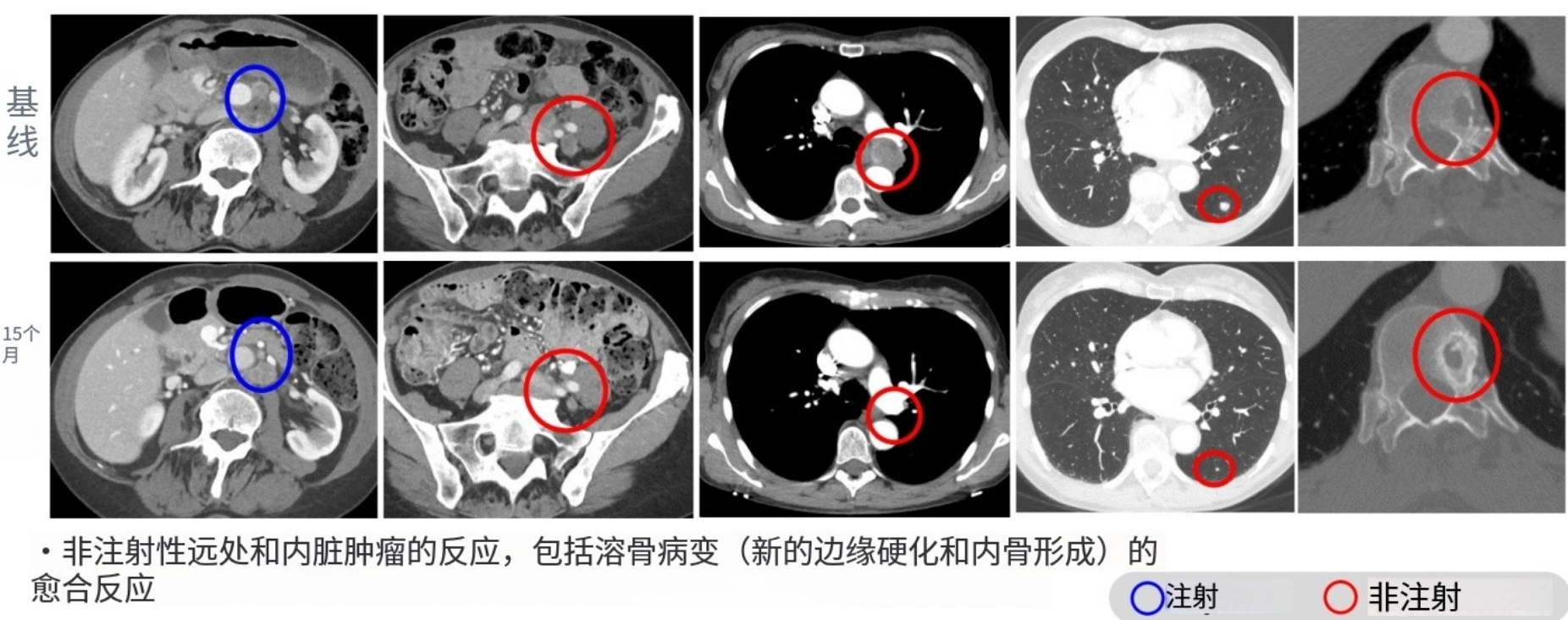
1例既往接受过阿替利珠单抗、考比替尼、伊匹木单抗等治疗方案的黑色素瘤患者,经RP1方案治疗后肿瘤缩小,具体治疗情况如下图所示:
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前溶瘤病毒有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://ir.replimune.com/news-releases/news-release-details/replimune-receives-breakthrough-therapy-designation-rp1-an
2.https://ir.replimune.com/news-releases/news-release-details/replimune-presents-late-breaking-abstract-featuring-data-ignyte
3.https://ir.replimune.com/static-files/d2e658a8-4d69-4400-9bbe-57c8ec88a482

相关推荐
随便看看
- 能与淋巴瘤抗衡的除了CAR-T外,还有溶瘤病毒
- 惊爆!溶瘤病毒产品各显神通,黑色素瘤、肛门癌、肝癌疗效超乎想象!
- 71%疾病控制率!这种向病毒“借力”的溶瘤病毒新疗法,正在成为击碎难治性癌症的“破局者”
- 以毒攻癌的奇迹正在发生!溶瘤病毒为晚期癌症患者开辟一条新的生路,12cm肿瘤近乎消失
- 溶瘤病毒候选药物BS006注射液获得临床试验许可
- 临床验证:溶瘤病毒疗法VT1093展现良好安全性及疾病控制潜力
- “以毒攻癌”!溶瘤病毒只杀癌细胞不伤正常组织?已有患者病灶缩小!溶瘤病毒治癌真相大揭秘
- CAN-3110 治疗黑色素瘤的临床前数据即将亮相SITC年会
- 中生复诺健溶瘤病毒产品-VG161用于肝癌的研究成果亮相2025 ASCO
- 无病生存!溶瘤病毒TILT-123 神奇“组合拳”让卵巢癌、黑色素瘤、甲状腺癌、胰腺癌等“节节败退”











