
近日,科济药业开发的通用型BCMA CAR-T实现首例入组多发性骨髓瘤患者达到严格意义上的完全缓解(sCR)和微小残留病(MRD)阴性。 该患者既往曾经接受过3线联合药物治疗和自体造血干细胞移植,疾病进展后接受了该CAR-T技术治疗,整体安全性良好。第28天随访疗效评估为严格意义上的完全缓解(sCR)和微小残留病(MRD)阴性。 CAR-T细胞疗法是一种完全不同于以往的治疗方式:首先,医生从患者体内将T细胞提取出体外,然后通过人类的基因工程技术对T细胞进行改造,这一操作让T细胞能够精准找到癌细胞,也就是给T细胞装上了“导航”,然后将拥有“超能力”的T细胞大量扩增,让T细胞们形成一支“抗癌军队”,最后将这支“抗癌军队”回输到患者体内。拥有“超能力”的T细胞战斗力飙升,战力满满,很快便对癌细胞进行打击,以此来恢复患者的身体健康。 目前CAR-T细胞疗法有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。 如何接受CAR-T细胞治疗 目前CAR-T细胞临床试验正在寻找B细胞淋巴瘤患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。 部分入选标准: 1.18周岁及以上成年复发或难治性B细胞淋巴瘤患者,包括大B细胞淋巴瘤(LBCL),套细胞淋巴瘤(MCL)或滤泡细胞淋巴瘤(FL)等; 2.预计生存期≥12周; 3.ASCT后疾病进展或≤12个月内复发(复发患者必须有活检证实其复发); 4.基线期ECOG(东部肿瘤协作组)评分为0或1。 临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。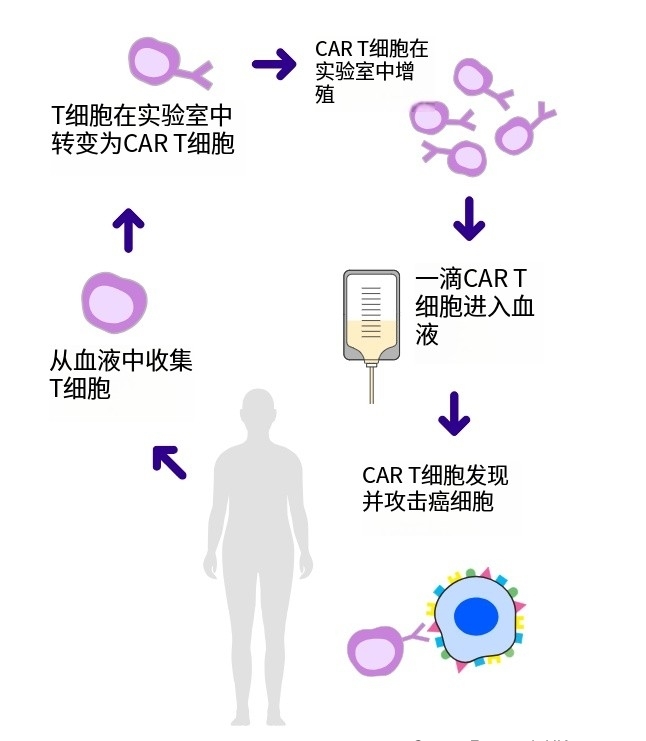



参考资料 1.https://ascopubs.org/doi/10.1200/JCO-24-01933 2.https://ascopubs.org/doi/10.1200/JCO-24-01785 3.https://www.nejm.org/doi/full/10.1056/NEJMoa2406526 4.https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(24)00746-3/fulltext 5.https://www.carsgen.com/media/0yylooxm/ct071-ash-poster_-3451.pdf 6.https://jitc.bmj.com/content/10/9/e005145
相关推荐
随便看看
- CAR-T细胞产品C-CAR031治疗鳞状细胞肺癌完成首例患者给药
- 96.3%的缓解率!CAR-T细胞疗法显示强劲疗效,为淋巴瘤、骨髓瘤患者带来长期生存希望
- 艺妙神州IM19 CAR-T细胞注射液上市许可申请获国家药监局受理
- 靶向BCMA的CAR-T细胞疗法DRL-1801在多发性骨髓瘤患者中取得积极结果
- 同种异体靶向 CD7 靶向 CAR-T 细胞疗法 WU-CART-007 的关键试验中实现首批患者给药
- 告别终身服药?CAR-T疗法再封神:不仅治癌,更能跨界到红斑狼疮,让自身免疫病患者长期无药缓解
- CD19 CAR-T疗法 ORG-101在B细胞急性淋巴细胞白血病中取得积极结果
- 抗CD19 CAR-T细胞疗法治疗B细胞非霍奇金淋巴瘤和慢性淋巴细胞白血病的生存情况及10年随访公布
- 国内首个!CAR-T细胞疗法瑞基奥仑赛获批用于治疗套细胞淋巴瘤,客观缓解率为81.36%
- CAR-T疗法2.0版来了!“体内CAR-T”疗法,告别百万天价与漫长等待!体内直接编程,癌细胞6小时清零?











