作者:小编
更新时间:2025-11-18
点击数:
11月17日,华赛伯曼宣布FAST-TIL(HS-IT101)治疗晚期黑色素瘤关键II期临床试验获得获批。
2025年欧洲肿瘤内科学会(ESMO)年会上华赛伯曼公布了其自主研发的FAST-TIL产品(HS-IT101注射液)的I期临床试验数据。
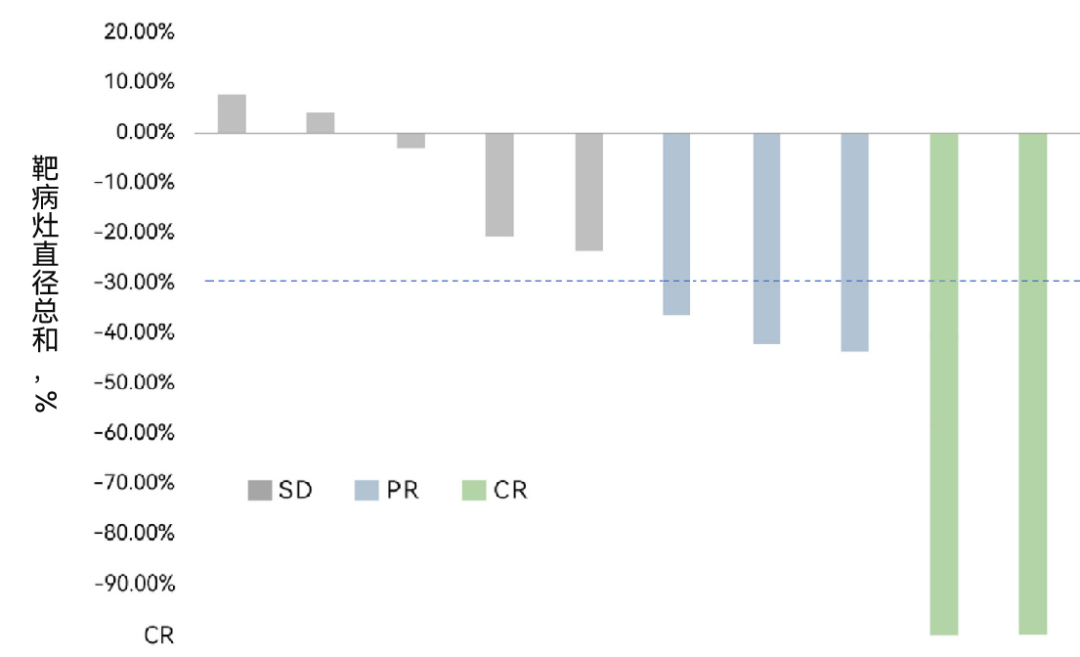
在针对晚期黑色素瘤的10例可评估患者中,HS-IT101取得了40%的客观缓解率(ORR),其中1例完全缓解(CR),3例部分缓解(PR),疾病控制率(DCR)更是达到了惊人的100%。尤为值得一提的是,这个40%的客观缓解率,已经显著超越了目前全球唯一获批的TIL产品Lifileucel(Amtagvi)在其关键临床试验中报告的31.4%的缓解率。

之后1例部分缓解(PR)和1例病情稳定(SD)患者转化为完全缓解(CR)和部分缓解(PR)疗效。这意味着,疗效并非静止不变,随着时间的推移,FAST-TIL在患者体内持续发挥作用,使得部分缓解(PR)的患者达到了更高的完全缓解(CR)标准,甚至疾病稳定(SD)的患者也进入了部分缓解(PR)的队列。
目前HS-IT101正在国内开展临床试验,如果你或身边的黑色素瘤患者正面临治疗困境,不妨尝试一下HS-IT101的临床试验。参加临床试验可以免费接受治疗。部分入选标准如下:
1.至少存在2个以上病灶,且至少1个病灶位于浅表部位(方便肿瘤组织采集);
2.年龄在18-75岁之间;
3.ECOG评分≤1分(即日常生活能力基本正常,能从事轻体力活动);
4.预期生存时间≥3个月。
如果您或家人正在为黑色素瘤治疗寻找新的方向,可考虑咨询HS-IT101临床试验。有意向的患者可直接致电400-880-3716,提交病例资料、治疗经历等信息进行初步筛选。

相关推荐
随便看看
- 英国癌症患者抗癌奇迹!TIL细胞治疗6周肿瘤消失!全球首款TIL疗法长期数据公布,近1/5患者生存超5年
- 关于肿瘤浸润淋巴细胞(TIL)疗法:胆管癌患者的十年“奇迹”
- 华赛伯曼HS-IT101又一例多线治疗患者达到缓解
- 癌症治疗又一“王炸”!TIL疗法正式登场:面对肺癌、宫颈癌、黑色素瘤,缓解时间超36个月
- 肿瘤减少57.1%!TIL疗法惠及黑色素瘤、宫颈癌、肺癌、肝癌、乳腺癌……疾病控制率高达90%
- HS-IT101治疗晚期黑色素瘤关键II期临床试验获得获批
- 官方受理!国内TIL疗法密集爆发:黑色素瘤之后,肺癌、卵巢癌、肝癌也迎来转机!
- 中位缓解长达36.5个月!TIL疗法让部分实体瘤患者肿瘤完全消失,疗效持久,带来长期生存曙光
- Amtagvi(lifileucel)在加拿大获批上市
- TILs细胞











