
近日,IBI363拟纳入突破性治疗,用于既往未经过系统性治疗的不可切除局部晚期或转移性肢端型及黏膜型恶性黑色素瘤。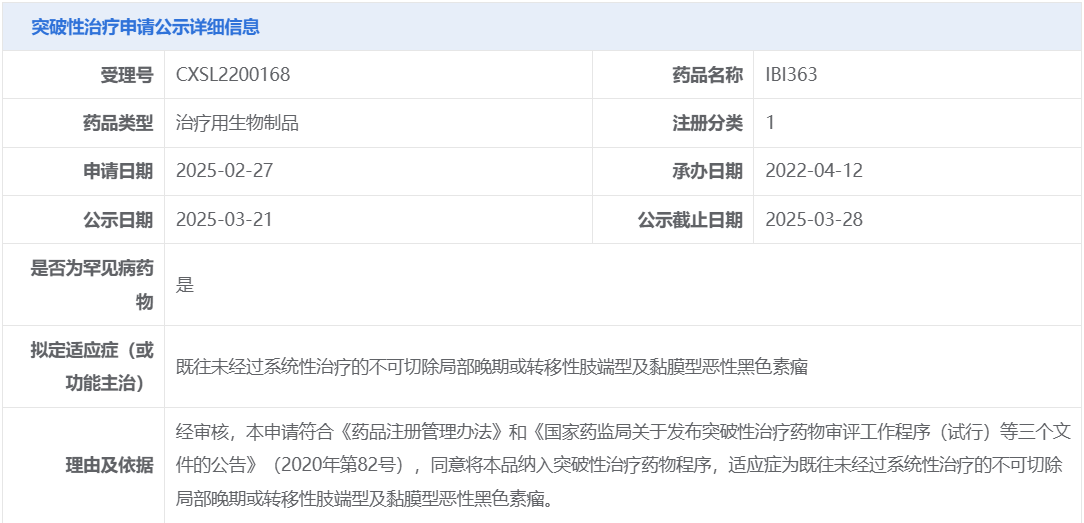
IBI363是由信达生物自主研发的全球首创PD-1/IL-2α-bias双特异性融合蛋白,2024年美国临床肿瘤学会(ASCO)年会上公布了IBI363治疗晚期黑色素瘤的I期临床研究(NCT05460767)数据。结果显示:37例既往接受过免疫治疗的黑色素瘤患者中,1例患者达到完全缓解(CR),10例患者达到部分缓解(PR),73.0%的患者病情得到控制。
8例既往未经过免疫治疗的黏膜型黑色素瘤患者中,75.0%的患者肿瘤缩小或消失,其中1例患者最佳疗效为完全缓解(CR),5例患者最佳疗效为部分缓解(PR),疾病控制率(DCR)高达100%。
黑色素瘤是一种起源于皮肤色素生成细胞即黑色素细胞的皮肤癌,是一种恶性程度较高的侵袭性疾病。随着靶向治疗、免疫治疗、生物治疗的不断发展,晚期黑色素瘤的治疗得到显著进展。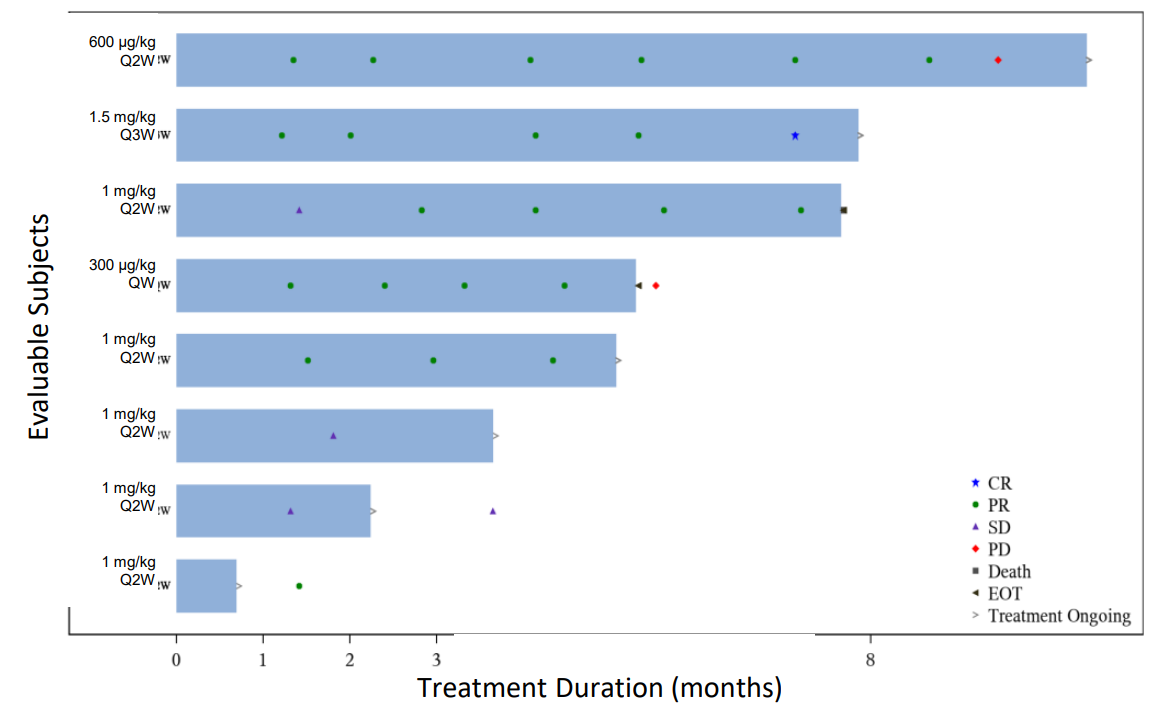
TIL细胞疗法作为一种新兴的个体化免疫治疗技术,在黑色素瘤治疗中具有强大的疗效。
近日,世界最著名医疗机构之一的克利夫兰诊所中有一位黑色素瘤患者接受了肿瘤浸润淋巴细胞(TIL)治疗,并得到了显著效果。2014年,该患者被诊断出患有结膜黑色素瘤,在接受手术切除肿块4年后复发。随后,该患者在两年内接受了免疫治疗药物 ipilimumab 和 nivolumab。然而,疾病持续进展,并且黑色素瘤已经转移到腹部的淋巴结。
经核实,该患者非常适合TIL治疗。于是2024 年 8 月,她接受了TIL细胞输注,并且在输注期间没有产生严重的副作用。在TIL细胞输注后,该患者肿瘤持续缩小。
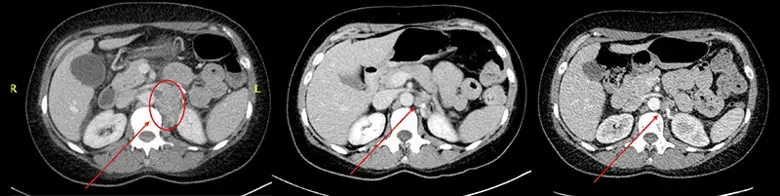
目前,TIL细胞疗法已经批准一款lifileucel(Amtagvi)用于黑色素瘤。这款Amtagvi临床数据显示:66例接受lifileucel治疗参与疗效评估的患者,有22例患者实现部分缓解(PR),2例患者实现完全缓解(CR),29例患者病情稳定(SD)。中位总生存期为17.4个月,一年总生存率(OS)为58%。
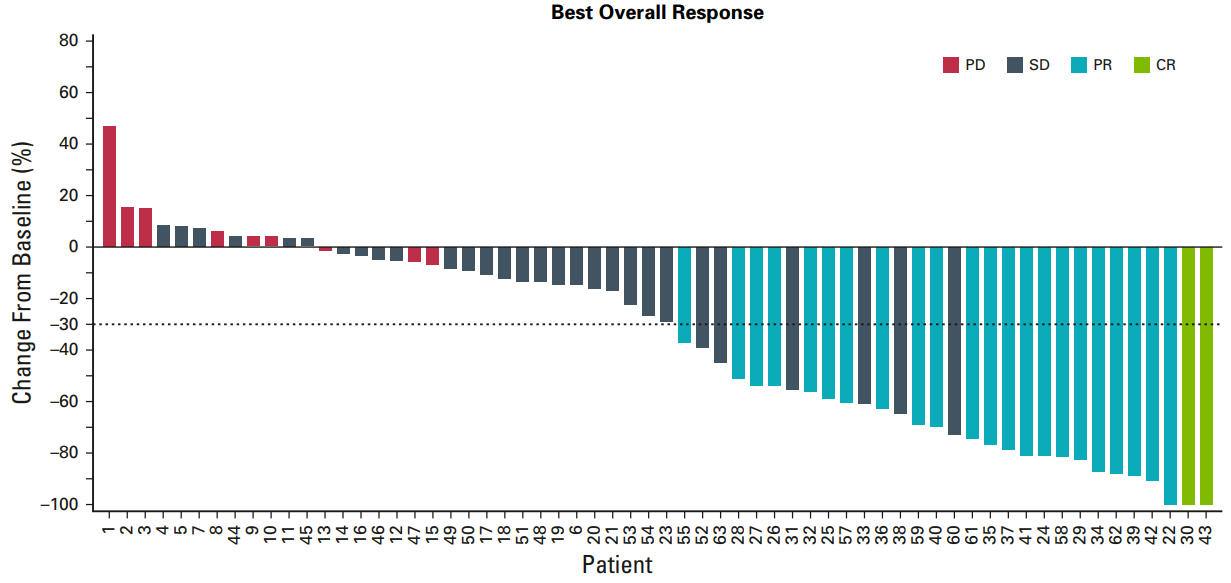
目前国内还未批准TIL细胞产品上市,但患者可选择参加临床试验来接受TIL细胞治疗。临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。国内多家权威三甲医院已开展TIL细胞疗法针对黑色素瘤的临床试验,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。正在寻找新治疗方式或已广泛转移且对手术和常规治疗反应不佳的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
溶瘤病毒是一类能选择性地感染并杀死肿瘤细胞而不损伤正常细胞的天然或重组病毒。随着基因工程技术的发展,科学家开始改造病毒,增强其靶向性和安全性。直到现在,溶瘤病毒疗法已经在癌症治疗中展现出巨大潜力。
BT-001是一种溶瘤性牛痘病毒,2024年欧洲肿瘤内科学会(ESMO)上报告了BT-001联合帕博利珠单抗用于晚期实体瘤患者的临床(NCT04725331)结果。共13例黑色素瘤患者、5例肉瘤以及6例其他肿瘤患者接受治疗,结果显示:BT-001单药治疗组18例患者中有4例患者免疫稳定(iSD),BT-001联合帕博利珠单抗组有2例实现免疫部分缓解(iPR)。
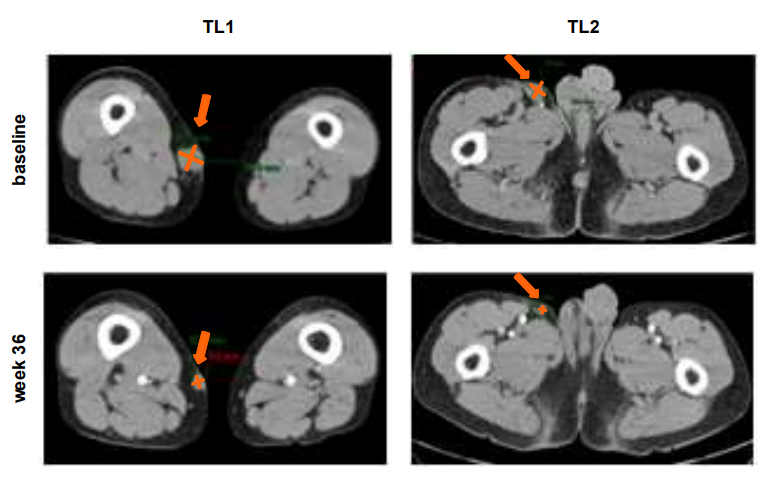
一名黑色素瘤患者,既往接受纳武利尤单抗联合伊匹单抗、度伐利尤单抗+Ceralasertib治疗。BT-001治疗后目标病灶逐渐缩小,并达到部分缓解(PR)。
mRNA疫苗是一种新兴的癌症治疗策略,信使RNA(mRNA)会对体内的免疫细胞进行抗病毒训练,提前备战以对抗外来入侵者来预防感染。所以,当一个人在接受mRNA疫苗接种后,接触到病毒时,就可以快速识别病毒,并将其标记销毁。
mRNA-4157是一种新型的基于信使RNA(mRNA)的个体化疫苗,在黑色素瘤中具有显著生存效益。2024年美国临床肿瘤学会(ASCO)年会上公布了mRNA-4157(V940)联合帕博利珠单抗用于完全切除后的高危III/IV期黑色素瘤的一项IIb期研究三年随访数据。结果显示:mRNA-4157(V940)联合帕博利珠单抗的2.5年无复发生存率为74.8%,帕博利珠单抗的2.5年无复发生存率为55.6%,复发或死亡风险降低了49%,远处转移或死亡的风险降低了62%。mRNA-4157(V940)联合帕博利珠单抗2.5年的总生存期(OS)高达96.0%,而单独帕博利珠单抗组2.5年的总生存期略低于联合治疗组(90.2%)。
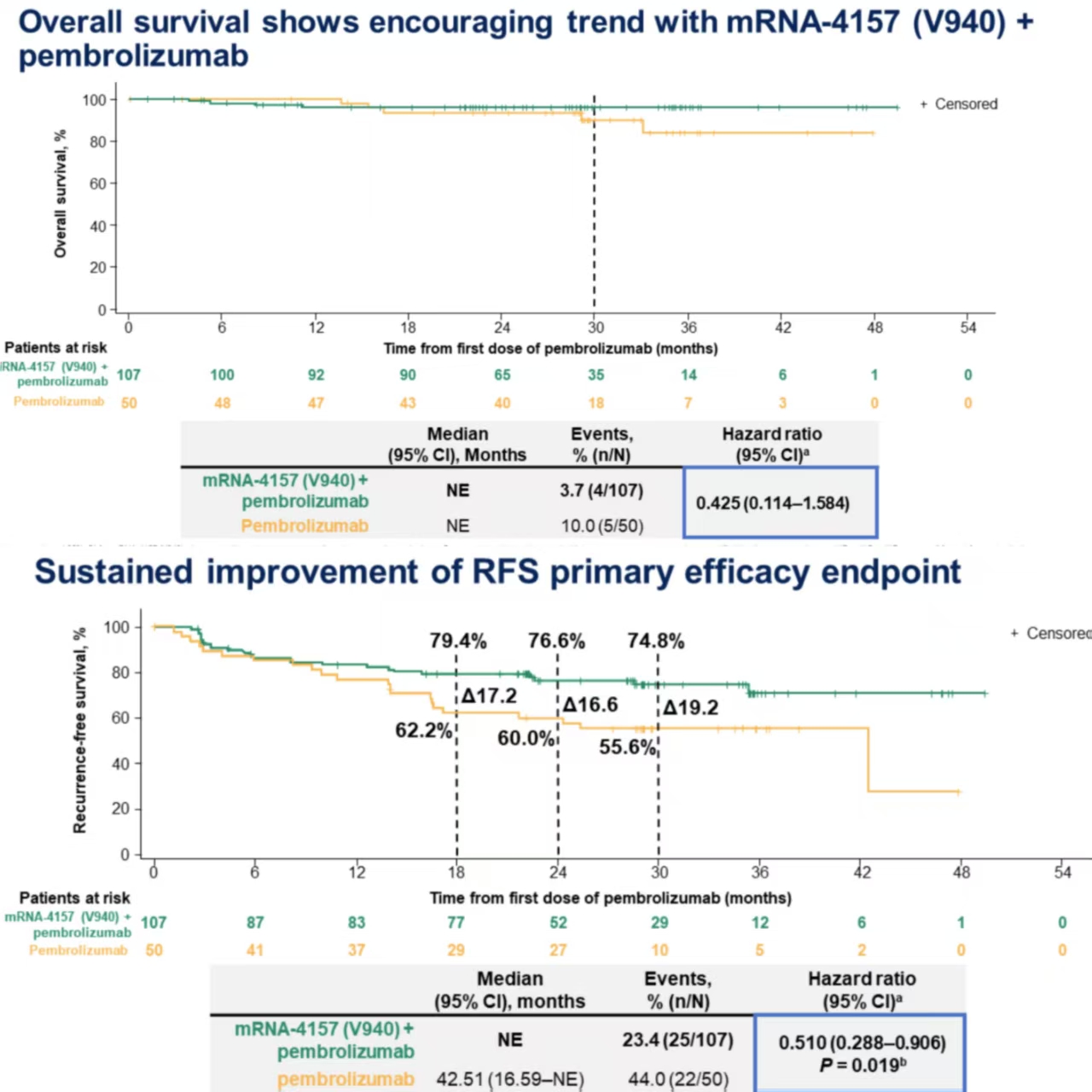
该疫苗有在延长晚期黑色素瘤患者的生存期方面具有显著益处。据了解,mRNA-4157或将上市。
T细胞受体工程化T细胞疗法(TCR-T)作为一种精准、高效的癌症免疫治疗手段,在黑色素瘤中显示出治疗前景。
1月3日,BioNTech在全球知名期刊《Nature Medicine》发表了荷兰癌症研究所开展的I期试验(NCT04625205)结果,该研究评估了一种来源于外周血的个性化、新抗原特异性自体 T 细胞产品(BNT221)在局部晚期或转移性黑色素瘤患者中的疗效。

共9名患者接受BNT221,6例患者最佳总体反应为病情稳定(SD),其中4名病情稳定的患者在输注 BNT221后显示肿瘤消退,并且这4名患者中有3名在输注前的几周内均有明显的肿瘤进展。2 例患者(NAC08和NAC09)自我报告疾病相关症状有所改善,包括关节活动度改善、患肢水肿减轻和日常生活基本活动能力增强。
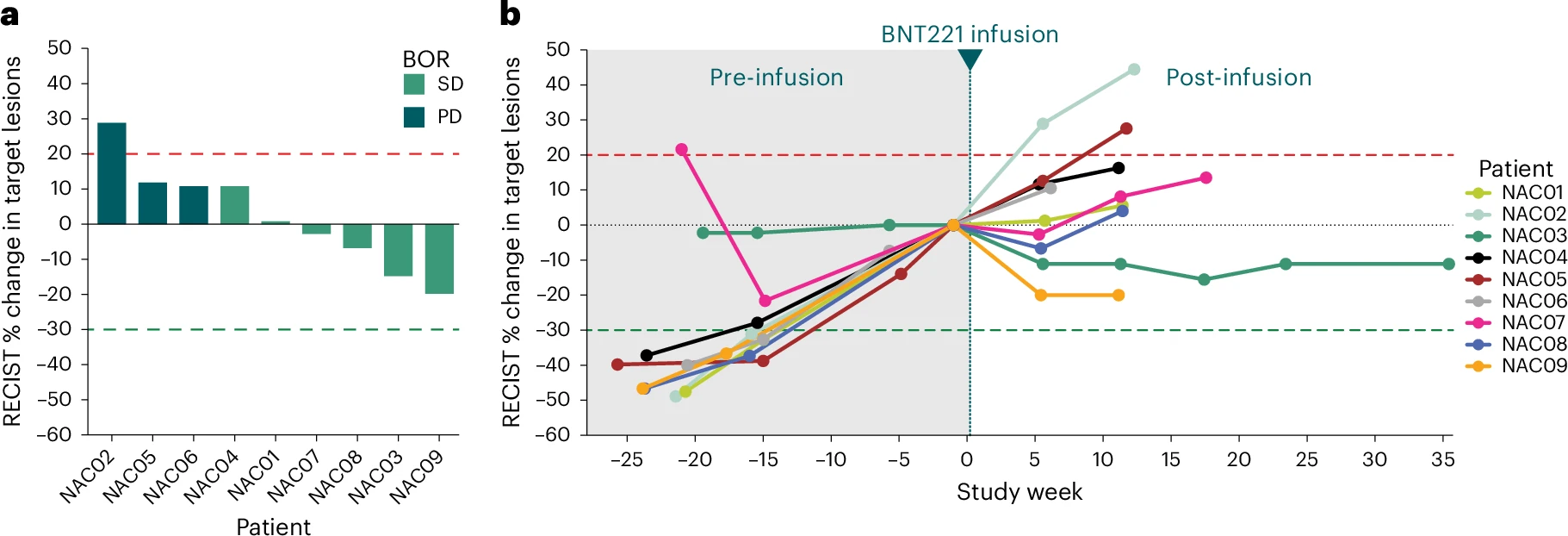
患者NAC09在输注6周后,左腋窝的靶病变减少了20%,非靶病变也显著缩小,其中包括继发性腋窝淋巴结和毫米级肺部病变。
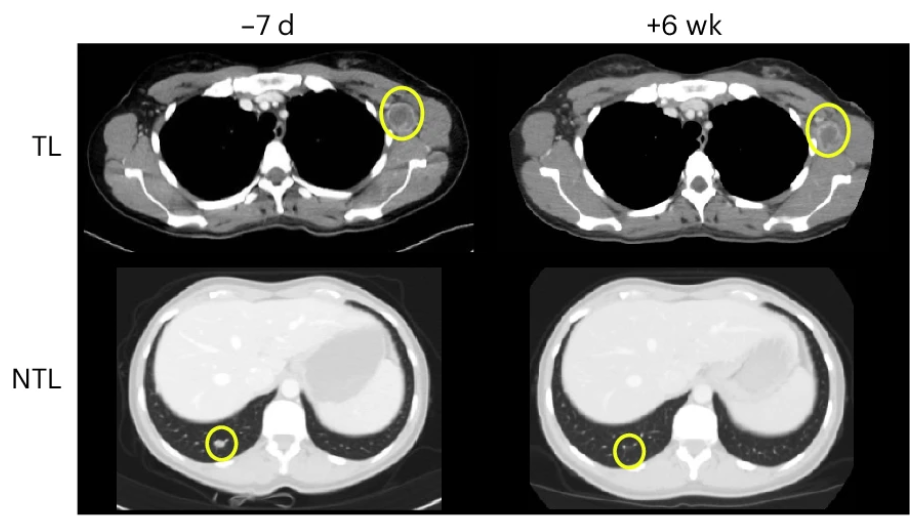
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前TCR-T细胞疗法有临床试验正在寻找黑色素瘤患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
一旦发现可疑的皮肤病变,一定要进行检查以确认黑色素瘤的诊断。靶向药物、免疫治疗等不断进步,为黑色素瘤治疗带来了希望。未来,肿瘤疫苗与化疗、细胞疗法联合免疫检查点抑制剂等联合治疗方案或得到发展,改写黑色素瘤的治疗史,为实体瘤治疗提供新思路。
参考资料
1.https://investor.innoventbio.com/media/1227/innovent_oncology_clinical_data_update_call_20240617.pdf
2.https://consultqd.clevelandclinic.org/case-study-first-patient-at-cleveland-clinic-treated-with-tumor-infiltrating-lymphocyte-therapy
3.https://s29.q4cdn.com/435878511/files/doc_events/2024/Jun/03/moderna-investor-oncology-event.pdf
4.https://www.nature.com/articles/s41591-024-03418-4
扫描下方二维码,或者直接电话咨询康和源免疫之家医学部(400-880-3716),持续为您关注并分享最新消息。

免责声明:文本参考来源于网络,版权归原作者所有。
该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!











