7月30日,国家药品监督管理局药品审评中心(CDE)将TCR-T细胞产品TAEST16001注射液纳入突破性治疗品种名单,标志着该产品作为中国第一个IND获批开展临床试验的TCR-T细胞治疗新药取得重大突破,有望成为中国第一款上市的TCR-T细胞治疗药物。
关于TAEST16001注射液
TAEST16001注射液是香雪生命科学自主研发的一款靶向NY-ESO-1的亲和力增强的TCR-T细胞免疫治疗产品,其首个临床研究适应症是HLA-A*02:01阳性且表达NY-ESO-1抗原的晚期软组织肉瘤患者。
2022年美国临床肿瘤学会(ASCO)公布TAEST16001治疗晚期软组织肉瘤患者I期临床试验的数据结果。

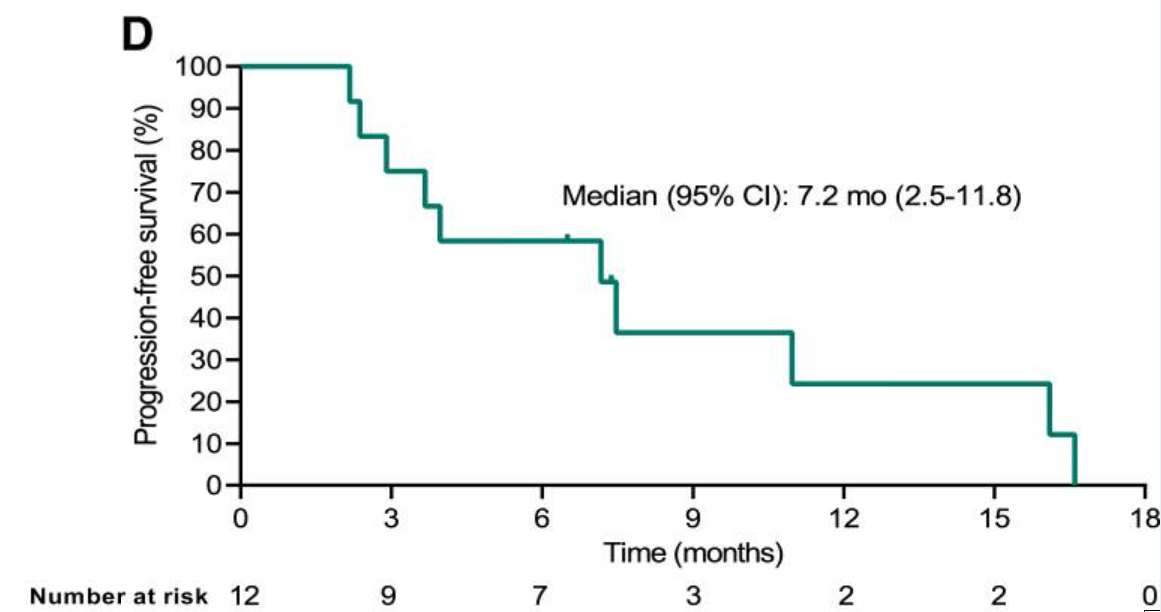
该试验共入组12例晚期软组织肉瘤患者,其中有10例滑膜肉瘤患者,2例脂肪肉瘤患者。结果显示:5例患者实现部分缓解(PR),5例患者病情稳定(SD),疾病控制率(DCR)为83.3%,中位无进展生存期(PFS)为7.2个月,中位缓解持续时间(DOR)为14.1个月。
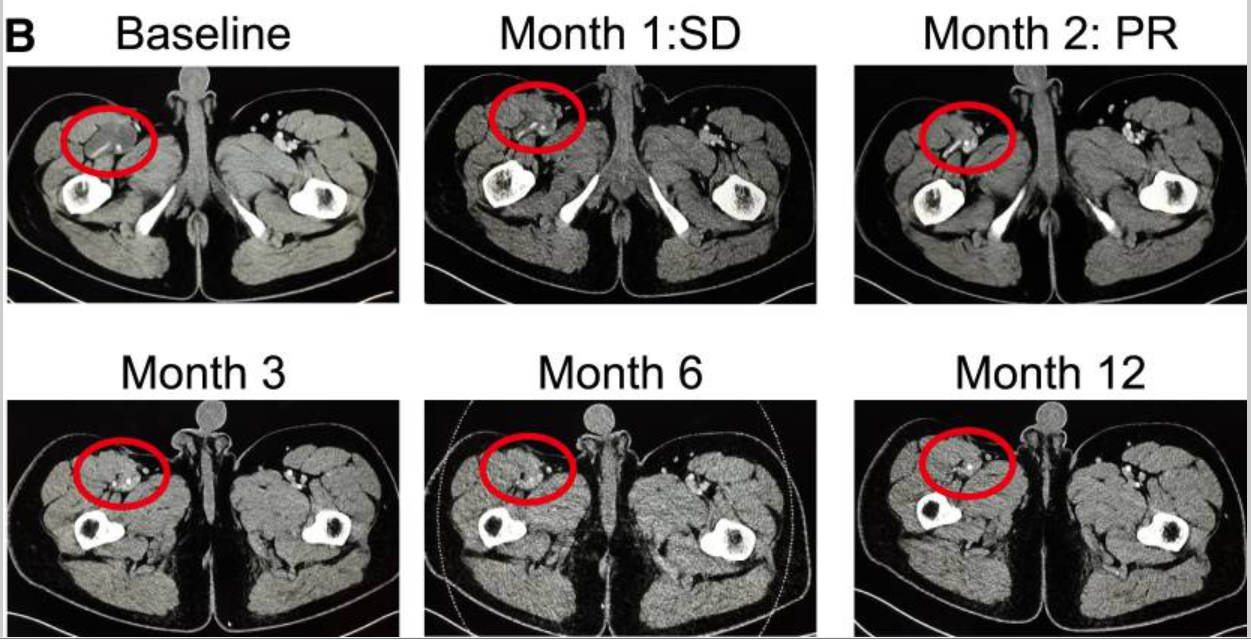
值得注意的是,该试验中1例脂肪肉瘤患者,在TCR-T细胞TAEST16001治疗后实现部分缓解,并持续缓解超1年!
2024年美国临床肿瘤学会(ASCO)公布了TCR-T细胞疗法TAEST16001在晚期软组织肉瘤(STS)中的II期临床数据(NCT05549921)。

该试验共有8例软组织肉瘤患者入选,结果显示:4例患者实现部分缓解(PR),3例患者病情稳定(SD),客观缓解率(ORR)为50%,该缓解率远超预期疗效!
值得庆幸的是,目前TCR-T细胞疗法有多款临床试验正在寻找患者,如滑膜肉瘤、肝细胞癌、黑色素瘤、卵巢癌、宫颈癌、肺癌等多款实体瘤。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
参考资料
https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(23)00261-6

相关推荐
随便看看
- 100%疾病控制率!TCR-T疗法让晚期肾癌患者肿瘤显著缩小,哪些患者能受益?
- TCR-T细胞疗法重拳出击!胰腺癌、黑色素瘤等实体瘤治疗中具有广阔的前景!
- 42.9%胰腺癌患者肿瘤缩小,94%肝癌患者病毒暴跌!TCR-T让晚期癌症患者活了两年以上
- TCR-T细胞疗法针对实体瘤患者的临床试验开始了
- TCR细胞疗法与HLA
- 肿瘤缩小65%!滑膜肉瘤、肝癌、肺癌…TCR-T疗法疾病控制率最高达100%,国内患者这些免费用药机会别错过
- 向实体瘤宣战——TILS,TCR-T更创佳绩!
- ESMO 2025重磅发布!TCR-T疗法在多种实体瘤中取得显著进展,癌症患者实现100%控制率!
- 《消失的肿瘤病灶》之TCR-T细胞迎战胰腺癌
- 再获突破!TCR-T细胞疗法进攻胃癌,MDG1015研究性新药申请获批











