12月20日,西比曼生物科技集团(以下简称“西比曼”)宣布,公司申办的“靶向GPC3装甲型嵌合抗原受体自体T细胞注射液C-CAR031(AZD7003)治疗GPC3+晚期/复发性肝细胞癌的I/II期临床研究”(STARLIGHT研究)全国研究者会已于此前11月在浙江杭州成功召开。
C-CAR031(AZD7003)是西比曼和阿斯利康联合开发的一种自体、装甲靶向GPC3的CAR-T细胞疗法,其设计“装备”了TGFβ以抵抗免疫抑制微环境,以增强其效力。
2024年美国临床肿瘤学会(ASCO)年会上,浙江大学医学院附属第一医院梁廷波教授团队口头报告了C-CAR031的首次人体IIT研究成果,该疗法在经过多线治疗的晚期HCC患者中展现出初步可控的安全性和积极的抗肿瘤活性。
疗效方面,公布数据显示,截至2024年3月14日,24名晚期HCC患者疾病控制率(DCR)高达 91.3%,客观缓解率(ORR)达56.5%。在第四组剂量中,ORR 更是高达75.0%。这意味着,既往治疗失败的难治性HCC患者,接受最大试验剂量的CAR-T治疗后,3/4的患者肿瘤缩小了30%以上。中位总生存期(mOS)为 11.14 个月。
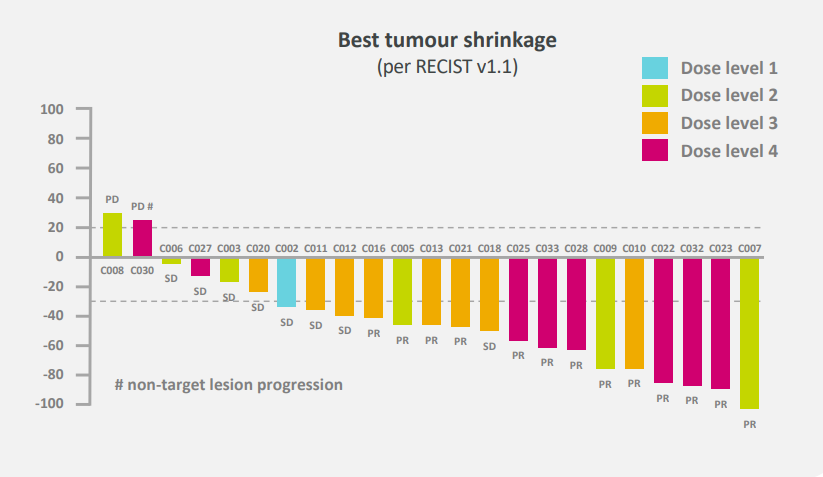
截图源于参考资料2
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前Ori-C101的临床试验仍在临床招募中,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。
项目名称:一项在既往接受过至少二线规范系统性治疗后失败或不可耐受的GPC3阳性晚期肝细胞癌(HCC)受试者中评估靶向GPC3嵌合抗原受体自体T细胞注射液(Ori-C101)的安全性、药代动力学和初步疗效的Ⅰb/Ⅱ期开放性、多中心临床研究
部分入选标准:
1.年龄18至70周岁的肝细胞癌患者;
2.预期生存期不低于 12 周;
3.美国东部肿瘤合作组织(ECOG)体能状态评分为 0 或 1;
4.有可测量病灶。
对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.oncologypipeline.com/apexonco/asco-2024-astrazenecas-gpc3-secret-sauce
2.https://www.astrazeneca.com/content/dam/az/Investor_Relations/events/ASCO-2024-IR-Presentation.pdf

相关推荐
随便看看
- CAR-T疗法令他实现完全缓解!瞄准胃癌、胰腺癌、肾癌、神经母细胞瘤
- CD19 CAR-T细胞候选产品KYV-101获再生医学高级疗法用于治疗进行性重症肌无力
- CAR-T细胞疗法让胃癌、胰腺癌、肝癌等实体瘤患者获益!疾病控制率达75.5%!
- 瑞基奥仑赛注射液用于系统性红斑狼疮的早期IIT研究积极结果被《中国狼疮肾炎诊治和管理指南(2025版)》收录
- 转机!CAR-T疗法让80%肠癌患者肿瘤缩小,最后3个名额,这些患者可报名!
- 无癌生存12年!CAR-T疗法在血液系统肿瘤、实体瘤以及自身免疫系统疾病治疗中全面开花!
- CAR-T细胞疗法治疗系统性红斑狼疮在美获批临床试验
- 多发性骨髓瘤的CAR-T细胞疗法
- 淋巴瘤患者不得不了解的两种抗癌利器——CAR-T和溶瘤病毒
- CAR-T疗法12个月生存率高达90%!退休消防员两度患癌濒临崩溃,终靠CAR-T赢得生两年无癌生存











