
CAR-T是当下研发热度非常高的癌症免疫治疗方法,但是CAR-T细胞治疗在实体瘤中缺乏特异性抗原使得很难在不伤害健康组织的情况下靶向肿瘤细胞,越来越多的患者期待新型的治疗方式。
截图源于参考资料1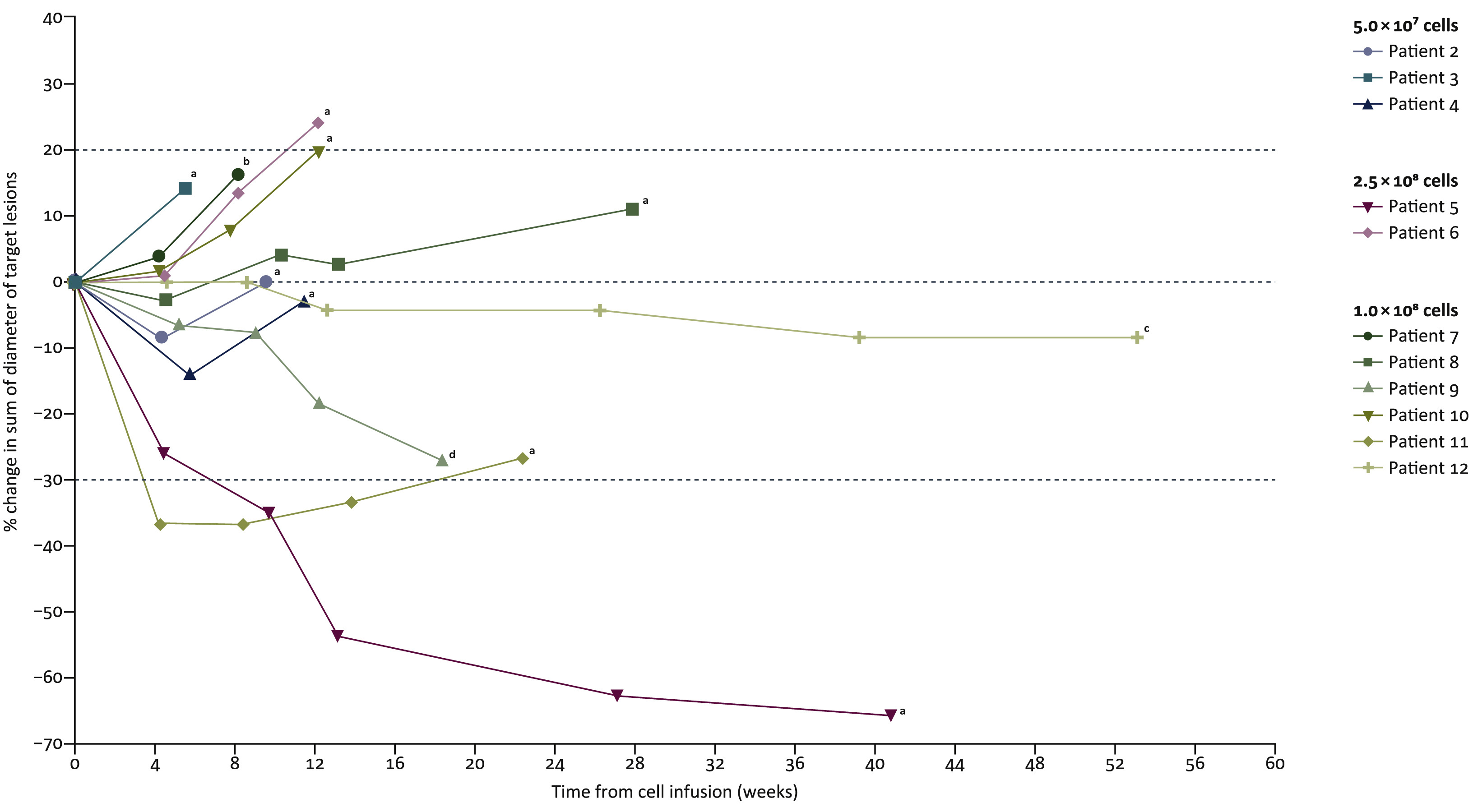

相关推荐
随便看看
- TCR-T细胞疗法强势登场!71岁胰腺癌患者的奇迹转折全靠它!
- 新选择!TCR-T细胞疗法已见显著疗效,肉瘤、黑色素瘤、宫颈癌、胰腺癌患者迎来新希望
- 晚期癌症患者的新选择:TCR-T疗法国际案例显示肿瘤缩小超50%,国内胰腺癌试验首例缓解
- TCR-T细胞疗法崭露头角,精准狙击肉瘤、黑色素瘤、结直肠癌
- 6周时间肿瘤减少了20%!TCR-T细胞疗法打击黑色素瘤、肉瘤、肝癌
- 靶向黑色素瘤相关抗原-A4 的 T 细胞受体工程化T细胞(TCR-T)疗法成功治疗子宫平滑肌肉瘤
- 肿瘤病灶完全消失!TCR-T疗法对抗实体瘤获突破!54.5%患者肿瘤显著缩小
- 攻克癌症的“神奇钥匙”!TCR-T细胞治疗让胰腺癌、肺癌、黑色素瘤、肉瘤退缩
- TCR-T细胞疗法产品LioCyx-M004获得美国FDA批准开展临床试验
- ESMO会议重磅:星汉德生物公布了TCR-T细胞疗法SCG142针对 HPV相关癌症患者的 I 期试验结果











