作者:小编
更新时间:2025-09-15
点击数:
近日,来恩生物宣布其创新mRNA编码TCR-T细胞疗法产品LioCyx-M004获得美国食品药品监督管理局(FDA)批准,开展治疗慢性乙型肝炎(CHB)的1b/2期临床试验(IND)。这是全球首个获得FDA批准用于慢性乙型肝炎治疗的TCR-T细胞疗法,同时也是首个获得FDA快速通道资格的乙肝病毒特异性TCR-T疗法。LioCyx-M004是一种自体T细胞疗法,通过mRNA编码表达靶向乙肝病毒表面抗原的TCR,赋予T细胞特异性识别并杀伤乙肝病毒感染肝细胞的能力。这种创新方法利用mRNA瞬时表达的特性,结合多次输注的方式,既能很好地控制安全性又能保证疗效。
该疗法此前已获得FDA批准用于治疗乙肝病毒相关肝细胞癌,现在又获批开展慢性乙型肝炎治疗的临床试验,证明了该平台技术的广泛应用前景。
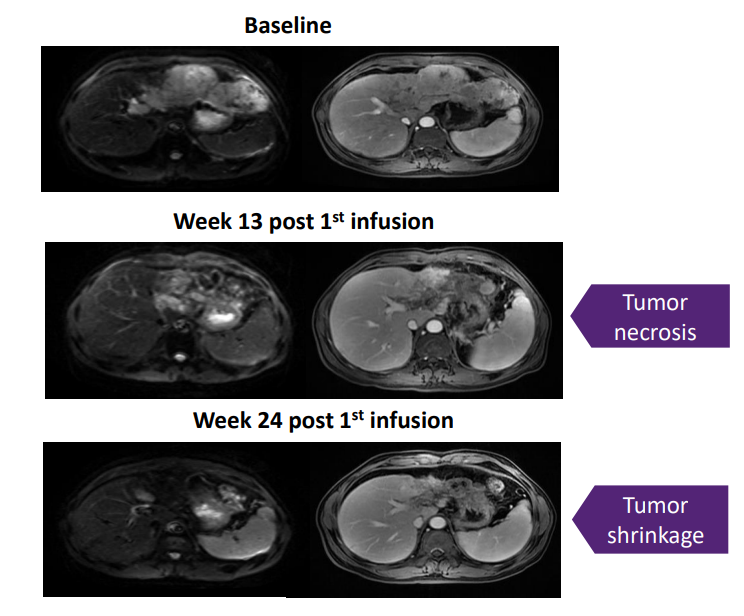
在早期的1期临床研究中,LioCyx-M004已展现了良好的安全性,使晚期肝癌患者生存期得到显著提升,实现了33.1个月的中位总生存期,并观察到乙肝表面抗原(HBsAg)的下降,显示出抗肿瘤和抗病毒治疗效果。
目前,TCR-T疗法正在多种实体瘤中开展临床试验。NW-101是一种靶向肿瘤相关抗原(TAA)的TCR-T免疫细胞治疗药物。目前正在招募卵巢癌、肺鳞癌、三阴性乳腺癌、滑膜肉瘤、黑色素瘤、食管癌患者。这为更多类型的癌症患者提供了新的治疗选择。
如果您或家人正在寻找适合的治疗方式,可考虑咨询相关临床试验,有意向的患者可致电400-880-3716提交病例资料、治疗经历等进行初步筛选。

相关推荐
随便看看
- 重磅!全球首款TCR-T细胞疗法获批上市!肿瘤缩小81%!
- 国内首款!TCR-T细胞产品TAEST16001注射液纳入突破性治疗品种名单
- 肿瘤缩小了!TCR-T疗法让T细胞精准杀癌,临床试验见肿瘤缩小成效,为晚期患者打开新希望之门
- 无瘤生存超9年!TCR-T细胞疗法效果更上一层楼!
- 74%肿瘤缩小!TCR-T疗法攻克实体瘤,卵巢癌、儿童肾母细胞瘤数据亮眼,脑、肺、肝多发转移消退
- 靶向黑色素瘤相关抗原-A4 的 T 细胞受体工程化T细胞(TCR-T)疗法成功治疗子宫平滑肌肉瘤
- 1个月病情稳定,2个月部分缓解!TCR-T疗法“暴击”肉瘤、肺癌、胰腺癌
- TCR-T细胞治疗产品“XLS-103注射液”新药临床试验申请获批
- SCG101 TCR-T疗法公布抗病毒和抗肿瘤“双杀”效果:94%肝癌患者病毒暴跌,近一半肿瘤缩小!
- 星汉德生物SCG101一期临床亮相AASLD











