近日,来恩生物宣布其mRNA编码TCR-T细胞产品Liocyx-M004获得美国食品药品监督管理局(FDA)批准,启动国际多中心2期临床试验。
Liocyx-M004是全球首个针对乙肝病毒(HBV)相关肝细胞癌的mRNA编码TCR-T细胞疗法。I期试验(NCT03899415)对8名晚期乙肝病毒(HBV)相关肝细胞癌患者进行研究,结果显示中位总生存期(OS)为33.1个月,将近3年!患者1实现了持续 27.7 个月的部分缓解,肝脏肿瘤大小显著缩小。
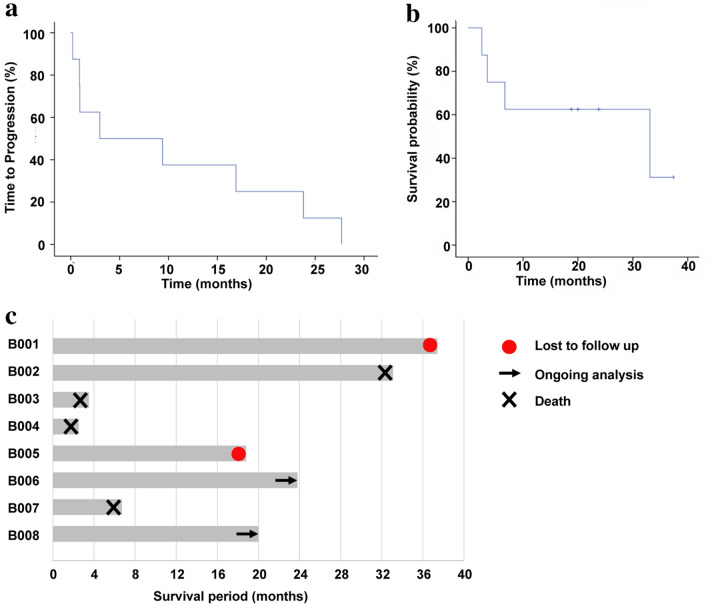
典型病例如下图:
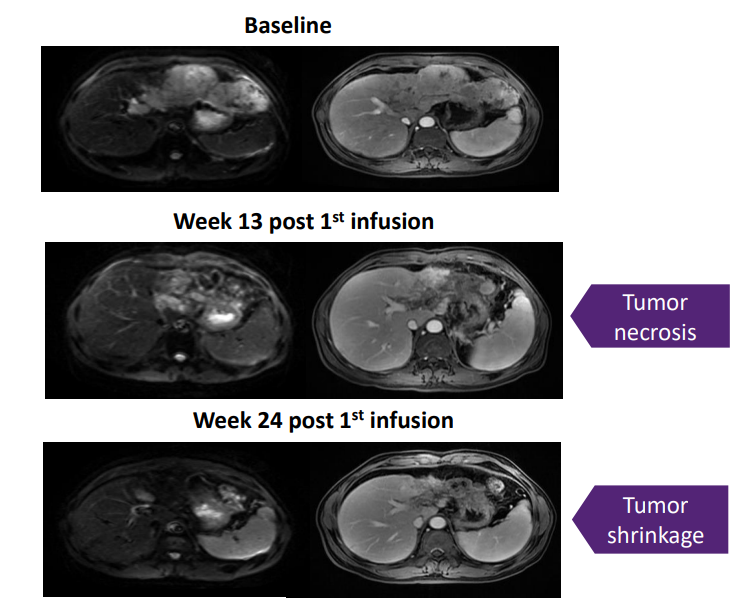
TCR-T细胞疗法通过将能够识别特定癌症抗原的TCR基因导入患者的T细胞中,使这些T细胞发挥特异性识别和杀伤肿瘤细胞的作用,以此来达到抗癌的目的。据统计,世界上约90%的癌症都是实体肿瘤,由于缺乏胞内特异性抗原靶标,目前CAR-T在实体瘤领域临床治疗效果也十分有限。与近年来热门的CAR-T细胞疗法相比,TCR-T具有更高的靶点特异性及更高的安全性,更适合于实体瘤的治疗。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前TCR-T细胞疗法有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
部分入选标准:
1.年龄≥18岁,男女均可;
2.HPV相关恶性肿瘤患者,已经失去手术或其他根治性治疗的机会,且肿瘤组织学或细胞学检测HPV 16+;
3.至少有一个符合可测量靶病灶;
4.HLA分型检测结果为HLA-A*02:01;
5.东部肿瘤协作组(ECOG)体力状况评分0-1;6.预计生存期>3个月。
参考资料
1.https://pmc.ncbi.nlm.nih.gov/articles/PMC8651587/
2.https://uploads-ssl.webflow.com/601374d8bb5a8e0e97896107/6020f331af6eba78c6c07f3e_2020%2C%20%5Bposter%5D%20Use%20of%20LioCyx-M.pdf

相关推荐
随便看看
- 74岁晚期胰腺癌患者肿瘤缩小!国内团队用TCR-T疗法成功挑战“癌王”胰腺癌,肿瘤标志物直降90%
- 中国力量:TCR-T疗法在胰腺癌、肝癌、肉瘤中频传突破,肿瘤缩小90%,肿瘤标志物骤降
- 国内针对TCR-T细胞疗法的研发在胰腺癌领域取得突破
- 走投无路?试试TCR-T!专杀实体瘤的“超级战士”来了!针对晚期食管癌、肺癌、乳腺癌等多癌种
- 2年无进展生存!NY-ESO-1 TCR-T细胞疗法点亮软组织肉瘤患者的希望
- 1年生存率高达90%!这两款TCR-T细胞疗法上市有望!肉瘤患者曙光
- 生存超2年!!抗癌“新星”TCR-T细胞疗法在肉瘤、结直肠癌患者中显威
- 520万人民币的TCR-T疗法,在结直肠癌、肾癌、胰腺癌、尿路上皮癌以及肝癌中发挥显著疗效
- TCR-T疗法步步紧逼,专攻实体瘤软肋!柳叶刀发布Afami-cel新数据,首款TCR-T疗法上市在即
- 重磅!TCR-T疗法让晚期癌症患者肿瘤完全消退!卵巢癌/肺癌等患者速抢名额











