尽管嵌合抗原受体(CAR) T细胞已成为复发/难治性b细胞恶性肿瘤患者的重要治疗选择,但超过60%的弥漫性大b细胞淋巴瘤(DLBCL)患者接受CAR-T细胞疗法治疗后未能获得持久的反应。为了揭示CAR-T细胞治疗的变化并识别反应生物标志物,研究人员对58例接受CD19/CD20 CAR-T细胞治疗的r/rDLBCL患者进行了制造前T细胞和CAR-T细胞产物及其与预后的关联进行了回顾性分析。研究人员对来自DLBCL患者的CAR-T细胞产品和预制造T细胞进行了大量RNA-Seq、单细胞RNA-Seq和配对T细胞受体测序。研究人员注意到,具有更高比例和增强的CAR-T细胞产品激活能力的CD8干细胞样记忆T细胞群是实现持久临床反应的关键。通过分析自体衍生的预制造T细胞,数据表明,预制造T细胞的细胞和分子特征的异质性导致了CAR-T细胞治疗DLBCL后疗效的差异。CAR-T细胞在不同临床结果的患者中抗肿瘤疗效的差异似乎是由于CCR7基因表达的缺失,加上来自分子反应较差的患者的单采T细胞中CD8 naïve-T细胞群中活化和抑制相关基因的表达增加。这些发现显著地促进了对制造前T细胞功能的潜在分子决定因素的理解。
DLBCL是一种常见的侵袭性血液恶性肿瘤,约60%的患者在最初的蒽环类药物和含利妥昔单抗的治疗方案后达到完全缓解(CR)。然而,在复发/难治性DLBCL (r/rDLBCL)患者中,达到1年生存率的患者比例不到30%。4,5尽管自体抗cd19 CAR-T细胞疗法在治疗大b细胞淋巴瘤方面非常有效,但只有不到一半的r/rDLBCL患者达到1年以上的缓解。6,7在一项回顾性研究中,809例患者接受市售抗cd19 CAR-T细胞治疗,最佳总缓解率/完全缓解率(ORR/CRR)为66-80%/42-66%,CAR-T细胞输注后的中位总生存期(OS)为19.0个月,中位无进展生存期(PFS)仅为5.6个月8确定导致治疗耐药的因素以及如何通过设计创新的CAR-T细胞来克服这些因素一直是近年来该领域研究的主要焦点。
CD19抗原表达的缺失或突变是b细胞恶性肿瘤中CAR-T细胞抵抗和复发的共同机制。9,10同时靶向两种抗原的CAR-T细胞设计已被证明可以降低由于靶向单一抗原的CAR-T细胞输注后抗原丢失而导致的疾病复发率。11,12,13之前,研究人员筛选了CD19和CD20串联CAR-T细胞(TanCAR7 T细胞),并提供了它们治疗复发/难治性非霍奇金淋巴瘤(r/rNHL)疗效的证据在研究人员的一项研究中,87名接受TanCAR7 T细胞治疗的r/rNHL患者的中位PFS为23.5个月相比之下,在DLBCL中,串联CAR-T细胞的持久性和有效性似乎超过了抗cd19 CAR-T细胞。然而,仍有超过四分之一的患者未达到临床客观缓解,约30%达到临床缓解的患者在一年内出现疾病复发。抗原丢失可以解释一些复发,但并非所有复发患者都是抗原阴性疾病,这表明可能有其他因素导致耐药性。
一些临床数据表明,CAR-T细胞在体内可检测的扩增水平和存在时间与治疗效果和完全缓解率呈正相关,并且细胞输注后快速完全缓解的患者复发率低。16,17强健的CAR-T细胞体内植入和扩增是诱导抗肿瘤疗效的先决条件。16,18,19,20来自一些研究的证据表明,注入CAR-T细胞缺乏具有中枢记忆表型的细胞比例,并且在体内维持肿瘤细胞长期靶向的能力较差。19,21,22此外,接受无记忆细胞群的CAR-T细胞输注的患者往往有更高的复发率每个CAR-T细胞产品都是不同的,因为它是由患者的特异性T细胞制成的,而受损的分离T细胞会导致CAR-T细胞产品的记忆和激活功能降低,并且容易在体内过早衰竭。23,24,25,26,27因此,影响CAR-T细胞治疗效果的一个重要因素是分离- t细胞与CAR-T细胞的差异。然而,这种相关性尚未在接受CAR-T细胞治疗的DLBCL患者中进行研究。需要进一步确定与CAR-T细胞治疗后DLBCL进展风险增加相关的因素,以实现早期和潜在的更有效的治疗干预。
在这里,研究人员对58名接受CAR-T细胞治疗的DLBCL患者进行了随访研究,研究人员分析了56名可评估患者的CAR-T细胞在体外对CD19/ cd20阳性肿瘤细胞系的杀伤,在排除肿瘤相关因素后,研究人员发现CAR-T细胞在耐药患者中的抗肿瘤功能与CAR-T细胞在持久反应(DR)患者中的功能相比。随后,研究人员对56例可评估患者进行了T细胞亚型组成分析,对6例DR和6例耐药患者进行了大量RNA-seq分析,对6例DR和3例耐药患者进行了单细胞RNA-seq分析,并进一步分析了CAR-T细胞产物和分离细胞的组成、功能和基因表达与临床疗效的相关性,以确定与持续临床反应相关的特征。这些数据为CAR-T细胞治疗在DLBCL患者中疗效变异性的细胞和分子基础提供了新的见解。
结果:反应患者的CAR-T细胞比耐药患者具有更好的抗肿瘤能力和活化能力
在2017年7月至2020年1月期间,58名DLBCL患者被分配接受TanCAR7 t细胞治疗。如先前报道,在总共58例DLBCL患者中,最佳CRR为71%截至2022年5月10日研究截止时,58%的患者仍处于缓解期,49% (95% CI, 34-64)的患者在输注后24个月未出现疾病进展。未达到中位OS和持续时间反应,24个月时估计生存概率为67% (95% CI, 53-77)。在本研究中,缓解患者包括CAR-T细胞输注后达到CR或部分缓解(PR)的患者,根据这些患者在细胞治疗后1年内是否出现疾病复发来定义DR或复发。CAR-T细胞治疗后出现进行性疾病(PD)的耐药患者。共有45名患者获得缓解;这45例患者中有32例被定义为DR;另有13例定义为复发;11例患者对CAR-T细胞治疗出现耐药性。研究人员首先分析了肿瘤异质性因素与CAR-T细胞治疗疗效之间的关系。与一些报道的使用抗cd19 CAR-T细胞治疗的NHL患者的数据一致,7,20对串联CAR-T细胞治疗的最佳反应与患者先前治疗的特征(治疗线数、治疗耐药或复发)、肿瘤Ki67表达和基因突变无关。
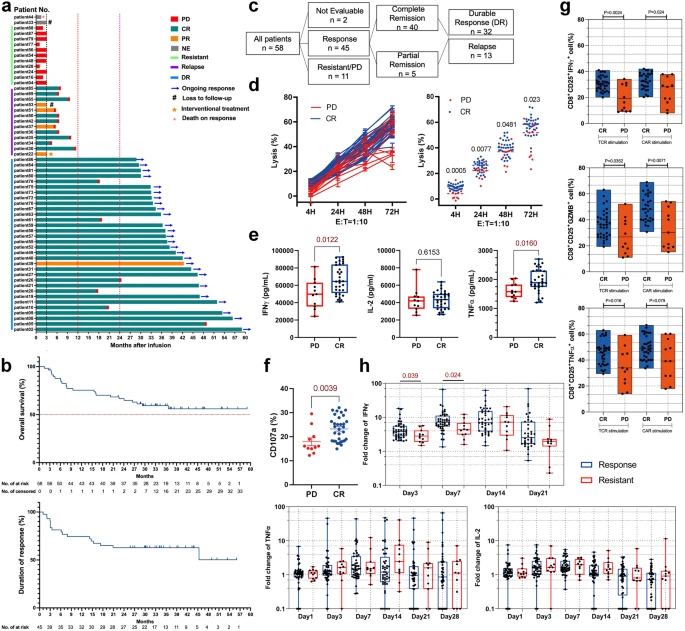
为了评估临床疗效是否由于CAR-T细胞产品的内在因素,研究人员使用临床制造的CAR-T细胞随着时间的推移杀死人类白血病细胞系,在排除个体患者差异和肿瘤异质性的影响后,评估患者CAR-T细胞的抗肿瘤疗效。在72小时内,从CR患者获得的CAR-T细胞比从PD(耐药)患者获得的CAR-T细胞更有效地杀死nam16肿瘤细胞。从CR患者获得的CAR-T细胞分泌的TNFα和IFNγ水平明显高于PD患者。对CAR-T细胞上CD107a表达的分析证实了这一发现。与Nalm6细胞共培养1小时后,CR患者获得的CAR-T细胞的CD107a表达高于耐药患者获得的细胞。接下来,研究人员研究了CAR-T细胞对活化反应的TCR或car特异性功能特性。在细胞内流式细胞术分析之前,将注入的CAR-T细胞刺激4小时,诱导下游TCR信号(iononomycin)或Nalm6细胞。刺激后,CR患者的CD8CD25 CAR-T细胞群表达的颗粒酶B (GZMB)、IFNγ和TNFα水平高于耐药患者。在对56例可评估患者细胞输注后的细胞因子水平的回顾性分析中,在细胞输注后6周内的大多数时间点,有抵抗的患者的血清IFNγ水平明显高于有反应的患者。这些数据表明,与细胞治疗前来自耐药患者的CAR-T细胞相比,来自应答患者的CAR-T细胞具有更好的抗肿瘤和活化能力。
CD8TSCM CAR-T细胞在CAR-T细胞治疗应答中发挥重要作用
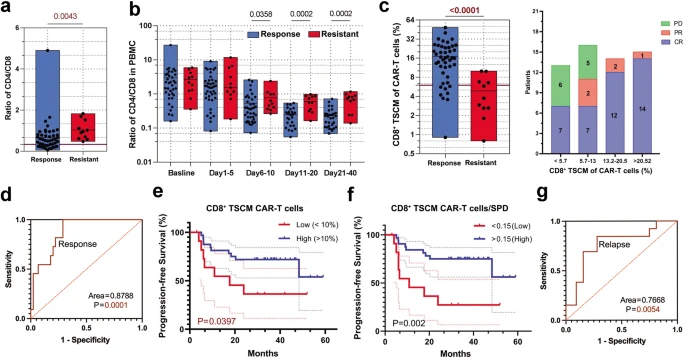
接下来,研究人员试图确定与临床反应相关的CAR-T细胞产物的关键表型特征。注射CAR- t细胞总数和CAR感染率与最佳反应或持久反应无关。一些研究报道,在CAR-T细胞产物中,较高比例的终端T细胞表达一种衰竭相关表型,导致抗cd19 CAR-T细胞的扩增和记忆能力下降。27,28,29在这项研究中,研究人员观察到来自耐药患者的CAR-T细胞比来自应答患者的CAR-T细胞含有稍高的PD-1TIM3细胞群,但DR和复发患者之间没有差异(Supplementary Fig. S2b)。在CAR-T产品中,中枢记忆T细胞(TCM, CD45RA++−CD62L)和效应T细胞(TEF, CD62L+−)的比例在应答和耐药患者之间或DR和复发患者之间没有显著差异。应答患者的CAR-T细胞产物CD4/CD8比值明显低于耐药患者。
相应的,应答患者体内CAR-T细胞扩增以CD8 T细胞为主。细胞输注后第5天开始扩增,持续3-4周。在一些CD19-CAR-T细胞治疗的研究中,表现出最佳临床结果的患者在其CAR-T细胞产品中记忆T细胞的频率也有所增加。在研究人员的研究中,在所有56例可评估的DLBCL患者的CAR-T细胞产物中,CD8 TSCM(干细胞样记忆T细胞,+19,30,31 CD45RACD62L)在应答患者中的比例显著高于耐药患者(p < 0.0001),高四分位数患者的应答率为100%。CD8 TSCM人群根据ROC曲线下面积下的面积成功区分客观应答和耐药患者。然后,研究人员使用Kaplan-Meier分析对45名获得客观缓解的患者进行PFS评估,这些患者根据CAR-T细胞产品中CD8 TSCM人群的高低水平分为两组。CD8水平较高的TSCM患者的PFS略好。在肿瘤负荷较大的患者中,CD8 TSCM含量高的患者PFS较长。值得注意的是,CAR-T细胞产品中CD8 TSCM的数量在持续缓解和复发之间有显著区别。这些数据表明,CAR-T细胞产品中的cd8阳性TSCM群体与接受CAR-T细胞治疗的r/rDLBCL患者的客观和持久反应最显著相关,特别是在肿瘤负担重的患者中。在输注的CAR-T细胞中缺乏CD8 TSCM细胞可能是与原发性治疗耐药相关的一个主要因素。
为了确定CAR-T细胞治疗的持久缓解是否是CD8 CAR-T细胞数量优势的结果,研究人员对DR和耐药患者的CD8 CAR-T细胞产物进行了大量RNA-seq分析。测序样本来自6例耐药患者,这些患者在之前的疗效实验中杀伤效果明显降低,以及6例CR超过24个月且疾病特征与6例耐药患者相似的DR患者。在应答和耐药患者的CD8 CAR-T细胞产物中存在基因表达差异。与上述表型结果相似,大多数记忆相关基因,如CD27、TCF7、CCR7、LEF1、BACH2、SELL和CAPG在应答患者的CD8 CAR-T细胞中的表达明显高于耐药患者;此外,激活和衰竭相关基因,如GZMK、TBX21、EOMES、TOX、TIGIT和SP140的表达显著下调。基因本体(Gene Ontology, GO)分析显示,T细胞相关通路的激活,包括活化、粘附、增殖和共刺激通路,在应答患者和耐药患者之间存在差异。基因集富集分析(GSEA)结果显示,DR患者获得的CD8 CAR-T细胞中激活相关基因和细胞增殖相关基因的表达较低,而记忆相关基因和复合物相关基因的表达高于耐药患者。与耐药患者的CD8 CAR-T细胞相比,DR患者的CD8 CAR-T细胞处于相对静止状态。

文章转载自《自然杂志》
目前免疫管家已开通微信公众号,健康界,知乎,今日头条等多自媒体网站并且同名[免疫管家]
扫描下方二维码,或者直接电话咨询免疫管家医学部(400-880-3716),为癌友患者们分享更多信息。

免责声明:免疫管家为免疫科普平台,文本参考来源于网络,版权归原作者所有。该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!











