9月18日,Imugene宣布美国食品和药物管理局(FDA)授予新型溶瘤病毒疗法CF33-hNIS(VAXINIA)孤儿药资格认定(ODD),旨在治疗胆管癌(一种罕见的侵袭性胆管癌)。

2024年美国临床肿瘤学会(ASCO)胃肠道癌症研讨会上报告了CF33-hNIS单药治疗或联合 pembrolizumab治疗7例晚期或转移性实体瘤患者的疗效。其中有3例结直肠癌患者,2例胆管癌患者,胰腺癌和肝细胞癌患者各1例,结果显示:疾病控制率(DCR)为86%。

截图来源于参考资料2,侵权请联系删除
值得注意的是,其中1例胆管癌患者表现假性进展,第四个周期达到完全缓解 (CR),1年未复发。
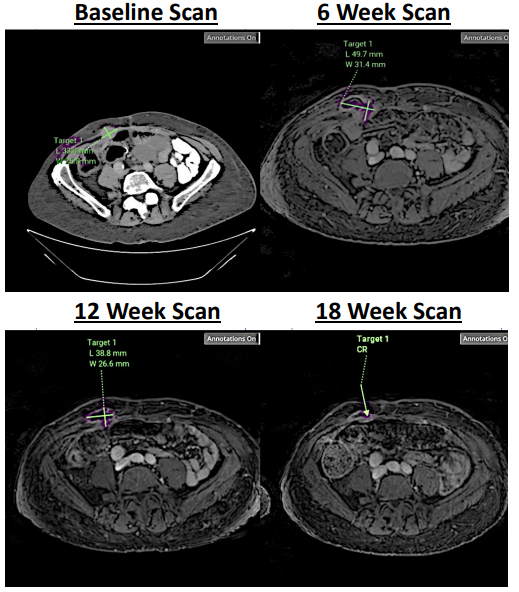
截图来源于参考资料2,侵权请联系删除
溶瘤病毒(OVs)是一类新兴的癌症治疗药物,具有优先靶向和消除癌细胞的独特能力以及与其他癌症治疗药物在很大程度上不重叠的可耐受安全性。
目前溶瘤病毒针对实体瘤的临床试验正在全国范围内寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
项目名称:重组人IL-21溶瘤痘病毒注射液(hV01)治疗晚期恶性实体瘤的I期临床研究
部分入选标准:
1.年龄18-75周岁;
2.晚期恶性实体瘤患者;
3.预计生存期≥3个月;
4.体力状态评分(ECOG)0-1分。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.targetedonc.com/view/fda-grants-orphan-drug-designation-to-cf33-hnis-in-cholangiocarcinoma
2.https://static1.squarespace.com/static/5b63d41b3e2d09b1f56bf483/t/65a9aff332d3180e08db85c7/1705619461250/749+ASCO-GI+MAST-Final+%281%29.pdf
3.https://ascopubs.org/doi/10.1200/JCO.2024.42.3_suppl.749

相关推荐
随便看看
- 美国FDA快速通道认证!溶瘤病毒疗法AdAPT-001为晚期癌症患者带来希望
- 病毒抗癌疗法?溶瘤病毒疗法使患者肿瘤持续缩小超30个月
- 延长499天生存期!溶瘤病毒 OH2在黑色素瘤、结直肠癌、食管癌治疗中大放异彩
- 74.5%完全缓解率!病毒学家用自制溶瘤病毒治愈自身癌症,晚期癌症患者迎来"以毒攻癌"新曙光
- 疾病控制率71.4%!溶瘤病毒“特种部队”已杀入战场,免疫治疗无效的晚期肠癌患者,终于迎来新希望!
- 完全缓解率为82.9%!溶瘤病毒联合帕博利珠单抗治疗膀胱癌
- 溶瘤痘苗病毒Olvi-Vec治疗广泛小细胞肺癌患者的1b期/2期临床试验取得积极数据
- 生存期延长至22.3个月!FDA快速通道认证!溶瘤病毒联合疗法为结直肠癌、肉瘤患者带来希望
- 利用自己在实验室中培养的溶瘤病毒成功治疗自己的乳腺癌
- 溶瘤病毒Ad-TD-nsIL12为弥漫性脑桥脑胶质瘤(DIPG)患儿带来新希望











