12月2日,Elicio Therapeutics宣布在2024 年 ESMO 免疫肿瘤学大会上公布了 ELI-002 的 1 期 AMPLIFY-201 临床试验 (NCT04853017) 的最新结果。

AMPLIFY-201 是一项多中心、开放标签、剂量范围的 1 期研究,旨在评估 ELI-002的安全性和耐受性。该试验共招募了 25 名患者,包括 20 名胰腺导管腺癌 (PDAC) 患者和 5 名结直肠癌 (CRC) 患者。结果显示:所有患者中位无进展生存期(PFS)为16.3 个月,中位总生存期(OS)为28.9 个月。
胰腺导管腺癌队列中位无进展生存期为15.3个月,结直肠癌队列为16.3个月。
安全性方面,ELI-002 2P耐受性良好,未观察到3级/4级治疗相关不良事件、剂量限制性毒性(DLT)或细胞因子释放综合征。
ELI-002是一种结构新颖的研究性AMP癌症疫苗,其靶向由KRAS基因突变驱动的癌症,KRAS基因是许多人类癌症的普遍驱动因素。2024年1月,《Nature》发表了癌症疫苗ELI-002用于治疗KRAS突变的胰腺癌和结直肠癌患者的1期AMPLIFY-201试验(NCT04853017)早期结果。该试验纳入的25例患者中,有21例患者观察到肿瘤生物标志物反应,3例胰腺癌和3例结直肠癌患者肿瘤标志物清除,无复发生存期(RFS)为 16.33个月,中位总生存期(OS)为16.33个月。
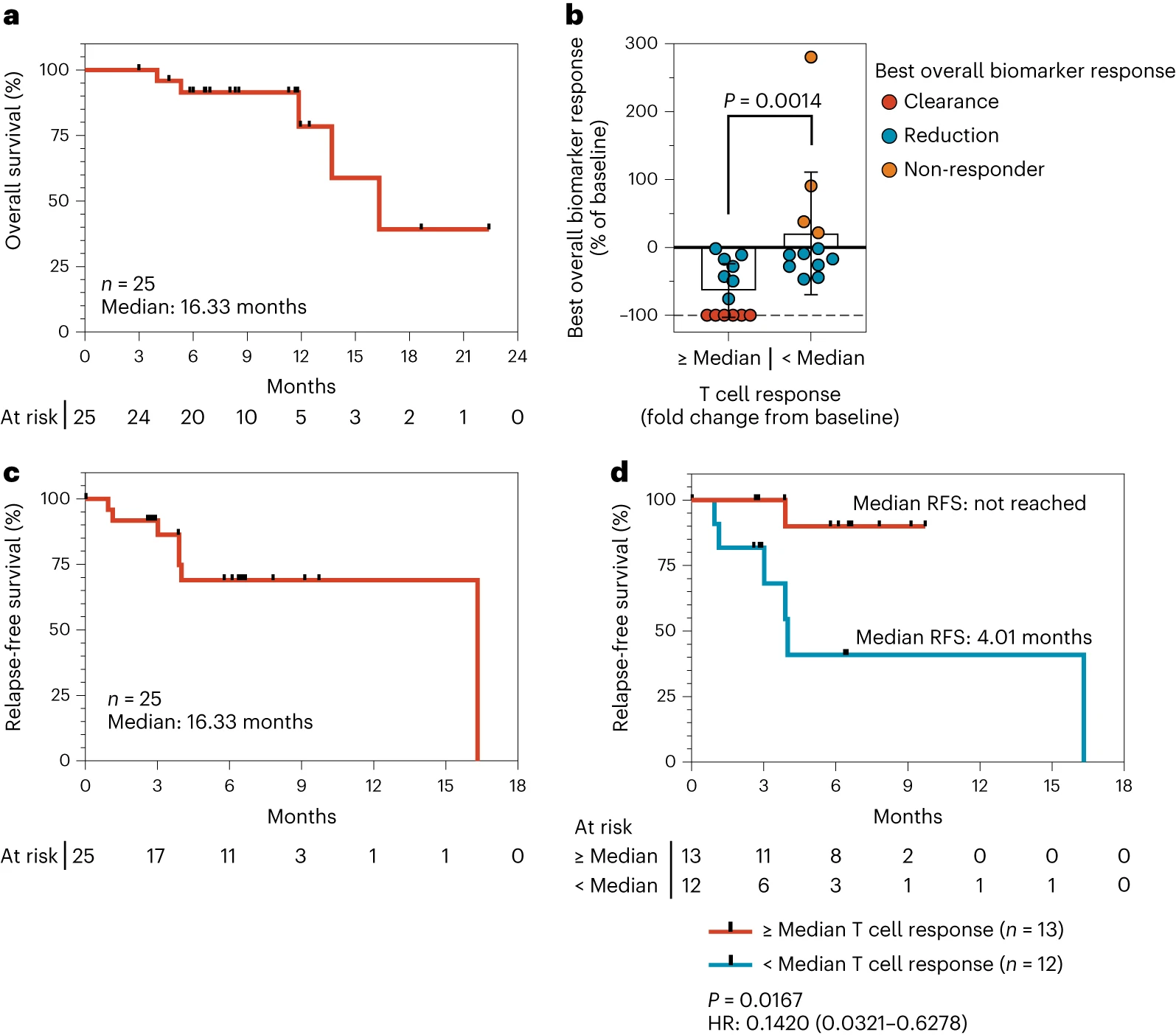
该试验中,ELI-002癌症疫苗是在KRAS突变肿瘤患者中诱导了强烈的T细胞反应,安全性良好。
值得庆幸的是,目前癌症疫苗临床试验正在全国范围内寻找患者,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://elicio.com/press_releases/elicio-therapeutics-presents-updated-results-from-eli-002-phase-1-amplify-201-study-at-esmo-immuno-oncology-congress-2024/
2.https://www.nature.com/articles/s41591-023-02760-3

相关推荐
随便看看
- 个性化mRNA疫苗联合PD-1抑制剂治疗晚期食管鳞状细胞癌患者的病例
- mRNA疫苗|mRNA呼吸道合胞病毒疫苗mRESVIA获批上市!肿瘤赛道毫不示弱!
- mRNA肿瘤治疗性疫苗的新药临床申请获受理
- 36个月生存率达84.4%!癌症疫苗在宫颈癌、头颈癌、胃癌、胰腺癌、黑色素瘤领域“杀疯了”
- 免疫治疗战队“新人小生”——肿瘤疫苗,到底有什么魅力?
- 5年随访多名患者存活!癌症疫苗大放异彩,从“遥远梦想”到临床可能,开启癌症精准打击新篇章
- 肿瘤疫苗给肿瘤治疗增加一线希望的光
- 肿瘤也有疫苗?注射mRNA疫苗18个月后都没有复发迹象!攻克癌症有戏
- OSE2101(Tedopi)用于晚期或转移性胰腺导管腺癌(PDAC)的2期TEDOPaM试验达到主要终点
- 5年生存率100%!科学家正为您“量身定制”抗癌方案,癌症疫苗交出满意答卷!术后3年74%未复发











