2 月 24 日,PDS Biotech宣布在美国癌症研究协会的期刊《临床癌症研究》上发表其主要免疫疗法候选药物 Versamune® HPV 的循环肿瘤 DNA (ctDNA) 结果。

共有 66 名局部晚期宫颈癌患者入组,其中 49 名接受标准护理治疗,17 名参加CRT 和 Versamune HPV 联合治疗,(PDS0101;IMMUNOCERV)。中位随访时间为 23 个月,2 年无复发生存期 (RFS) 为 78.4%。基线淋巴结疾病范围与 HPV cfDNA 水平相关。HPV cfDNA 水平在放疗第 1 周达到峰值,并通过治疗降低。与接受标准护理治疗的患者相比,接受 PDS0101 疫苗的患者检测不到 HPV 16 型 cfDNA 的比率更高。HPV cfDNA 清除率与更好的 2 年 RFS 相关 (92.9% vs. 30%,对数秩;P = 0.0067)。RFS 的最强预测因子是随访中 HPV cfDNA 清除率达到 0.83 的一致性指数评分,与 MRI 反应联合时有所改善。
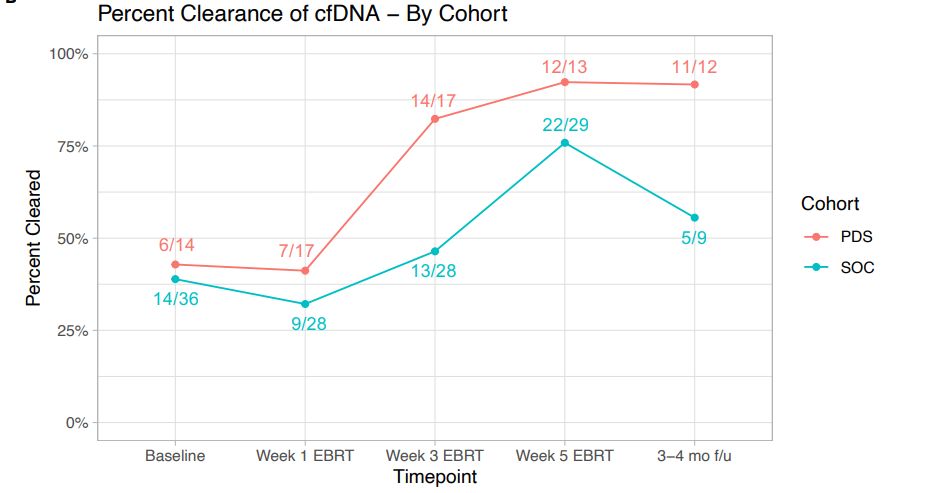
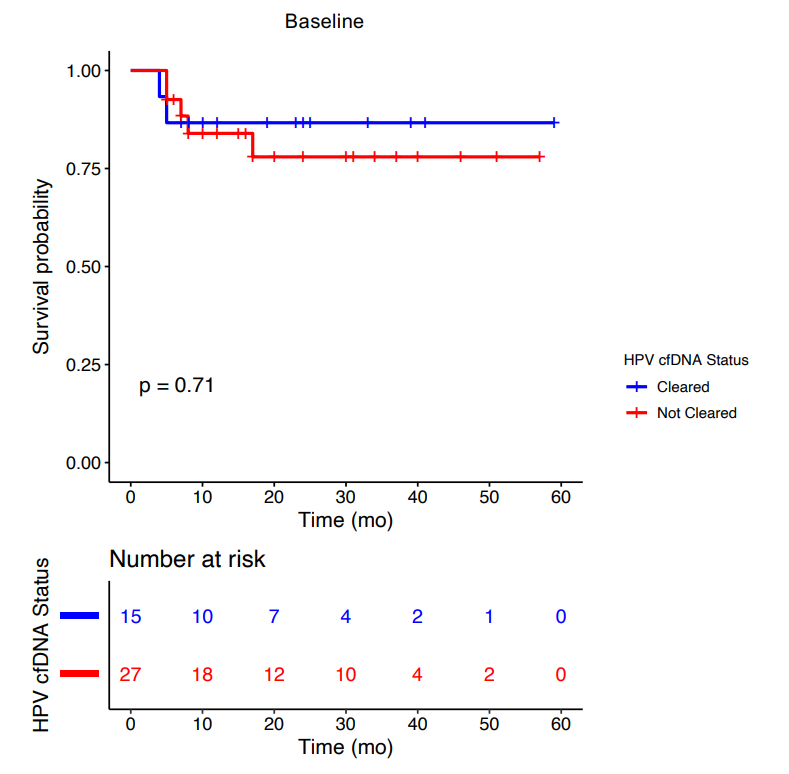
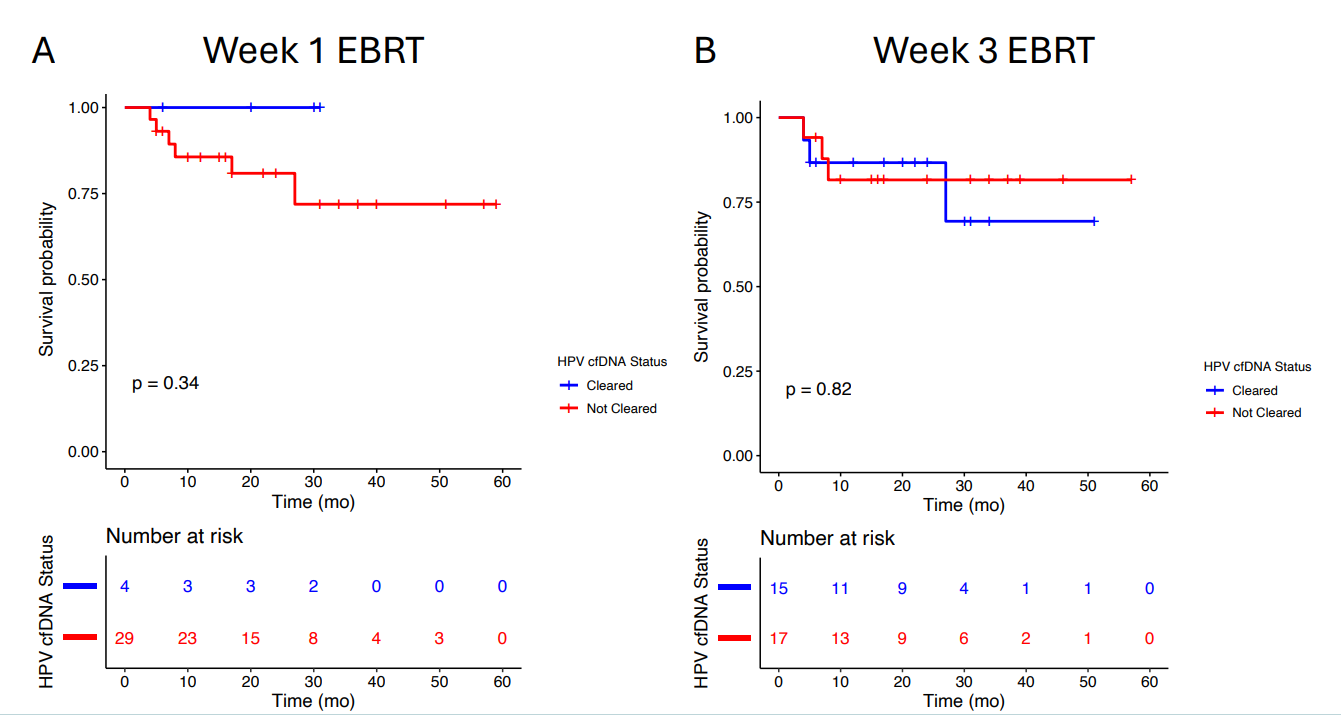
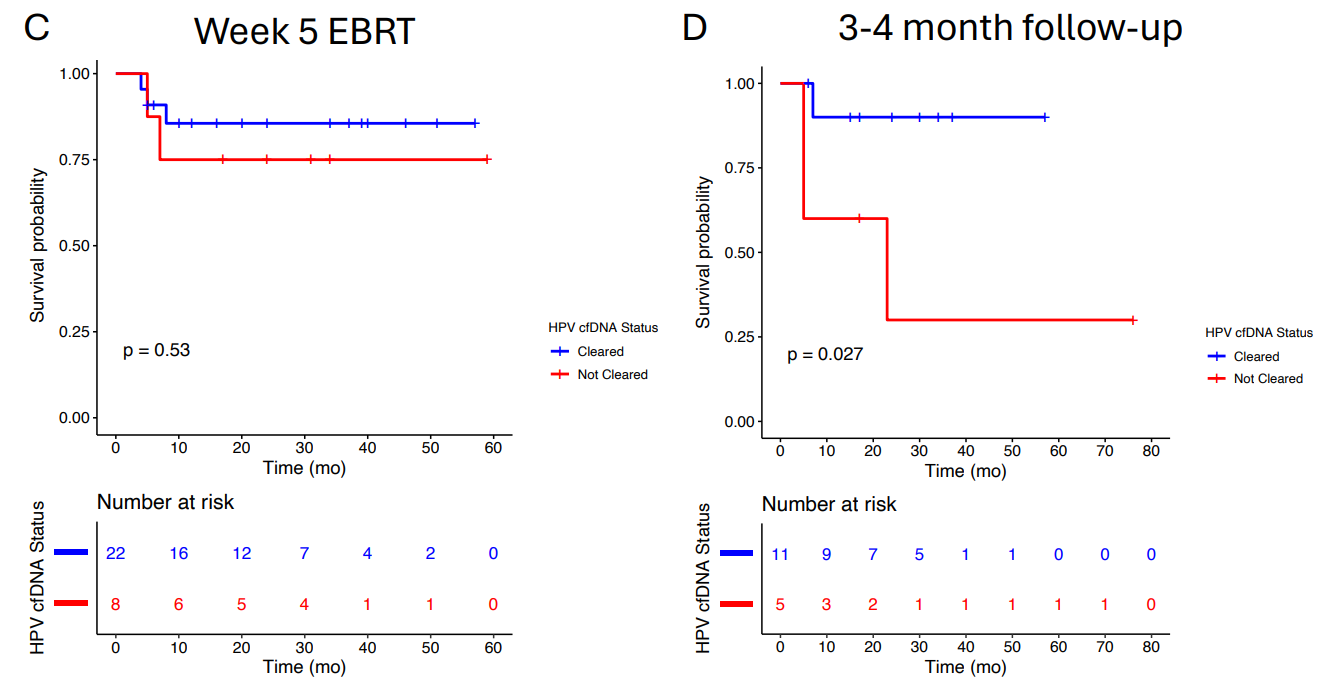
早些时候报道,试验中接受 5 剂 Versamune HPV + CRT 的 8 名患者的 36 个月总生存率 (OS) 和无进展生存率为 100%,17 名接受至少 2 剂 Versamune HPV + CRT 的患者的 36 个月 OS 率为 84.4%。
PDS0101(Versamun HPV)是一款针对HPV阳性的靶向治疗性癌症疫苗。2024年美国放射肿瘤学会(ASTRO)年会上公布了PDS0101联合同步放化疗治疗局部晚期宫颈癌的2期IMMUNOCERV研究试验。该试验共纳入了17例患者,所有患者都接受至少两剂PDS0101,结果显示:36 个月总生存率(OS)为84.4%,36 个月无进展生存期(PFS)率为74.9%。
目前癌症疫苗临床试验正在全国范围内寻找患者,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
https://aacrjournals.org/clincancerres/article-abstract/31/4/697/751733/Human-Papilloma-Virus-Circulating-Cell-Free-DNA

相关推荐
随便看看
- 癌症治疗新突破:mRNA癌症疫苗让晚期肿瘤显著消退,肺癌、胰腺癌、肝癌、黑色素瘤等患者获益
- 癌症疫苗PDS0101联合治疗方案用于头颈癌的最终顶线生存数据公布
- 存活超五年!古巴肺癌疫苗有何过人之处?为什么越来越多的患者前往古巴寻求癌症疫苗治疗?
- 个性化新抗原癌症疫苗GEN-009联合PD-1抑制治疗晚期实体瘤的1期试验的长期结果公布
- mRNA疫苗加帕博利珠单抗在黑色素瘤中实现83%的缓解效果
- 2年不进展!癌症疫苗创造晚期患者生存奇迹,无进展生存期延长1倍!
- 艾博生物靶向EGFR突变新型mRNA治疗性肿瘤疫苗-ABOR2013的研究成果即将亮相2025年AACR年会
- 87.5%患者3年未复发!癌症疫苗崛起:乳腺癌、肺癌、胃癌、黑色素瘤、宫颈癌患者生存期有效延长
- 肿瘤mRNA疫苗进展:黑色素瘤、胰腺癌、肺癌、乳腺癌、头颈癌的希望
- 癌症疫苗数据惊艳ASCO!癌症疫苗联合治疗延长生存期超2年,患者肿瘤缩小、生存期延长!











