12月20日,美国食品药品监督管理局(FDA)加速批准 encorafenib(Braftovi,康奈非尼)联合西妥昔单抗和 mFOLFOX6方案用于具有 BRAF V600E 突变的转移性结直肠癌 (mCRC) 患者。
此次批准主要基于BREAKWATER (NCT04607421)的临床数据,结果显示:encorafenib + 西妥昔单抗 + mFOLFOX6 组的客观缓解率(ORR)为 61%,对照组为 40%,联合治疗组中位缓解持续时间(DOR)为 13.9 个月,对照组为 11.1 个月。
最常见的不良反应 (≥25%) 是周围神经病变、恶心、疲劳、皮疹、腹泻、食欲下降、呕吐、出血、腹痛和发热。最常见的 3 级或 4 级实验室异常 (≥20%) 是脂肪酶升高和中性粒细胞计数降低。
典型病例
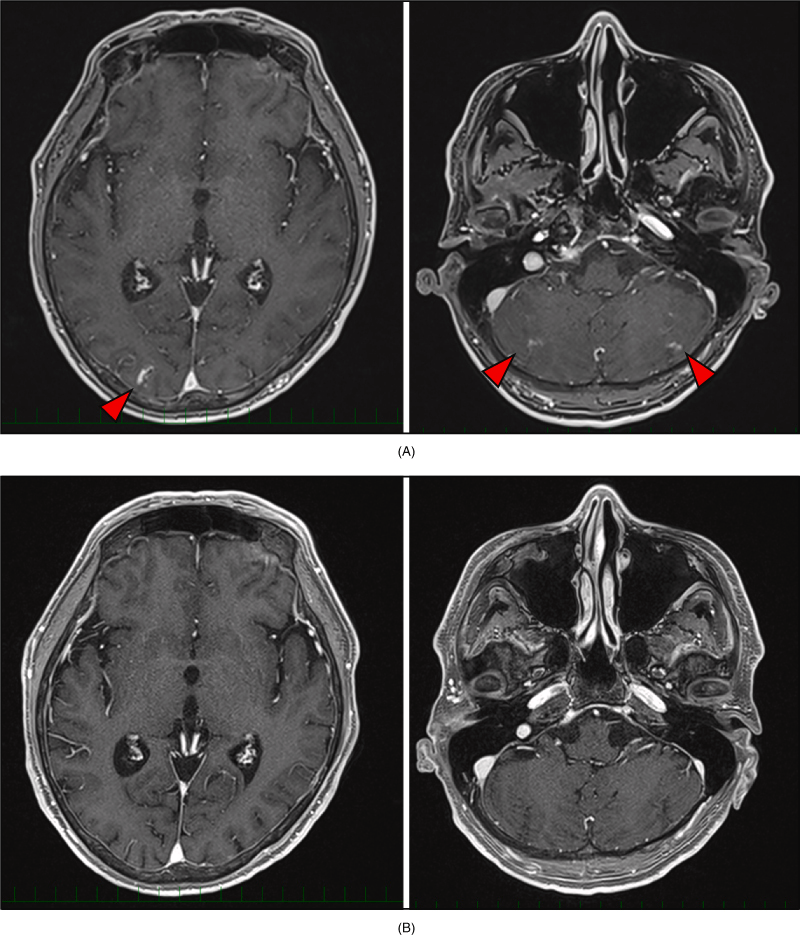
2022 年 10 月,一名 53 岁的男性因腹痛而就诊,被诊断为升结肠癌,并伴有肝转移、肺转移和腹膜播散。既往接受手术、化疗等治疗后,病情持续进展。于是患者开始使用encorafenib联合binimetinib和西妥昔单抗,一个月后,脑转移和软脑膜疾病有显著改善,肝脏和肺部的转移病灶也得到了很好的控制。
BRAF参与丝裂原活化蛋白激酶(MAPK)通路,当BRAF突变发生时,会导致细胞不受控制的生长和增殖,导致癌症的发生。BRAF突变见于多种癌症,包括黑色素瘤、甲状腺癌、结直肠癌、非小细胞肺癌。
BRAF是恶性肿瘤的驱动基因之一,可传导来自各种刺激的信号,触发细胞生长、增殖、分化和存活。据报道,肺癌中BRAF突变的发生率为0.9%至8.9%。这些突变已在多种肺癌组织学类型中发现,包括腺癌、鳞状癌和大细胞癌,但在腺癌中更为普遍。
目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以联系康和源免疫之家医学部(400-880-3716)。
项目名称:妥拉美替尼联合维莫非尼治疗BRAF V600E突变的晚期非小细胞肺癌Ⅱ期临床研究
部分入选标准:
1.年龄18-75周岁,性别不限;
2.预期生存期>3个月;
3.能够提供BRAF V600E突变的基因检测报告;
4.至少有一处符合RECIST v1.1定义的可测量病灶。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可致电至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
2.https://pmc.ncbi.nlm.nih.gov/articles/PMC11137764/












