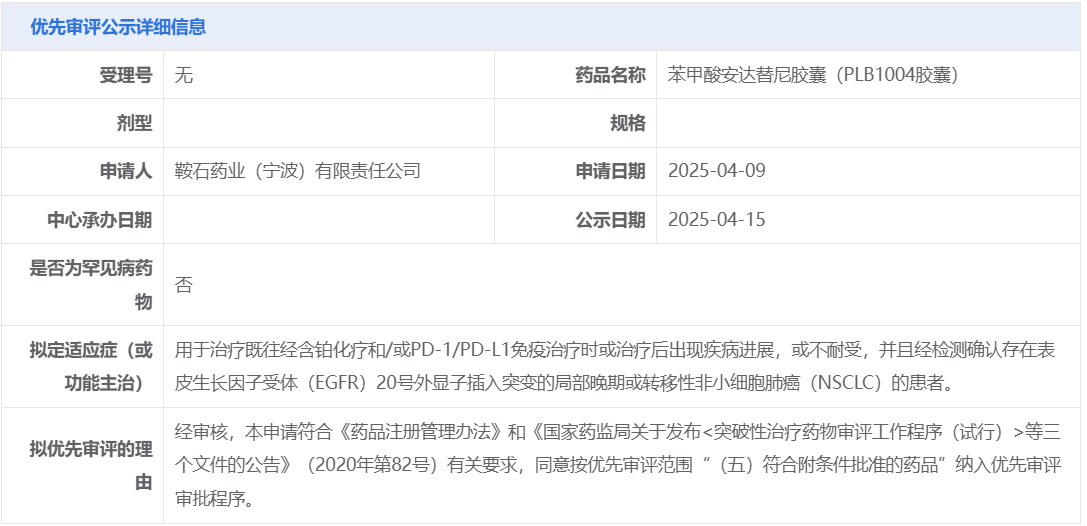
4月15日,国家药品监督管理局药品审评中心(CDE)显示:鞍石药业申请的苯甲酸安达替尼胶囊(PLB1004胶囊)拟纳入优先审评,用于治疗既往经含铂化疗和/或PD-1/PD-L1免疫治疗时或治疗后出现疾病进展,或不耐受,并且经检测确认存在表皮生长因子受体(EGFR)20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)的患者。
PLB1004是新型小分子酪氨酸激酶不可逆抑制剂(EGFR-TKI),具有高选择性,可以透过血脑屏障。
2024世界肺癌大会(WCLC)上,鞍石生物科技公布了伯瑞替尼联合PLB1004胶囊治疗既往接受EGFR-TKI治疗失败后,具有表皮生长因子受体(EGFR)突变、间质-上皮转化因子(MET)扩增和/或过表达的局部晚期或转移性非小细胞肺癌(NSCLC)的患者初步研究结果(MA12.11)。
在2024WCLC大会公布的研究中共纳入44例EGFR-TKI治疗后进展、经NGS和/或FISH检测伴MET扩增的EGFR突变局部晚期或转移性NSCLC患者,采用伯瑞替尼联合PLB1004治疗,主要终点为剂量递增阶段的剂量限制性毒性(DLT)、最大耐受剂量(MTD)、不良事件(AE),以及剂量扩展阶段的客观缓解率(ORR)、缓解持续时间(DoR)、疾病控制率(DCR)、无进展生存期(PFS)、总生存期(OS)、2期推荐剂量(RP2D)。相较于其他既往接受EGFR-TKI治疗失败后,具有表皮生长因子受体(EGFR)突变、间质-上皮转化因子(MET)扩增和/或过表达的局部晚期或转移性非小细胞肺癌(NSCLC)临床研究,伯瑞替尼联合PLB1004胶囊是唯一仅凭NGS检测MET扩增阳性即可入组无阈值限制的临床研究,数据更具有临床普适性 。
截至2024年6月30日,共41例患者疗效可评估。中位随访5.4个月,26例(59%)的患者仍在治疗中。整体患者的ORR为48.8%。亚组分析显示,经NGS检出MET扩增患者的ORR为54.3%,基线伴脑转移患者的ORR高达66.7%。整体患者的中位PFS为8.5个月
目前有临床试验正在寻找患者,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。

相关推荐
随便看看
- 疾病控制率为85.0%!ADC药物HS-20093获美国FDA突破性疗法认定,小细胞肺癌患者福音
- 氟唑帕利单药或联合方案用于晚期卵巢癌的研究亮相《临床医师癌症杂志》
- Zotiraciclib获得FDA快速通道认定
- 紫杉醇
- KRAS G12C抑制剂Krazati再获FDA批准,用于结直肠癌
- 宗艾替尼纳入突破性治疗
- 颅内客观缓解率高达90.9%!新型ALK/ROS1抑制剂伊鲁阿克疗效数据出炉,治疗非小细胞肺癌患者疗效惊艳
- ADC药物SHR-A1811治疗HER2表达或突变实体瘤疗效数据出炉!
- EGFR/HER2小分子抑制剂马来酸美凡厄替尼片获批上市
- 生存超过65个月!奥希替尼耐药不用担心,新型EGFR抑制剂强势来袭!EGFR突变肺癌不再可怕!











