
在现代医学领域,细胞免疫疗法(cellular immunotherapy)作为一种新兴的癌症治疗手段,近年来受到越来越多的关注。2024年细胞免疫疗法终于爆发了!
除了近几日火爆的CAR-T疗法和TIL疗法,T细胞受体工程化T细胞(TCR-T)疗法也是一种潜在的癌症治疗细胞免疫疗法。
由于CAR-T疗法在治疗B细胞恶性肿瘤方面具有显著的疗效,人们对 CAR-T疗法的兴趣已超过TCR-T疗法。然而,由于CAR-T试验迄今为止未能在实体癌的治疗中引起令人满意的反应,因此TCR-T疗法越来越受到关注。
关于TCR-T TCR-T细胞疗法也是过继细胞转移疗法(ACT)的一种,通过筛选和鉴定能特异性结合靶抗原的TCR序列,利用基因工程改造来自患者外周血的T细胞,然后将改造后的T细胞回输至患者体内,使其能特异性识别并杀伤表达抗原的肿瘤细胞,从而达到治疗肿瘤的目的。T细胞受体工程化T细胞疗法(TCR-T)治疗不受靶细胞表面抗原表达的限制,是一种潜在的肿瘤细胞免疫治疗方法。可广泛用于治疗包括实体瘤在内的多种恶性肿瘤细胞,在肿瘤治疗方面也显示出巨大的潜力。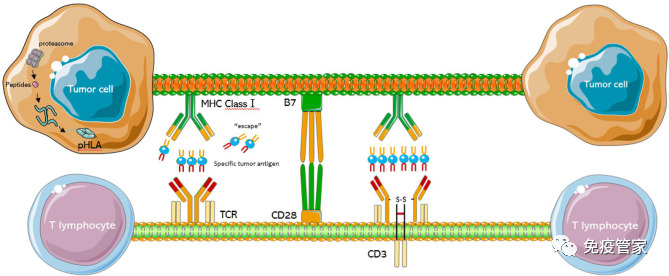
TCR-T细胞疗法在头颈癌、肝癌、黑色素瘤、滑膜肉瘤等实体瘤的治疗中都显示出巨大的潜力。
黑色素瘤 TCR-T细胞治疗实体瘤的临床试验首先在黑色素瘤患者中进行。2011年,研究人员报告了一项临床试验的结果:20例NY-ESO-1黑色素瘤患者中有11例(55%)接受了NY-ESO-1反应性TCR转导的自体T细胞,表现出客观的临床反应。黑色素瘤患者的估计总体3年和 5年生存率均为33%,4例黑色素瘤患者完全缓解。 其中一名完全反应者,表现出多发性肝和肺转移消退。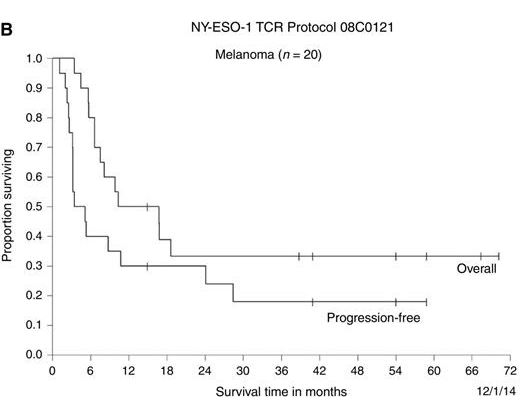
![]()
滑膜肉瘤 在上述临床试验中,纳入了18例NY-ESO-1滑膜细胞肉瘤患者,有11例(61%),接受了NY-ESO-1反应性TCR转导的自体T细胞。部分缓解持续3个月至18个月,3年和5年的总生存率分别为38%和14%。 两名滑膜细胞肉瘤患者有持续的临床反应:患者1表现出多发肺转移几乎完全消退,以及大盆腔骨病变大幅消退,均在治疗后持续了近 4 年(下图A);患者2所有转移病灶均完全消退,包括治疗后维持超过一年的多发性肺转移(下图B)。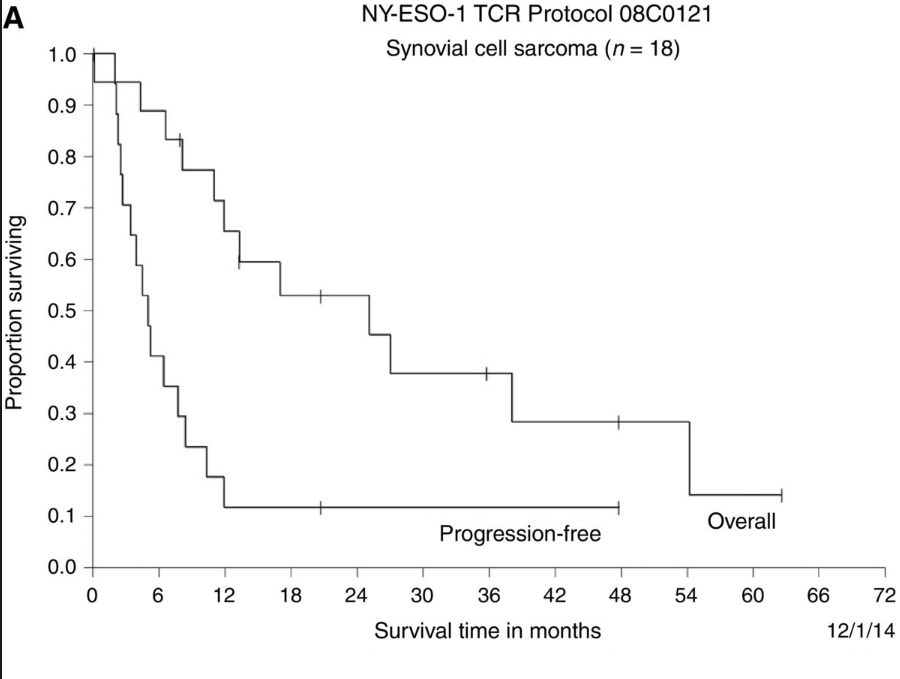
![]()
如何参加TCR-T临床试验 值得庆幸的是医瘤界这里有一款TCR-T针对滑膜肉瘤的临床试验正在全国范围内寻找受试者 项目名称:TC-N201注射液治疗滑膜肉瘤的1期临床研究 部分入选标准: 1.年龄18至70周岁(含18和70),性别不限 ; 2.预期生存期至少3个月 ; 3.美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)评分体能状态为0-1的受试者 ; 4.经组织病理学确诊的转移性或者复发性实体肿瘤(如食管癌、滑膜肉瘤、恶性黑色素瘤等)。 想要参加临床试验的患者可致电康和源免疫之家医学部(400-880-3716)了解详情后提交病理报告、治疗经历等资料进行初步评估。
即将上市的TCR-T 1月31日,Adaptimmune Therapeutics公司宣布,美国食品药品监督管理局(FDA)已经接受了其工程化T细胞受体(TCR)T细胞疗法afamitresgene autoleucel(Afami-cel)的生物制剂许可申请(BLA),并授予其优先审评资格。该申请的目标日期为2024年8月4日。 在SPEARHEAD-1试验中,70%对Afami-cel有反应的晚期滑膜肉瘤患者中在治疗两年后仍然保持存活。
综上所述,TCR-T细胞疗法是一种治疗肿瘤的强效免疫疗法,在众多癌症治疗中都有着明显的疗效。但是TCR-T细胞疗法的临床应用仍然具有挑战性。我们相信,TCR-T疗法能在科研人员的不懈努力下在癌症领域发挥更重要的作用。,成为抗癌治疗的重要组成部分。
扫描下方二维码,或者直接电话咨询康和源免疫之家医学部(400-880-3716),为癌友患者们分享更多信息。

免责声明:康和源免疫之家为免疫科普平台,文本参考来源于网络,版权归原作者所有。
该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!
参考资料
A Pilot Trial Using Lymphocytes Genetically Engineered with an NY-ESO-1–Reactive T-cell Receptor: Long-term Follow-up and Correlates with Response | Clinical Cancer Research | American Association for Cancer Research (aacrjournals.org)
相关推荐
随便看看
- 第三代 T 细胞受体工程 T 细胞(TCR-T)疗法MDG1015获美国FDA 新药研究申请
- TCR-T细胞产品Lete-cel获得突破性疗法认定
- 肿瘤病灶完全消失!TCR-T疗法对抗实体瘤获突破!54.5%患者肿瘤显著缩小
- 国内首款!TCR-T细胞产品TAEST16001注射液纳入突破性治疗品种名单
- 6个月肿瘤消失!TCR-T疗法为实体瘤患者迎来新希望,93%患者肿瘤缩小!
- 68.8%患者病情控制!TCR-T疗法治疗实体瘤临床数据积极,肺癌、肠癌、黑色素瘤患者肿瘤显著缩小
- TCR-T细胞疗法针对实体瘤患者的临床试验开始了
- 美国已上市!TCR-T疗法1年存活率高达90%,为多癌种患者带来长期生存
- 来恩生物mRNA TCR-T细胞疗法GZL-016注射液获得临床试验默示许可
- 67%的患者病情稳定!TCR-T细胞疗法让晚期黑色素瘤患者肿瘤缩小,症状明显改善!











