近日,君赛生物基因修饰型TIL疗法GC203在I期临床试验(KUNLUN-001)研究分中心重庆大学附属肿瘤医院完成首例受试者细胞回输后的首次肿瘤评估,患者肿瘤整体缩小约40%,达到部分缓解(PR)。
GC203是全球首款非病毒载体基因修饰TIL疗法,于2024年4月28日经NMPA批准进入临床试验,是目前国内唯一一个正式开展注册临床试验的基因修饰TIL疗法。该产品依托君赛生物自主开发、全球领先的DeepTIL®细胞富集扩增与NovaGMP®基因修饰技术平台开发而成,采用非病毒载体,在无高浓度IL-2、无滋养细胞的条件即可培养出足量高活性的TIL细胞,且对IL-2无依赖性,解决了常规TIL疗法依赖大剂量化疗清淋预处理,大剂量IL-2注射的临床痛点。
此前,GC203的安全性已得到亲历临床的受试者与研究者的实证,首次肿瘤评估达到PR进一步确证了GC203颇具前景的临床疗效,有望为更多患者带来新的治疗选择!
H女士从未想过有一天自己会登上肿瘤浸润淋巴细胞(TIL)这辆“细胞治疗复兴号”。
2023年初,H女士察觉腹股沟和腰部偶发疼痛,当时并未予以重视。直到3月份,疼痛不断加剧,在家人提醒下,H女士入院检查才发现自己腹膜后、腹股沟等多处的淋巴结肿大,已存在肿瘤转移可能。H女士于2023年3月首次进行了手术探查,术后病理结果证时了该疾病并非简单的疼痛,而是卵巢高级别浆液性癌(high-grade serous ovarian cancer,HGSOC),并且已经到了IVB期。卵巢癌是我国女性生殖系统第四大确诊癌症,呈逐年上升的趋势,严重威胁女性健康。上皮性卵巢癌中约70%为HGSOC,是一种具有侵袭性特征的常见亚型,高达70%的HGSOC患者在确诊时已处于盆腔外腹膜转移状态(Ⅲ/Ⅳ期)。全面分期手术和辅助化疗是HGSOC的标准疗法,然而约70%的患者会在术后2年内复发,进而产生继发性耐药。H女士一年多来认真接受传统治疗,先后进行了新辅助化疗、妇科晚期肿瘤减瘤手术,一线化疗联合抗血管生成药物以及免疫治疗,后期使用PARP抑制剂维持。漫漫抗癌路使H女士身心俱疲,健康每况愈下,今年8月份,肿瘤竟再次复发。
这次H女士有了一个新的选择--TIL细胞疗法!然而,常规TIL疗法繁琐的治疗过程,清淋化疗、IL-2注射带来的不良反应,长时间的住院重症监护让H女士及家人迟迟难以下定决心。
在仔细了解GC203无需清淋级预处理、无需IL-2注射、普通病房即可治疗的临床方案,及前期临床试验中GC203展现出的良好安全性和疗效后,H女士放下顾虑,参与了君赛生物GC203的这项临床试验。整个治疗过程仅出现持续几小时的发热和一过性的血象降低,出院时H女士身体状态一切良好。在之后的出院随访中也未见任何异常,接受治疗后的28天,H女士感受到左侧颈部的淋巴结已较前缩小。42天后的第一次肿瘤评估,H女士的整体肿瘤竟缩小了37.3%,CA125也较之前大幅度降低。
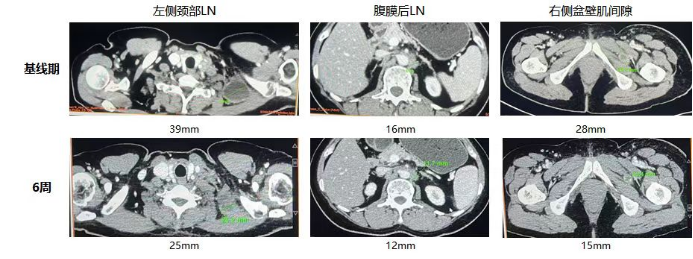
这次H女士回院肿瘤评估后,龚主任高兴地表示:“在保证安全的前提下,GC203 TIL的产品疗效也同样充满了惊喜,首个受试者首次肿瘤评估就已经达到了PR,肿瘤缩小了约40%,我更加期待此疗法能够早日惠及更多的受试者。”
如何参加TIL细胞临床试验目前国内多家权威三甲医院已开展TIL细胞疗法针对实体瘤的临床试验,且正在寻找患者,包括但不限于黑色素瘤、非小细胞肺癌、宫颈癌等。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
项目名称:HS-IT101注射液治疗晚期实体瘤患者的临床试验
部分入选标准:
1.年龄为18-75岁;
2.晚期实体瘤患者,包括但不限于黑色素瘤、非小细胞肺癌、宫颈癌等;
3.预期生存时间≥3个月;
4.有可测量病灶。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。

相关推荐
随便看看
- ROS1融合阳性非小细胞肺癌患者经GC101 TIL治疗后肿瘤缩小33%
- 抗癌利器TILS疗法上演碟中谍“戏码”让肿瘤无处可逃!
- 无癌超4年!TIL细胞疗法创造生命奇迹,黑色素瘤、子宫内膜癌、头颈癌、宫颈癌等患者获益
- 奇迹!TIL疗法有效率超90%,23岁癌症女孩肿瘤完全消失!
- 华赛伯曼自主研发的FAST-TIL(HS-IT101)临床试验数据亮相2026 AACR
- 这波流量TILS疗法先占了!国内外多款产品主攻实体瘤领域!黑色素瘤,宫颈癌都害怕!
- TILS作为对抗肿瘤的“潜力股”你知道多少
- 美国FDA授予肿瘤浸润淋巴细胞(TIL)疗法OBX-115再生医学高级疗法(RMAT)称号,用于黑色素瘤
- 癌症克星登场!TIL细胞疗法惠及肺癌、宫颈癌、黑色素瘤……持续缓解超三年
- 国内首例TIL治疗患者成功实现完全缓解!国内TIL疗法勇战肝癌、宫颈癌











