12月3日,中国医学科学院血液病医院研究人员在国际权威学术期刊《Blood Advances》发表了题为:Inaticabtagene Autoleucel (CNCT19) in adult relapsed or refractory B-cell acute lymphoblastic leukemia的研究论文,文中报告了CAR-T药物纳基奥仑赛(CNCT19)治疗成人复发难治急性B淋巴细胞白血病(r/r B-ALL)的II期HY001201研究(NCT04684147)试验的长期疗效和安全性数据。

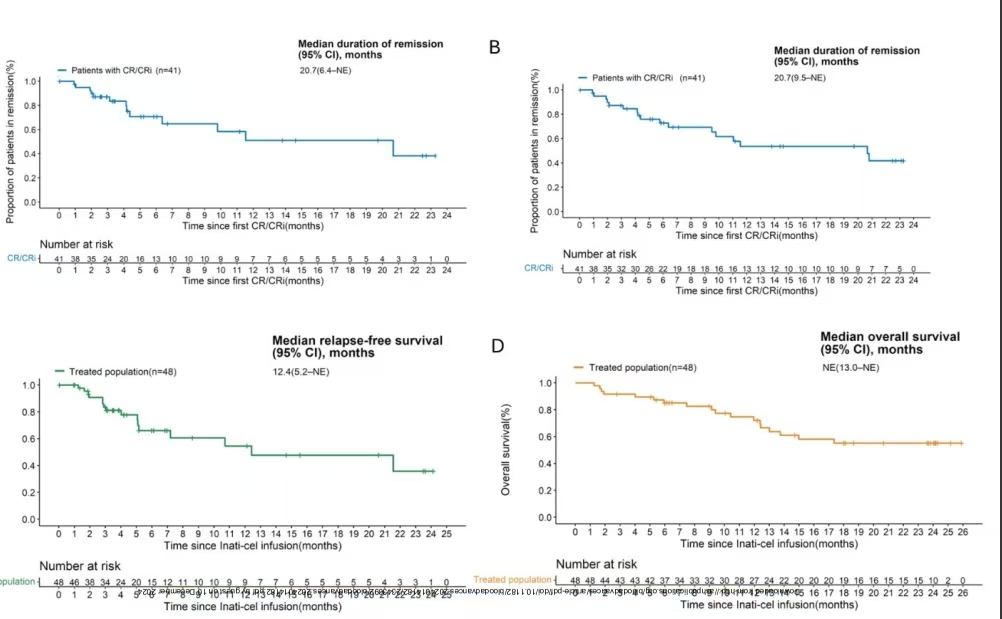
共48例患者接受纳基奥仑赛注射液输注,结果显示:最佳客观缓解率(ORR)为85.4%,其中35例患者达到完全缓解(CR),6例患者为完全缓解伴血液学不完全恢复(CRi),这41例患者均达到微小残留病变(MRD)阴性,中位缓解持续时间(DOR)为20.7个月,中位无复发生存期(RFS)为12.4个月,预估12个月无复发生存率为54.5%,24个月无复发生存率为35.8%,中位总生存期(OS)未达到,预计12个月生存率为72.1%,2年总生存率为55.2%。
关于纳基奥仑赛
源瑞达(纳基奥仑赛注射液,CNCT19,Inaticabtagene Autoleucel Injection)是具有自主知识产权的靶向CD19的CAR-T细胞治疗产品,2023年11月,获得国家药品监督管理局(NMPA)批准上市用于治疗成人复发或难治性B细胞急性淋巴细胞白血病。
2024年4月,国际权威学术期刊《Journal for ImmunoTherapy of Cancer》发布了纳基奥仑赛联合自体造血干细胞移植用于治疗复发难治大B细胞淋巴瘤(r/r LBCL)的临床数据。
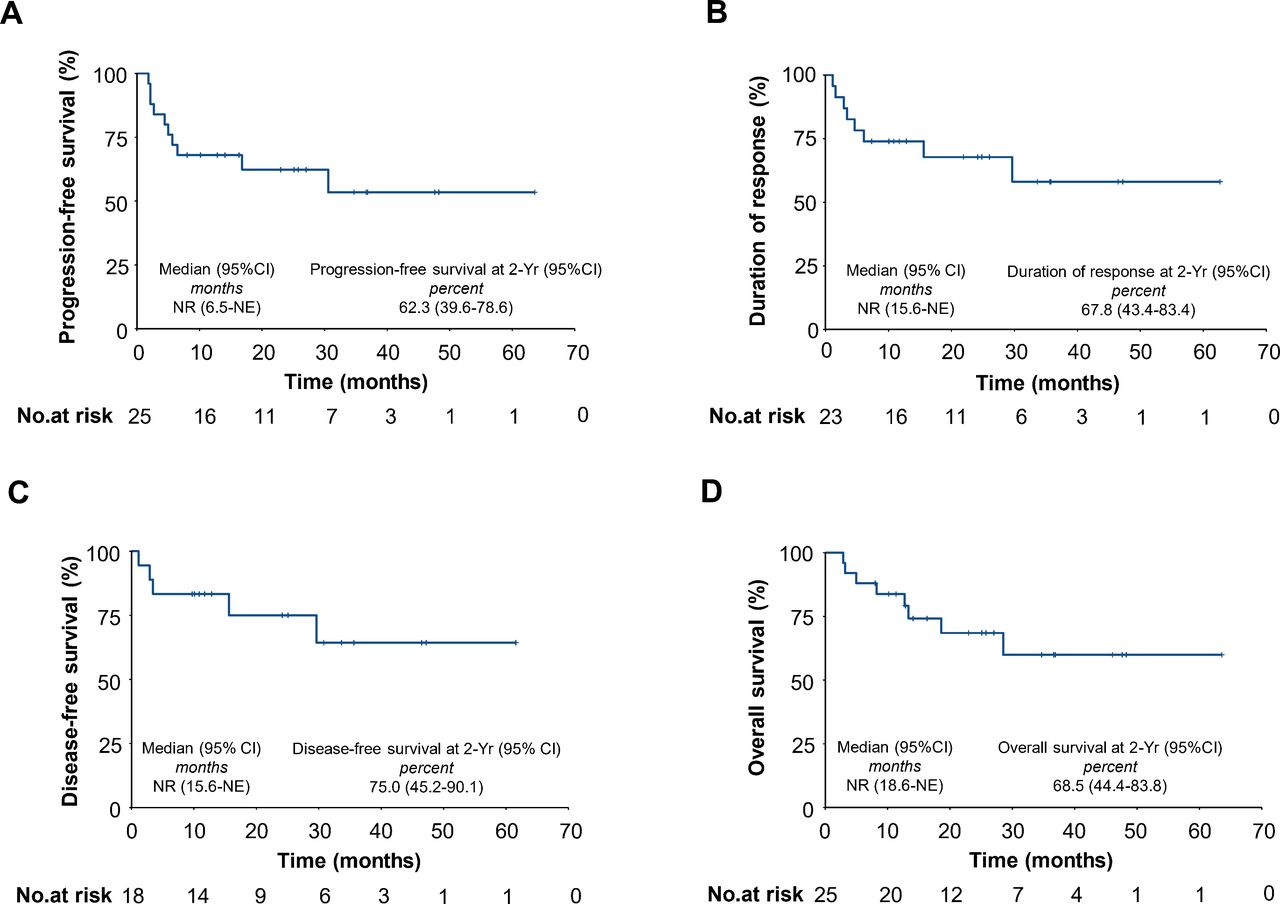
该试验共25例患者接受治疗,结果显示:客观缓解率(ORR)为92%,完全缓解(CR)率为72%,2年缓解持续时间(DOR)为64.9%,2年无进展生存率(PFS)为62.3%,2年总生存率(OS)为68.5%,2年无病生存率(DFS)为64.9%。
目前有靶向CD19/CD22/BCMA的CAR-T细胞产品正在进行临床试验,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://ashpublications.org/bloodadvances/article/doi/10.1182/bloodadvances.2024014182/534301/Inaticabtagene-Autoleucel-CNCT19-in-adult-relapsed
2.https://jitc.bmj.com/content/12/4/e008857.long

相关推荐
随便看看
- RD13-02治疗T 细胞急性淋巴细胞白血病/淋巴瘤患者的最新临床数据
- 血液肿瘤“神药”CAR-T疗法“跨界”实体肿瘤,胃癌、胰腺癌、肝癌、卵巢癌等福音
- 美国FDA授予C-CAR168再生医学先进疗法认定,用于系统性红斑狼疮和狼疮肾炎
- CAR-T细胞产品纳基奥仑赛注射液亮相2025 ASCO和EHA
- EpCAM CAR-T细胞治疗产品IMC001新增适应症IND申请获受理
- 晚期胰腺癌患者接受KD-496 CAR-T治疗后实现持续缓解
- 靶向CD7的通用型CAR-T细胞疗法CTD402新药临床试验申请获FDA批准
- CAR-T疗法2.0版来了!“体内CAR-T”疗法,告别百万天价与漫长等待!体内直接编程,癌细胞6小时清零?
- 惊爆!国内外CAR-T细胞疗法在癌症治疗领域“狂飙”,骨髓瘤、白血病、淋巴瘤患者的“救命稻草”!
- “谈成了!”百万一针的CAR-T有望飞入寻常百姓家,CAR-T疗法的“天价”门槛,这次真的松动了











