12月25日,易慕峰生物宣布其自主研发的靶向EpCAM自体CAR-T细胞注射液产品(IMC001)新增适应症的临床试验申请已获得中国国家药品监督管理局药品审评中心(CDE)受理,用于治疗上皮性晚期实体瘤。
IMC001是一款靶向EpCAM的CAR-T细胞产品,IMC001的开发旨在通过靶向EpCAM,解决转移和复发难题,为晚期消化系统肿瘤提供一种新的治疗选择。IMC001于2023年8月获得美国FDA ODD认定,其IND申请于2024年2月获得中美双报批准,是全球首个中美双报获批IND的靶向EpCAM的CAR-T产品。
2024年美国临床肿瘤学会(ASCO)年会上报告了IMC001用于治疗晚期胃癌的研究成果。共11例患者接受治疗,10例患者可评估疗效,结果显示:3例患者实现部分缓解(PR),6例患者病情稳定(SD),疾病控制率(DCR)为90%。该试验中1例患者在IMC001治疗16周后肿瘤缩小了48%。
IMC001有望为上皮性晚期实体瘤患者提供新的治疗选择,满足临床上对有效疗法的迫切需求。
EpCAM是一种I型跨膜糖蛋白,在食管癌、结直肠癌、胰腺癌、卵巢癌、肺癌、胃癌、乳腺癌等多种人上皮源性肿瘤的膜上均匀且高表达1,而在正常组织中的表达相对较低2。在一项研究中,129例正常胃黏膜均未见EpCAM表达,但是在77%胃癌中观察到EpCAM的表达且56%为中高表达。另外有研究显示转移性乳腺癌患者100%表达EpCAM4。由于EpCAM在肿瘤恶性转化后从基底外侧转变为细胞膜表面,并且在原位灶、转移灶和循环肿瘤细胞中均呈现高表达,这使得EpCAM成为了CAR-T细胞治疗的一个潜在靶点,并显示出在多种上皮源性肿瘤治疗中的潜在应用价值。
2023年12月,《科学》杂志发表了题为“EpCAM-targeting CAR-T cell immunotherapy is safeand efficacious for epithelial tumors”的研究论文,文中报告了CAR-T细胞在上皮肿瘤中的临床(NCT02915445)疗效。

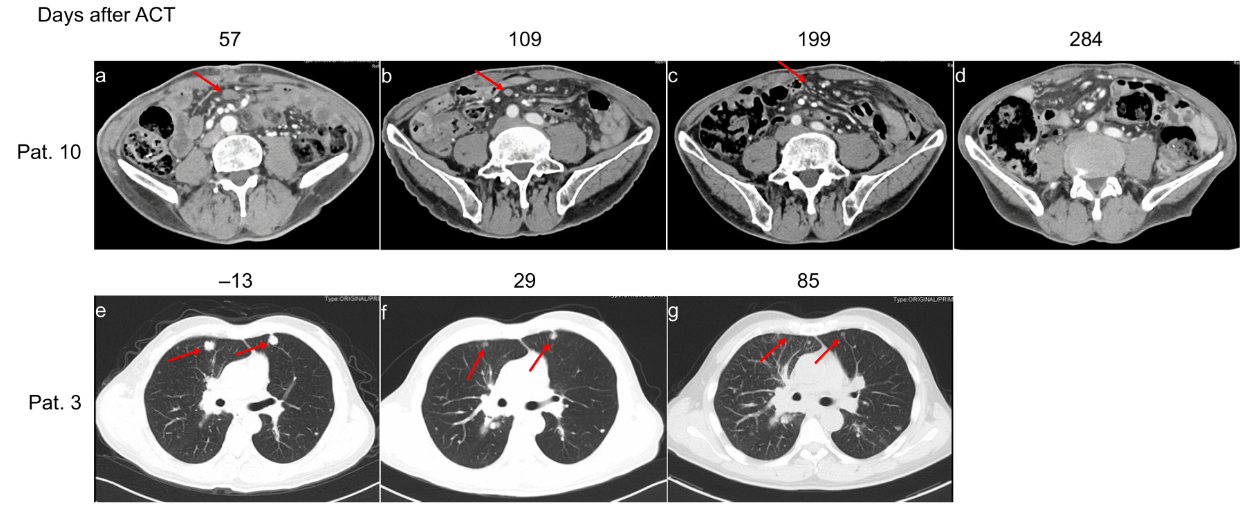
上皮肿瘤是指发生在人体上皮组织中的一种肿瘤。该试验中3例患者实现无进展生存(PFS)超700天。典型病例如下:其中1例患者在CAR-T细胞治疗7个月后腹膜肿瘤缩小,另1例患者在治疗3个月后肺部肿瘤实现部分缓解(PR)。
目前CAR-T细胞疗法临床试验正在寻找卵巢癌患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
部分入选标准:
1.年龄18-70岁,男女不限;
2.标准治疗失败的卵巢癌患者;
3.预计生存时间≥3个月;
4.ECOG评估0-1分;
5.存在可测量病灶。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.science.org/doi/10.1126/sciadv.adg9721

相关推荐
随便看看
- 靶向GPC3 CAR-T疗法大揭秘,肝癌患者肿瘤几乎消失
- 一名同时患有三种自身免疫疾病的女性在CAR-T 细胞治疗后症状完全消失
- 热点聚焦:靶向间皮素的CAR-T细胞疗法携手帕博利珠单抗,胸膜间皮瘤不再可怕
- 化疗、靶向药全耐药,肿瘤还在疯长?别慌,最后这张“底牌”CAR-T在晚期胃癌中打出“王炸”
- 超90%的缓解率!国产CAR-T细胞疗法拯救晚期多发性骨髓瘤、淋巴瘤、白血病患者
- 普瑞金生物自主研发的靶向BCMA的嵌合抗原受体T细胞注射液,针对难治性狼疮肾炎的新适应症临床试验申请获批
- 好消息!国内首款百万CAR-T按疗效付费,患者未完全缓解最高可退60万
- 全球首例体内CAR-T疗法治疗骨髓瘤
- 28天实现完全缓解!CAR-T疗法重锤T细胞淋巴瘤
- CAR-T细胞产品SYS6020获批临床用于治疗系统性红斑狼疮











