2月21日,国家药品监督管理局药品审评中心(CDE)显示:科济制药申报的CT041自体CAR T细胞注射液拟纳入突破性治疗,用于既往接受过至少二线治疗失败的Claudin18.2(CLDN18.2)表达阳性的晚期胃/食管胃结合部(G/GEJ)腺癌。

舒瑞基奥仑赛注射液(CT041)是一款针对Claudin18.2阳性的晚期消化系统肿瘤的CAR-T细胞候选产品,2024年6月,《自然医学》发表了舒瑞基奥仑赛注射液在Claudin18.2阳性的晚期消化系统肿瘤患者中的安全性和有效性的I期临床试验CT041-CG4006(NCT03874897)的最终结果。

该试验共98例患者参加试验,结果显示:疾病控制率(DCR)高达91.8%,38例患者实现缓解,总缓解率为38.8%,中位无进展生存期(PFS)为4.4个月,中位总生存期(OS)为8.8个月,中位缓解持续时间(mDOR)为6.4个月。90例基线靶病灶患者中,有70例患者实现不同程度的肿瘤缩小。
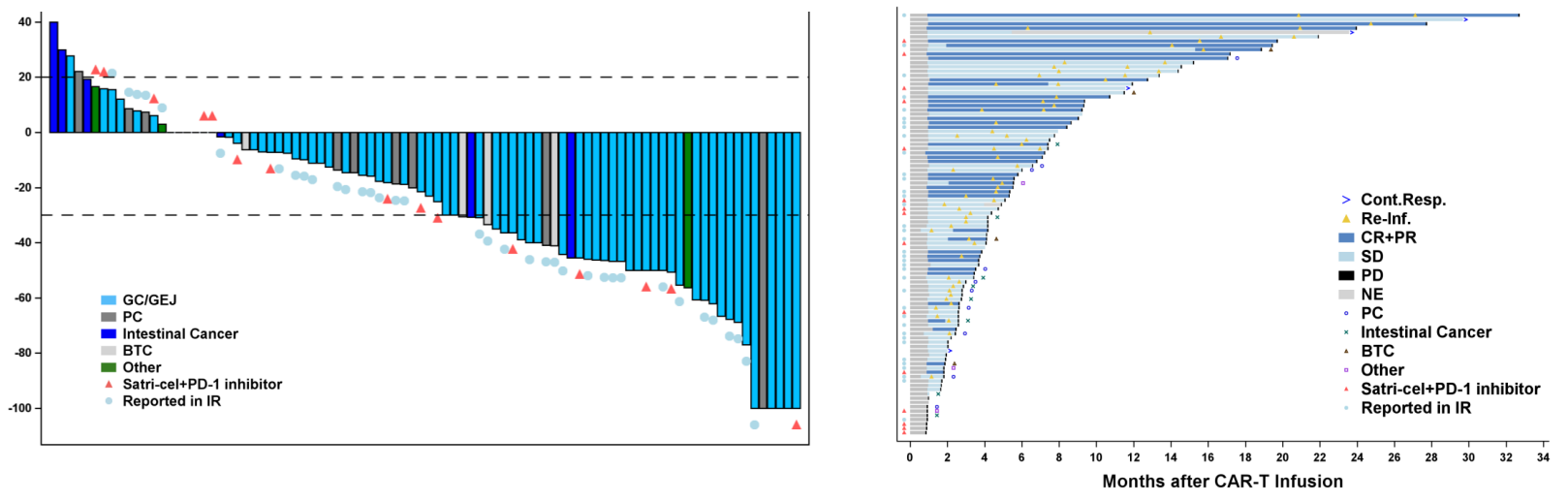
51例舒瑞基奥仑赛单药治疗的胃癌患者中,疾病控制率高达96.1%(49),总缓解率为54.9%(28),其中27例患者实现部分缓解(PR),1例患者完全缓解(CR),中位缓解持续时间(mDOR)为6.4个月。
典型病例
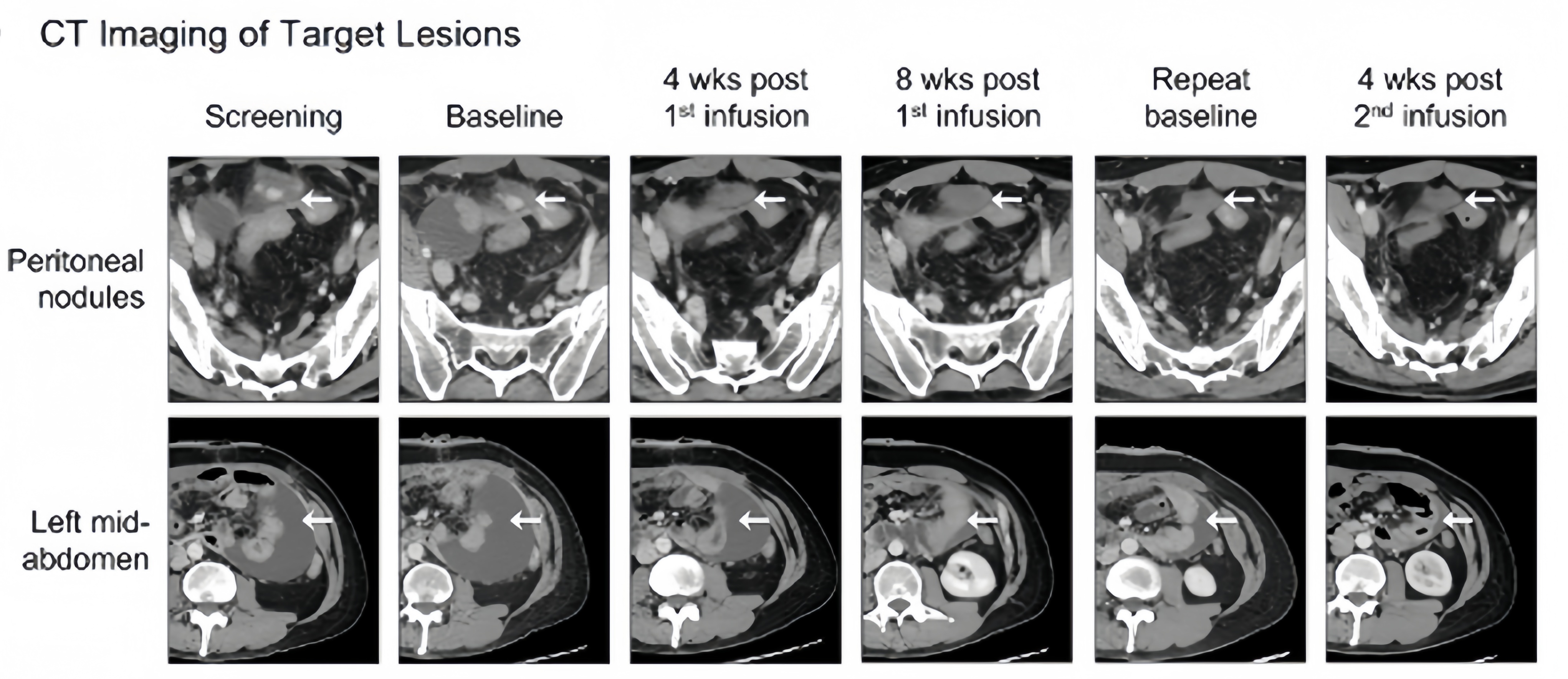
1例胃癌患者伴有沿膀胱圆顶和腹膜壁的两个腹膜结节,在CAR-T疗法CT041治疗后,两个腹膜靶病变明显减少,第四周患者就实现部分缓解(PR),第二次 CT041 输注后 4 周,患者实现完全缓解(CR)。
目前CAR-T细胞的临床试验正在寻找实体瘤患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.nature.com/articles/s41591-024-03037-z
2.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10860094/

相关推荐
随便看看
- 靶向CLDN18.2的自体CAR-T产品IMC002获得美国FDA孤儿药资格认定
- 好消息!国内首款百万CAR-T按疗效付费,患者未完全缓解最高可退60万
- 临床缓解5年后健康妊娠!癌症治疗新突破:CAR-T细胞疗法让癌细胞无所遁形,癌症患者迎来新生曙光!
- 100%缓解率!莱芒生物新型CAR-T疗法获《柳叶刀》子刊权威认可,为难治白血病患者带来新希望
- CAR-T产品IMC002 III期确证性临床研究全国启动
- 血液肿瘤“神药”CAR-T疗法“跨界”实体肿瘤,胃癌、胰腺癌、肝癌、卵巢癌等福音
- 全球首例通用现货型CAR-Vδ1T细胞药物(UTAA06)实体瘤患者给药
- 百万抗癌药CAR-T细胞疗法效果惊人但价格成“拦路虎”?价格高昂背后的抗癌希望
- 靶向PSCA的GoCAR-T 候选产品(BPX-601)在转移性胰腺癌和前列腺癌中的1 期剂量递增试验结果
- 全球首例体内CAR-T疗法治疗骨髓瘤











