
在与癌症的斗争中,科学家们从未停止探索更有效、更安全的治疗方法。近年来,一种新的抗癌方法-DC疫苗逐渐成为人们关注的焦点,为癌症患者带来了新的希望。
如果你或身边的人正在遭受癌症的困扰,不妨多了解一下DC疫苗,也许它就是你一直在寻找的抗癌新希望。咨询电话:400-880-3716。
DC疫苗,即树突状细胞疫苗,是一种肿瘤治疗性疫苗,利用人体的免疫系统来消灭癌细胞。
人体的免疫系统就像一支强大的军队,时刻守护着我们的身体健康。当外来病原体或异常细胞(如肿瘤细胞)入侵时,免疫系统会激活防御机制来攻击它们。然而,肿瘤细胞非常狡猾,并采用各种策略来逃避免疫系统的检测和攻击。而DC疫苗的出现,为免疫系统提供了更强大的"武器",帮助其重新识别并攻击肿瘤。
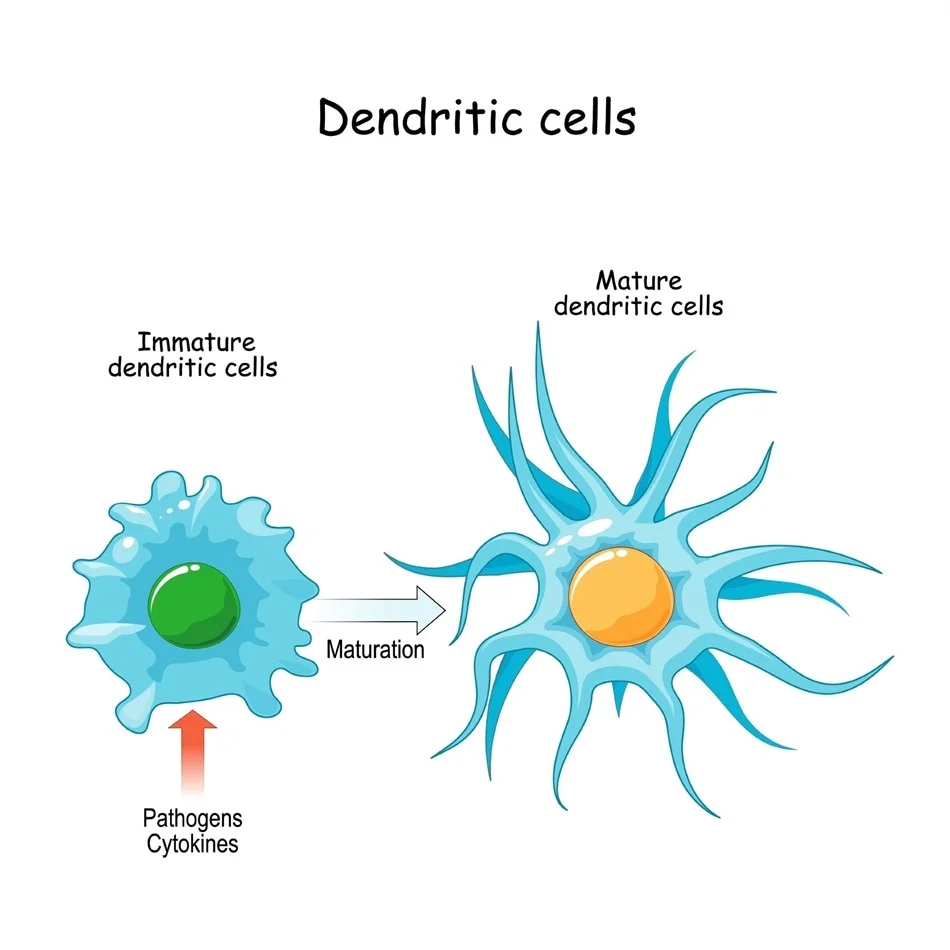
树突状细胞(DC)是人体内功能最强的专职抗原提呈细胞,这些具有独特树枝状突起的特殊细胞,堪称人体的“免疫指挥官”,它能够高效地摄取、加工处理和递呈抗原,激活T细胞,从而启动、调控和维持机体的免疫应答。
并且,树突状细胞具有巨大的表面积,可与周围大量细胞(如T细胞、自然杀伤细胞、中性粒细胞、上皮细胞等)紧密接触。实验表明,仅需1个成熟树突状细胞(mDC)即可激活100-3000个T细胞。
当病原体入侵时,未成熟树突状细胞识别入侵者,捕获抗原后迅速离开组织。穿过细胞间隙、跨越淋巴管内皮迁移至引流淋巴结。在从外周组织迁移过程中,树突状细胞经历显著的表型和功能成熟,积极向T细胞呈递抗原,激活T细胞。
虽然巨噬细胞和B细胞等其他免疫细胞也参与抗原呈递,但树突状细胞因其“交叉呈递”能力具有独特优势——它们能将外源性抗原通过MHC I类分子呈递,从而启动细胞毒性T细胞增殖。
DC肿瘤疫苗是利用DC细胞提呈抗原、激活免疫的功能,借助DC细胞来指挥T细胞。通过体外诱导或构建特异性识别肿瘤的DC细胞,并将其扩增后回输到肿瘤患者体内,激活T细胞,对癌细胞进行有效杀伤,从而达到治疗肿瘤的目的。
上世纪70年代,加拿大免疫学家拉尔夫·斯坦曼(Ralph Steinman)就发现了树突状细胞(DC)。2007年,斯坦曼被诊断出胰腺癌,作为树突状细胞(DC细胞)的发现者,他深知免疫系统在抗癌中的关键作用。于是,他决定利用DC细胞的特性,开发一种个性化疫苗。
令人震惊的是,他的病情得到了显著控制:原本预期仅剩几个月的生命,最终延长了四年半。

虽然斯坦曼的自我实验虽然未能彻底治愈癌症,但为癌症免疫治疗开辟了新方向。经过十余年的发展,DC疫苗已经逐渐从实验室研究走向临床应用。
近年来,随着生物技术的飞速发展,DC疫苗在癌症治疗领域取得了一系列重要的研究成果。
2025年欧洲血液学协会年会(EHA)年会于2025年6月12日至15日在意大利米兰盛大举行。EHA是欧洲乃至全球血液学领域最具影响力的学术会议之一,每年都会吸引来自世界各地的血液学专家、研究人员、临床医生和行业代表参加,是血液学领域交流和展示前沿成果的重要平台。此次大会上,恒赛生物公布其树突状细胞(DC)疫苗平台KSD-101的I期临床试验最新研究成果。
这项I期临床试验入组了多种类型的EB病毒相关淋巴增殖性疾病(EBV-LPDs)患者,包括血管免疫母细胞性T细胞淋巴瘤(AITL)、鼻型/外周型NK/T细胞淋巴瘤(ENKTL)、慢性活动性EB病毒感染(CAEBV)等。
中位随访42.7周时,研究显示KSD-101治疗带来了积极的疾病缓解,大部分患者达到了完全缓解(CR)并得以维持。
这一结果表明,KSD-101在治疗EBV-LPDs方面具有良好的有效性,为这类疾病的治疗提供了新的选择。
目前癌症疫苗有临床试验正在寻找食管癌患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
DC疫苗作为一种新型的癌症治疗手段,为癌症患者带来了新的希望。它独特的作用机制和良好的安全性,使其在癌症治疗领域具有广阔的应用前景。
然而,我们也要清楚地认识到,DC疫苗目前仍然处于研究和发展阶段,还需要更多的临床试验来验证其疗效和安全性。对于癌症患者来说,在选择治疗方法时,应该充分了解各种治疗方法的优缺点,并在医生的指导下做出合理的选择。
相信在不久的将来,DC疫苗将成为癌症治疗的重要手段之一,帮助更多的患者战胜癌症,重获健康。
参考资料
1.https://www.immunology.org/public-information/bitesized-immunology/cells/dendritic-cells
2.https://ar.iiarjournals.org/content/44/9/3713
康和源免疫之家 - 癌症患者的生命希望桥梁 康和源免疫之家作为肿瘤诊疗服务平台,始终秉持“以患者为中心”的理念。在肿瘤治疗领域,患者面临着巨大的身心压力和复杂的治疗选择,康和源免疫之家深知患者的需求和困境,致力于为患者提供全方位、个性化的服务。 为了实现这一目标,该平台整合了中国、美国、欧洲、日本、韩国等全球顶尖肿瘤专家资源。这些专家拥有丰富的临床经验和先进的治疗理念,能够为患者提供专业的诊断和治疗建议。同时,平台还与知名药企、创新药物研发机构建立了深度合作关系,这使得患者能够及时了解到最新的抗癌药物和治疗技术,为治疗提供更多的选择。 国际专家会诊服务 肿瘤治疗具有复杂性和个体差异性,不同患者的病情和身体状况各不相同,因此需要个性化的治疗方案。康和源免疫之家通过国际专家会诊服务,可协调中美欧日韩等多国权威肿瘤专家,针对癌症开展跨国联合诊疗。 对于那些需要第二诊疗意见的患者来说,国际专家会诊可以提供不同的视角和建议,帮助患者更全面地了解自己的病情和治疗方案。而对于寻求海外先进治疗方案的患者,平台的专业团队能够帮助他们获取国际最新治疗指南,为患者制定更加科学、合理的治疗计划。 临床试验 作为连接患者与创新疗法的纽带,康和源免疫之家与全球领先药企及研发机构保持战略合作,持续提供涉及PD-1/L1抑制剂、CAR-T细胞治疗、ADC药物等领域的临床试验项目。这些临床试验项目代表了当前癌症治疗的最新进展和研究方向,为患者提供了接触新型抗癌药物和治疗技术的机会。 康和源免疫之家团队会根据患者的病情阶段、基因检测结果和治疗史,精准匹配适合的临床试验机会。这不仅提高了患者参与临床试验的成功率,也确保了患者能够接受最适合自己的治疗。在康和源免疫之家,每个生命都被视为值得最好的医疗选择,无论是寻求国际顶尖专家的诊疗建议,还是尝试突破性的临床试验,平台都将竭诚为患者提供专业、可靠的全方位支持。让我们携手,在抗击肿瘤的征程上走得更远。 END 如果您或您身边的人正在遭受癌症的困扰,不妨拨打咨询电话400-880-3716,登录官网 https://www.myimm.net/ 或关注微信公众号“康和源免疫之家”(头条、知乎、百度、搜狐等自媒体同名),了解更多关于临床试验和肿瘤诊疗服务的信息。
相关推荐
随便看看
- 给免疫系统请一位“金牌教练”!DC疫苗实现脑瘤5年生存率翻倍,黑色素瘤12个月生存率率高达94%……
- 震撼!“免疫信使”树突状细胞放大招!DC疫苗精准打击癌细胞,黑色素瘤、肉瘤、肾癌、乳腺癌福音
- 5年总生存率达75%!DC疫苗在白血病、肝细胞癌、非小细胞肺癌中显奇效
- 疾病控制率达75%!树突状细胞(DC)疫苗重锤前列腺癌、肺癌、胶质母细胞瘤等
- 生存率惊人!DC疫苗为乳腺癌、胶质母细胞瘤、肠癌患者带来希望,肿瘤君不再“嚣张”
- CIK细胞冲向肝癌指南,DC-CIK解锁抗癌新密码!
- 一年生存率为88%!DC疫苗实现胶质母细胞瘤、肺癌、宫颈癌、尿路上皮癌长期生存
- 两年的总生存率达100%!DC疫苗来袭,对抗肿瘤不在话下
- 树突状(DC)细胞疗法是什么
- 2年未复发!哪些癌症适合树突状细胞(DC)疫苗?肿瘤患者迎来全新生机!











