9月12日,美国食品药品监督管理局(FDA)批准将 atezolizumab(阿替利珠单抗)和透明质酸酶-tqjs(Tecentriq Hybreza,Genentech, Inc.)作为 atezolizumab(Tecentriq,Genentech, Inc.)的静脉注射制剂用于所有成人适应症,包括非小细胞肺癌 (NSCLC)、小细胞肺癌 (SCLC)、肝细胞癌 (HCC)、黑色素瘤和肺泡软部分肉瘤 (ASPS)。

此次批准主要基于 IMscin001 (NCT03735121)研究试验,2024年5月8日,《Journal of Thoracic Oncology》发表了皮下注射阿替利珠单抗或静脉注射阿替利珠单抗的疗效。

该试验共纳入371例非小细胞肺癌(NSCLC)患者,其中247例患者接受皮下注射,124例患者接受静脉注射,结果显示:皮下注射组中位生存期(OS)为10.7个月,静脉注射组中位生存期(OS)为10.1个月。
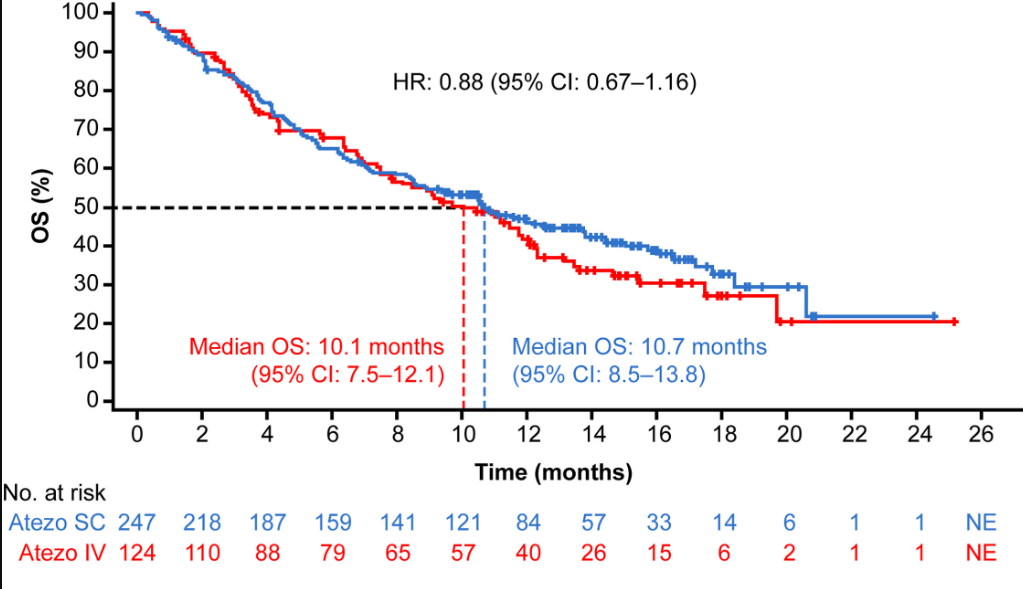
中位无进展生存期(PFS)分别为2.8个月和2.9个月,客观缓解率(ORR)分别为11.0%和10.5%,缓解持续时间(DOR)分别为15.1个月和11.2个月。
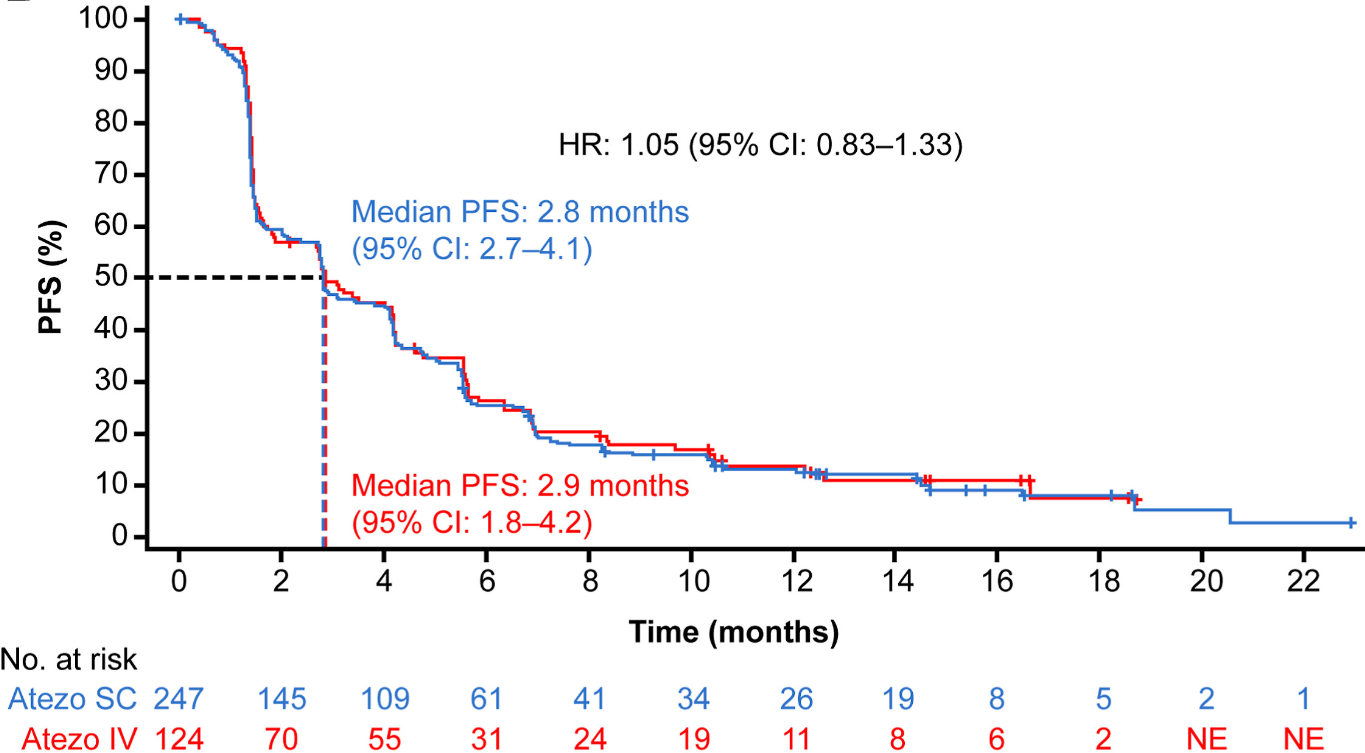
该数据表明,皮下注射阿替利珠单抗或静脉注射阿替利珠单抗疗效相似。
目前有临床试验正在寻找非小细胞肺癌患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-atezolizumab-and-hyaluronidase-tqjs-subcutaneous-injection
2.https://www.jto.org/article/S1556-0864(24)00210-7/fulltext

相关推荐
随便看看
- 卡瑞利珠单抗治疗小细胞肺癌2项临床数据即将公布于2024世界肺癌大会
- 美国FDA批准ADAM9靶向ADC新药DB-1317临床试验申请
- ADC药物德曲妥珠单抗DESTINY-Breast09 III期研究成果亮相2025 ASCO
- "生物导弹"精准打击!ADC药物为乳腺癌、胃癌等患者带来转机
- 欧洲药品管理局(EMA)授予KRAS G12C抑制剂戈来雷塞孤儿药疗法认定
- 在研 Rinatabart Sesutecan (Rina-S®) 在晚期卵巢癌患者中继续显示出令人鼓舞的抗肿瘤活性
- 芦康沙妥珠单抗第二项适应症获批
- 卡瑞利珠单抗辅助治疗高危局部晚期鼻咽癌Ⅲ期临床研究结果登《JAMA》
- Dato-DXd为晚期或转移性 HR+/HER2– 乳腺癌和三阴性乳腺癌患者带来曙光
- LM-108注射液拟纳入突破性治疗











