DB-1419是一款潜在同类首创的B7-H3/PD-L1双抗ADC药物,该药物采用了新型结合和内吞机制,相较于传统单抗ADC展现出更为卓越的疗效,并能有效克服因单靶点表达下降导致的耐药性问题。临床前研究表明,DB-1419能够杀伤癌细胞并进行T细胞活化,在免疫重构模型中DB-1419展现出比单特异性B7-H3 ADC更强的肿瘤生长抑制活性。
2024年9月9日,映恩生物宣布双抗ADC新药DB-1419在晚期/转移性实体瘤中的 1/2a 期首次人体研究(NCT06554795),已获得美国食品和药物管理局(FDA)新药研究申请(IND)批准和澳大利亚药品管理局(TGA)临床试验通知(CTN),并顺利完成了全球首例受试者的给药。
关于抗体偶联药物
抗体偶联药物(ADC)是一种很有前途的癌症治疗新型疗法,通过将细胞毒性有效载荷靶向肿瘤细胞。在单克隆抗体与靶抗原结合时,ADC被内化到肿瘤细胞中。最终的接头分解会促进有效载荷的细胞内释放,并在细胞内发挥其破坏微管或DNA的作用,是目前肿瘤领域发展最快的药物之一。
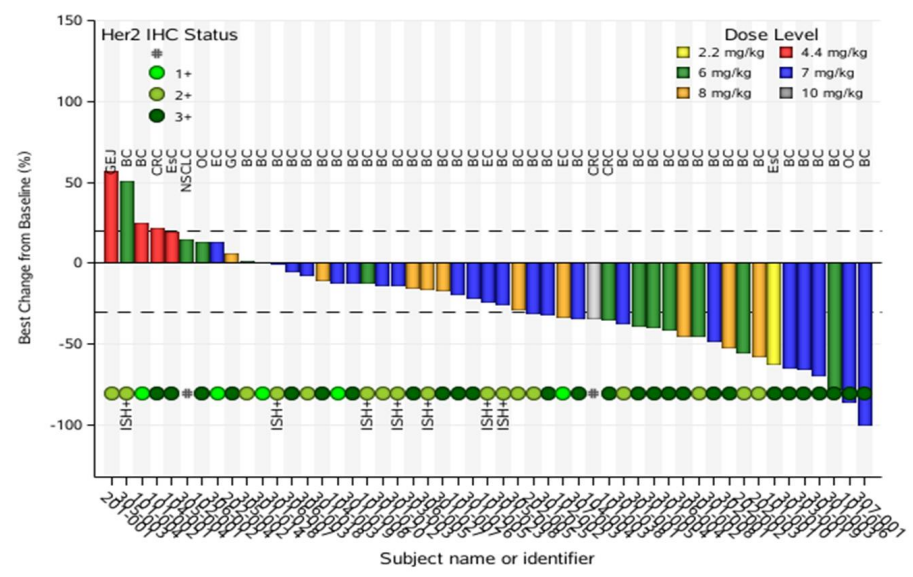
DB-1303(BNT323)是BioNTech和映恩生物合作开发的一款新一代靶向HER2的抗体偶联药物(ADC),2023年美国临床肿瘤学会(ASCO)上 BioNTech 报告了DB-1303在实体瘤中的I/2期(NCT05150691)临床数据。85例患者接受治疗,结果显示:
未确认的客观缓解率(ORR)为44.2%,疾病控制率(DCR)为88.5%,也就是46例患者疾病得到有效控制。26例HER2阳性乳腺癌患者中,50%的患者肿瘤缩小或消失,高达96.2%的患者病情得到控制。
2023年12月,DB-1303(BNT323)获得美国食品药品监督管理局(“FDA”)授予突破性疗法资格,用于治疗免疫检查点抑制剂治疗期间或治疗后进展的晚期子宫内膜癌患者。
在既往接受过大量治疗的晚期子宫内膜癌患者中,抗肿瘤活性令人鼓舞,未经证实的客观缓解率为 58.8%,未经证实的疾病控制率为 94.1%。
2024年11月27日,国家药品监督管理局药品审评中心(CDE)显示批准DB-1303(BNT323)治疗HER2低表达、激素受体阳性转移性乳腺癌的临床试验申请。
目前ADC药物正在进行临床试验,目前在积极寻找患者中,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可致电至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://investors.biontech.de/system/files-encrypted/nasdaq_kms/assets/2023/06/04/21-42-12/ASCO%202023_BNTX%20data_external%20slide%20deck.pdf
2.https://investors.biontech.de/news-releases/news-release-details/biontech-and-dualitybio-receive-fda-breakthrough-therapy












