1月26日,国家药品监督管理局药品审评中心(CDE)显示:明济生物M108单抗注射液拟纳入突破性治疗,拟定适应症为联合吉西他滨+白蛋白结合型紫杉醇,用于局灶晚期不可切除或转移性的CLDN18.2阳性的胰腺癌患者的一线治疗。
FG-M108是明济生物自主研发的靶向CLDN18.2的ADCC增强型单克隆抗体,以适中亲和力高特异性的靶向CLDN18.2阳性肿瘤细胞,并通过增强的ADCC效应等充分调动患者机体的免疫功能来杀伤肿瘤。
2025年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)上明济生物发布了FG-M108的最新临床试验数据。
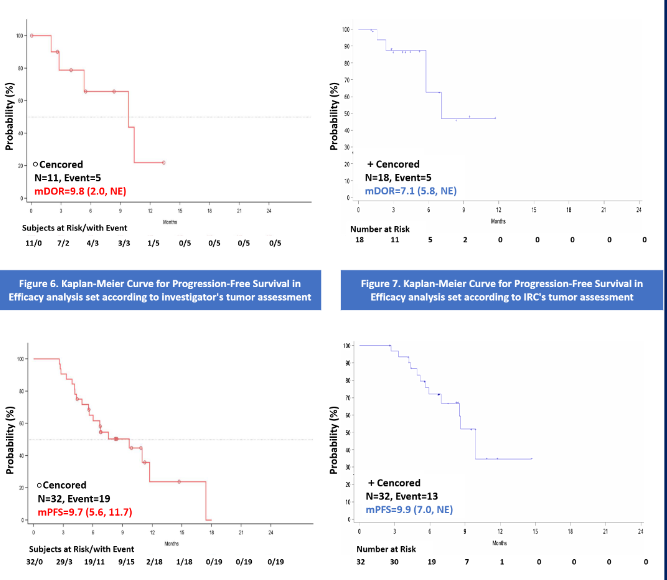
FG-M108联合白蛋白紫杉醇和吉西他滨(AG)治疗一线局灶晚期不可切除或者转移性胰腺癌(PC)的最新临床试验结果显示:入组的39例晚期胰腺癌患者,32例胰腺癌患者有可测量病灶且至少进行过一次治疗后肿瘤评估,ORR,DCR分别为34.4%及100%;更重要的是胰腺癌患者获得了长期的生存获益,其中mPFS为9.7月,mDoR为9.8月;独立影像评估(IRC)的临床疗效与研究者评估,疗效几乎一致,其中ORR,DCR分别为53.1%和100%;mPFS为9.9月; mDoR为7.1月。
FG-M108在多种CLDN18.2阳性肿瘤中具有成药潜力,单药及联药治疗晚期实体瘤的前期临床数据已显示出了良好的安全性和积极的疗效信号。
2025年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)上公布了FG-M108联合卡培他滨和奥沙利铂(CAPOX)一线治疗局灶晚期不可切除或者转移性胃/胃食管交界部(G/GEJ)腺癌的最新临床试验结果。
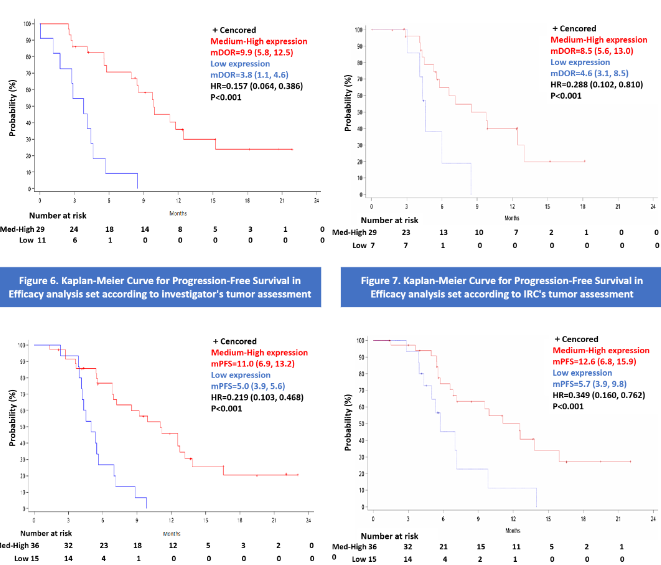
入组了52名患有HER2-/CLDN18.2+(IHC 1+/2+/3+≥10%)晚期或转移性G/GEJ 腺癌患者,51例可评估受试者中,中高表达受试者中1例实现了临床完全缓解(cCR),27例实现了完全病理缓解(CPR),ORR为81%,DCR为97%,mDOR为9.9月,mPFS为11.0月,mOS为20.3月;15例受试者属于CLDN18.2低表达的患者(≥10%的肿瘤细胞膜染色强度为1+及以上且<40%的肿瘤细胞膜染色强度为2+及以上),低表达受试者的ORR为66.7%, DCR为100%,mPFS为5.0月,mDOR为3.9月。低表达的疗效数据与CAPOX化疗的历史疗效数据基本一致。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://cloud.madeinidea-china.com/web/pdf/index.html?file=https://jw-ppt.oss-cn-beijing.aliyuncs.com/liu/futuregenbiopharm/ASCO%20GI%202025-Poster%23729.pdf
2.https://cloud.madeinidea-china.com/web/pdf/index.html?file=https://jw-ppt.oss-cn-beijing.aliyuncs.com/liu/futuregenbiopharm/ASCO%20GI%202025-Poster%23431.pdf

相关推荐
随便看看
- “不完美心动”——干细胞叫嚣“心衰”
- 德曲妥珠单抗获得美国FDA上市申请优先审评资格,用于HER2低表达或超低表达转移性乳腺癌
- 欧狄沃再添可切除肺癌新适应症
- IBI363获快速通道资格拟用于治疗黑色素瘤
- 艾力斯医药的AST2303片获批临床,用于治疗EGFR突变的晚期非小细胞肺癌
- 全球首个获批用于治疗鼻咽癌的PD-L1单抗(塔戈利单抗)上市
- 第四代EGFR抑制剂:BI-4020
- HL-085联合维莫非尼的治疗方案为BRAF V600E突变的实体瘤患者带来曙光
- 泽璟制药自主研发的新药Alveltamig、Nilvanstomig的临床研究数据及最新进展亮相2025 ESMO
- 塞普替尼(Retevmo,Selpercatinib)治疗 RET 融合阳性非小细胞肺癌的I/II 期LIBRETTO-001试验最新结果











