10月30日,第一三共和阿斯利康联合开发的德曲妥珠单抗(Trastuzumab Deruxtecan,优赫得,DS-8201,Enhertu,T-Dxd)补充生物制品许可申请(sBLA)已被美国FDA受理,并被授予优先审评资格,用于转移阶段接受过至少一种内分泌治疗、不可切除或转移性、HER2低表达(IHC 1+或IHC 2+/ISH-)或HER2超低表达(IHC 0伴膜染色)乳腺癌成人患者。
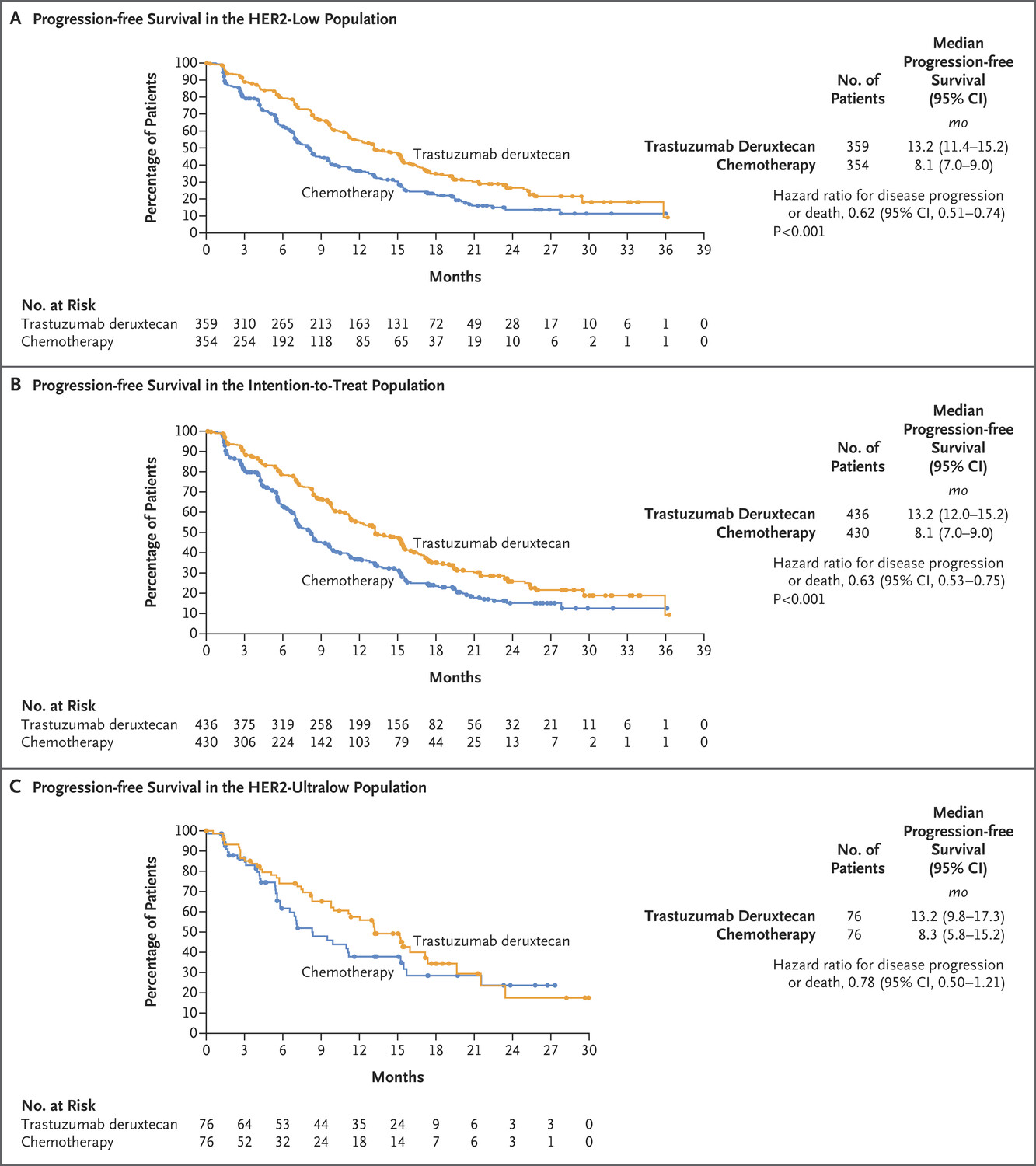
在III期DESTINY-Breast06研究(NCT04494425)中,化疗相比,德曲妥珠单抗可将疾病进展或死亡风险降低37%,德曲妥珠单抗与化疗的中位无进展生存期(PFS)分别是13.2个月和8.1个月。
在对HR阳性、HER2低表达转移性乳腺癌患者中,德曲妥珠单抗治疗组的中位PFS是13.2个月,化疗组的中位PFS是8.1个月。
在HER2超低表达患者中,德曲妥珠单抗治疗组和化疗组的中位PFS分别是13.2个月和8.3个月。
HER2低表达转移性乳腺癌患者中,德曲妥珠单抗治疗组的客观缓解率(ORR)为56.5%,其中9例患者完全缓解(CR),中位反应持续时间为14.1个月,化疗组客观缓解率(ORR)为32.2%,中位反应持续时间为8.6个月。总生存率(OS)分别为37.9%和41.2%,12个月总生存率分别为87.6%和81.7%。
HER2超低表达患者中,德曲妥珠单抗治疗组的客观缓解率(ORR)为61.8%,化疗组客观缓解率(ORR)为26.3%。
该试验中,德曲妥珠单抗可显著延长乳腺癌患者无进展生存期。
德曲妥珠单抗是一款采用独有技术设计的靶向HER2的DXd ADC,目前正在全国范围内寻找HER2过表达的实体瘤患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以联系康和源免疫之家医学部(400-880-3716)。
部分入选标准:
1.年龄至少18岁;
2.晚期实体瘤患者;
3.ECOG体能状态评分为0~1。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可致电至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.nejm.org/doi/full/10.1056/NEJMoa2407086












