10月8日,亚盛医药宣布国家药品监督管理局药品审评中心(CDE)批准APG-2449的临床试验申请,用于针对二代间变性淋巴瘤激酶(ALK)TKI耐药或不耐受的非小细胞肺癌(NSCLC)患者,或初治ALK阳性晚期或局部晚期NSCLC患者的两项注册III期临床研究。
APG-2449是亚盛医药自主研发、具有口服活性的小分子FAK抑制剂,是ALK/ROS1多靶点抑制剂,也是国内首个获CDE许可进行临床试验的FAK抑制剂。
2024年美国临床肿瘤学会(ASCO)年会上公布了APG-2449在非小细胞肺癌(NSCLC)患者中的最新数据。结果显示:
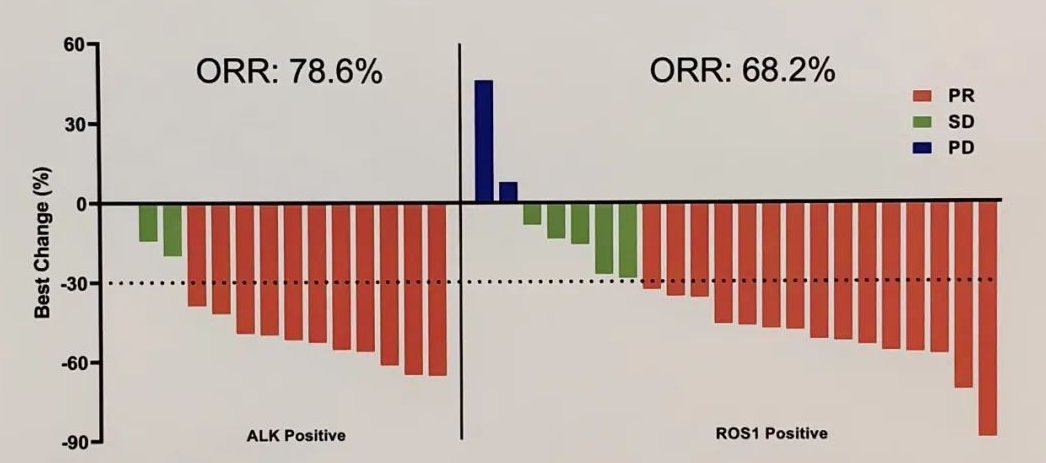
在22例没有接受过酪氨酸激酶抑制剂(TKI)治疗的ROS1阳性非小细胞肺癌患者中,客观缓解率(ORR)为 68.2%,也就是说有15例患者出现不同程度的肿瘤缓解。
14例没有接受过酪氨酸激酶抑制剂(TKI)治疗的ALK阳性非小细胞肺癌患者中,客观缓解率(ORR)为78.6%,11例患者出现不同程度的肿瘤反应。
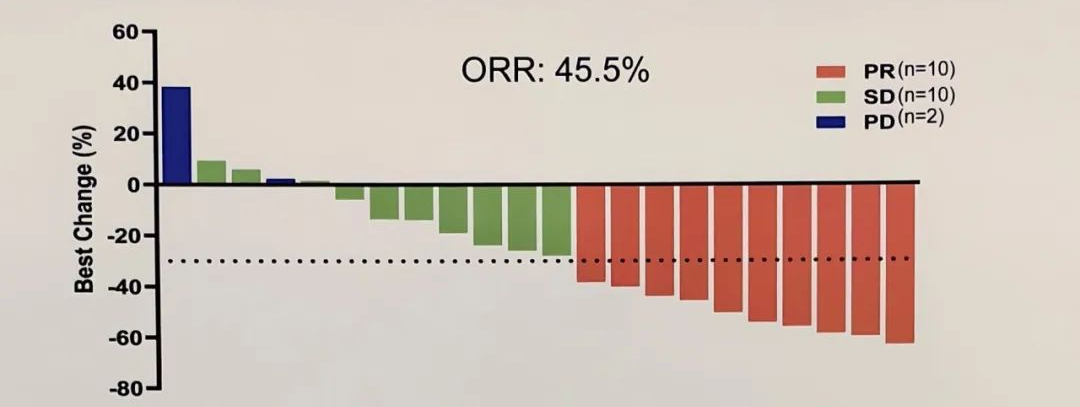
在2代 ALK TKI治疗耐药且无可靶向旁路基因突变(例如 KRAS G12C突变、BRAF V600E突变)的22 例NSCLC患者中,10例患者实现部分缓解(PR)。
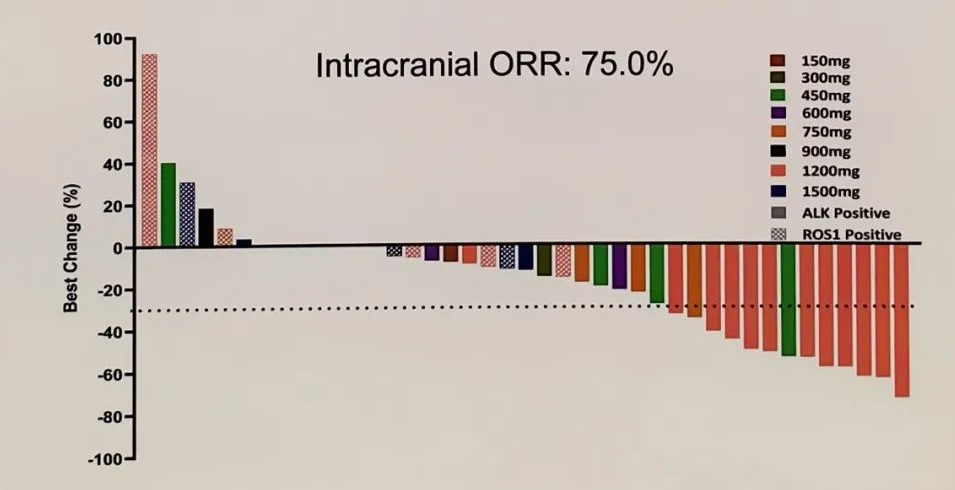
在接受RP2D治疗的患者中,12例患者基线有脑转移,其中9例达到颅内病灶PR,其ORR 为 75.0%。
共有 129 例 (89.6%) 患者出现治疗相关不良事件 (TRAEs),最常见TRAE(≥10%)包括血清肌酐升高(49.3%)、丙氨酸转氨酶升高(42.4%)、天冬氨酸转氨酶升高(36.1%)、恶心(28.5%)、呕吐(23.6%)、 腹泻(22.9%)和白细胞计数减少(22.2%),中性粒细胞减少 (17.4%)和皮疹(13.2%)。共有20 例患者 (13.9%) 出现≥ 3 级TRAEs。
该试验表明,APG-2449在未经TKI治疗或2代 ALK TKI耐药的NSCLC患者中都显示了初步疗效,对脑转移病灶亦有初步抑制作用。
目前有临床试验正在寻找非小细胞肺癌患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.3124#:~:text=APG-2449%20is%20well%20tolerated%20at%20the%20recommended%20phase%202%20dose












