12月6日,国家药品监督管理局药品审评中心(CDE)显示:MET抑制剂伯瑞替尼肠溶胶囊(PLB-1001)拟纳入优先审评,拟定适应症为用于治疗具有间质-上皮转化因子(MET)扩增的局部晚期或转移性非小细胞肺癌患者。

在非小细胞肺癌(NSCLC)中MET异常包括MET 14跳突、MET基因扩增、MET基因点突变、MET 基因融合及 MET 蛋白过表达等。MET不同类型异常形式的发生率及其临床意义存在差异,需要精准识别。原发MET基因扩增作为NSCLC驱动基因之一,其发生率为1%~5%1,为明确的靶向治疗标志物。目前国内对于MET扩增尚无治疗推荐,多参考无驱动基因治疗方案,疗效不佳,难以满足临床诊疗需求。
伯瑞替尼作为我国自主研发的1类新药,是一种高选择性的c-MET抑制剂,于2023年11月16日获批用于治疗具有间质-上皮转化因子(MET)外显子 14 跳变的局部晚期或转移性非小细胞肺癌患者。2024年4月23日获批用于既往治疗失败的具有 PTPRZ1-MET 融合基因的 IDH 突变型星形细胞瘤(WHO 4级)或有低级别病史的胶质母细胞瘤成人患者。2024年11月28日,MET抑制剂万比锐®(伯瑞替尼肠溶胶囊)成功纳入医保。
2024年7月27日,国际权威期刊Journal of Clinical Oncology发表了由广东省人民医院吴一龙教授团队牵头开展的伯瑞替尼用于MET异常晚期非小细胞肺癌(NSCLC)的多中心、多队列、开放标签Ⅱ期临床研究(KUNPENG研究)。
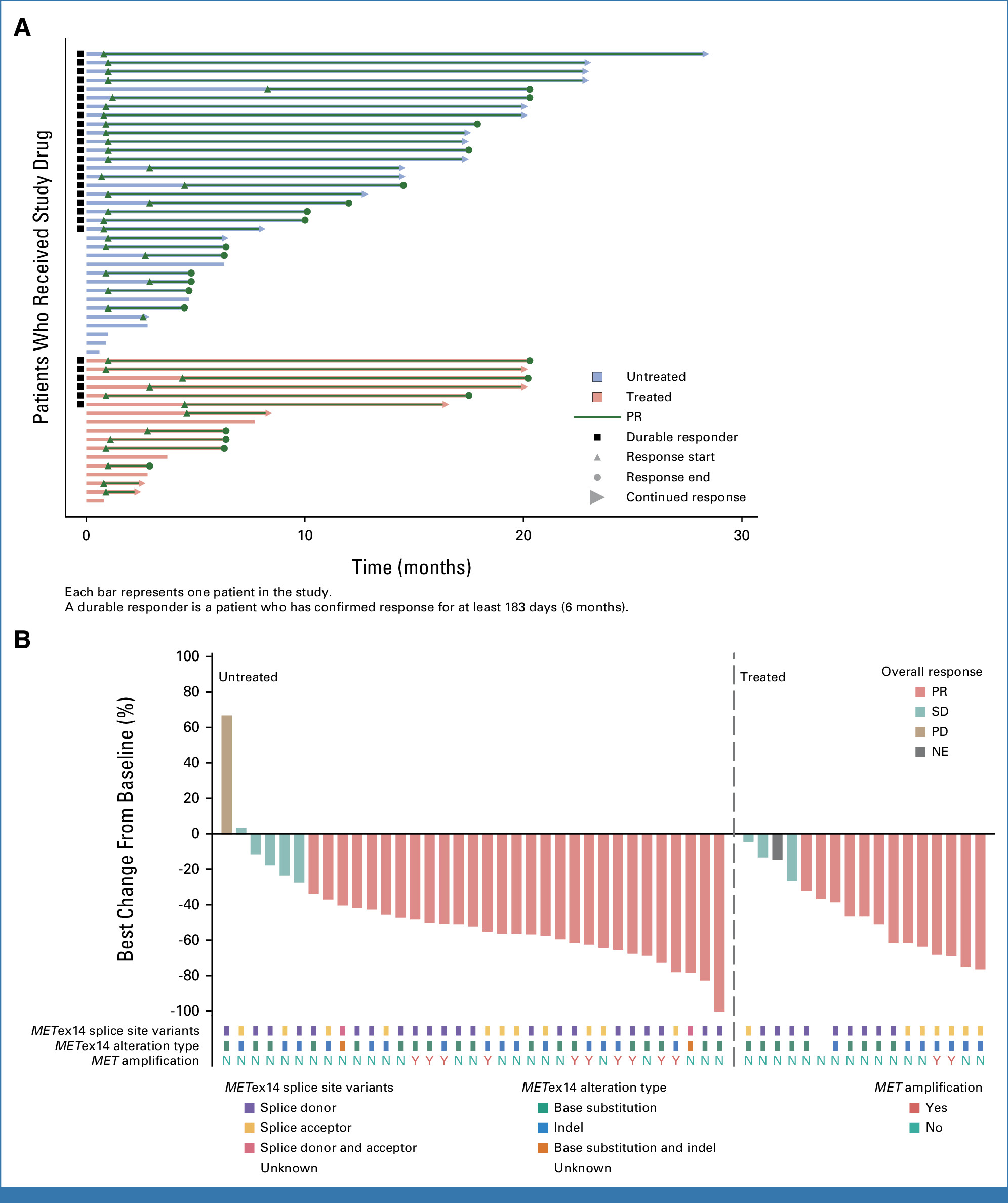
113例患者纳入研究,52例患者进行疗效分析,结果显示:39例患者肿瘤缩小或消失,客观缓解率(ORR)为75%,中位缓解持续时间(DOR)为15.9 个月,疾病控制率(DCR)为96.2%。
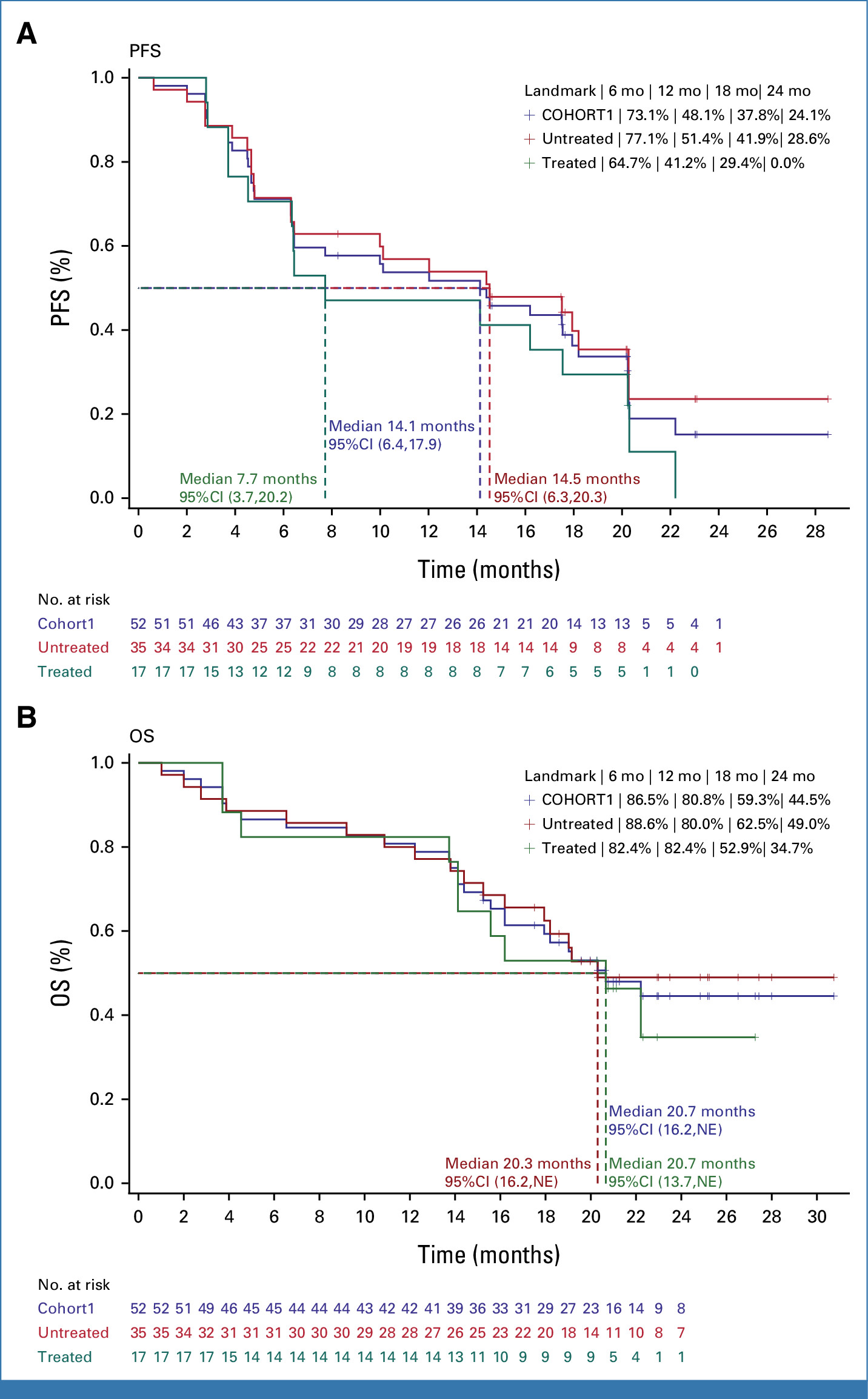
中位无进展生存期(PFS)为14.1 个月,中位总生存期(OS)为 20.7 个月,6 、 12 、 18 和 24 个月的生存率分别为 86.5% 、 80.8% 、 59.3% 和 44.5%。
目前有临床试验正在寻找患者,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
参考资料
https://ascopubs.org/doi/10.1200/JCO.23.02363

相关推荐
随便看看
- HER2靶向ADC药物SHR-A1811研究亮相,DS-8201拳击乳腺癌、肺癌、结直肠癌、胃癌等
- 恒瑞医药HRS-5041联合疗法获批临床用于前列腺癌
- 艾沙妥昔单抗获批多发性骨髓瘤
- 新一代ALK/ROS1激酶抑制剂伊鲁阿克片在ALK阳性非小细胞肺癌患者中的最新数据公布
- 科伦博泰ADC药物博度曲妥珠单抗新药申请获受理
- FDA 批准度伐利尤单抗用于治疗肌层浸润性膀胱癌
- 阿昔替尼获批肾细胞癌
- Cantargia 宣布 Nadunolimab 治疗晚期三阴性乳腺癌 (TNBC) 的 2 期 TRIFOUR 试验的初步顶线疗效结果
- 欧盟委员会批准orspono用于治疗滤泡性淋巴瘤和弥漫性大B细胞淋巴瘤
- 他泽司他获批上市,用于EZH2突变阳性滤泡性淋巴瘤











