2025年3月28日,美国食品药品监督管理局(FDA)批准度伐利尤单抗(durvalumab)联合吉西他滨和顺铂作为新辅助治疗,随后将单药 durvalumab 作为根治性膀胱切除术后的辅助治疗,用于肌层浸润性膀胱癌(MIBC)成人患者。

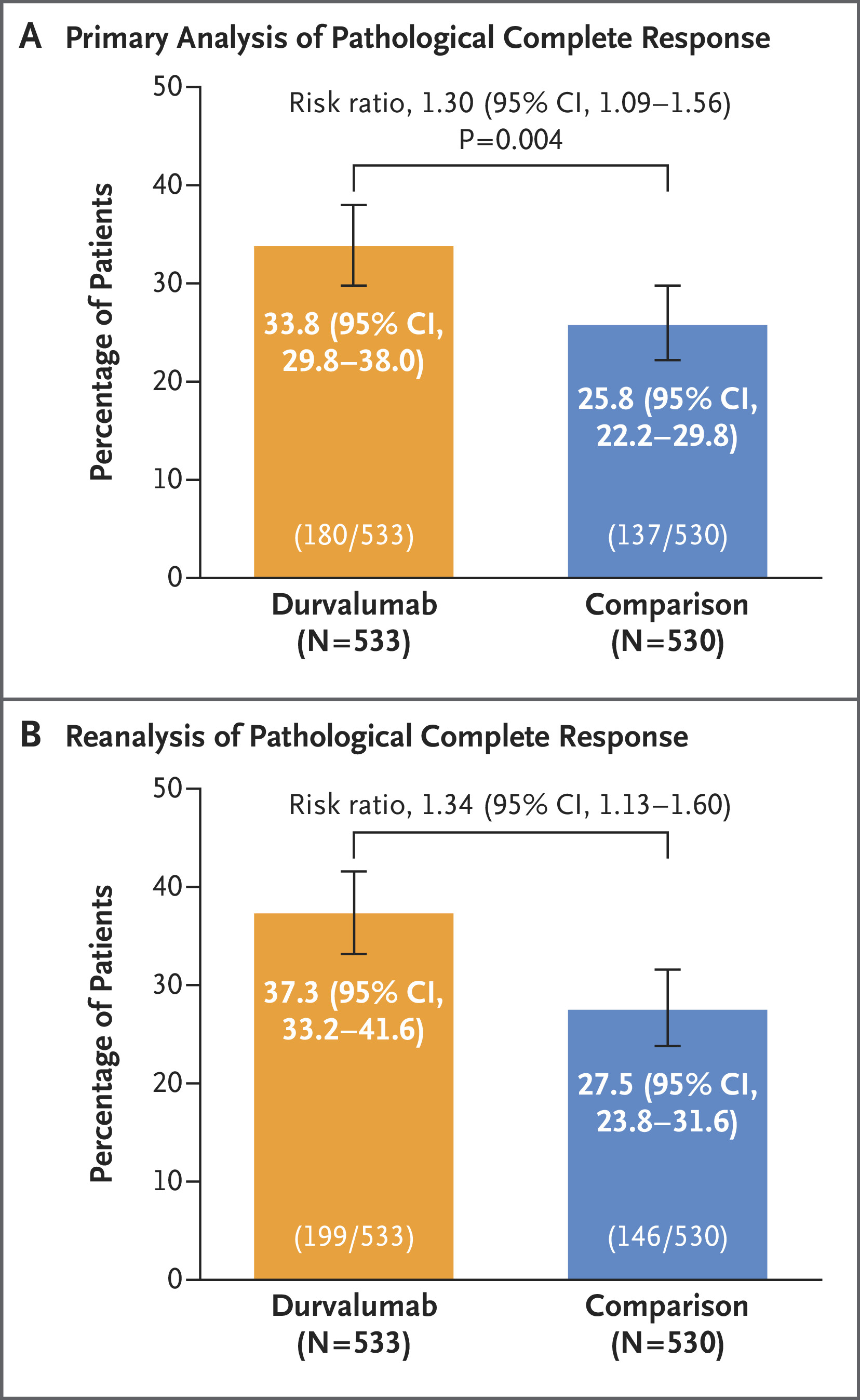
1063名患者接受了随机分组,其中 533 名被分配到 durvalumab 组,530 名被分配到对照组。结果显示:度伐利尤单抗组 33.8%的患者出现病理完全缓解,对照组为25.8%。
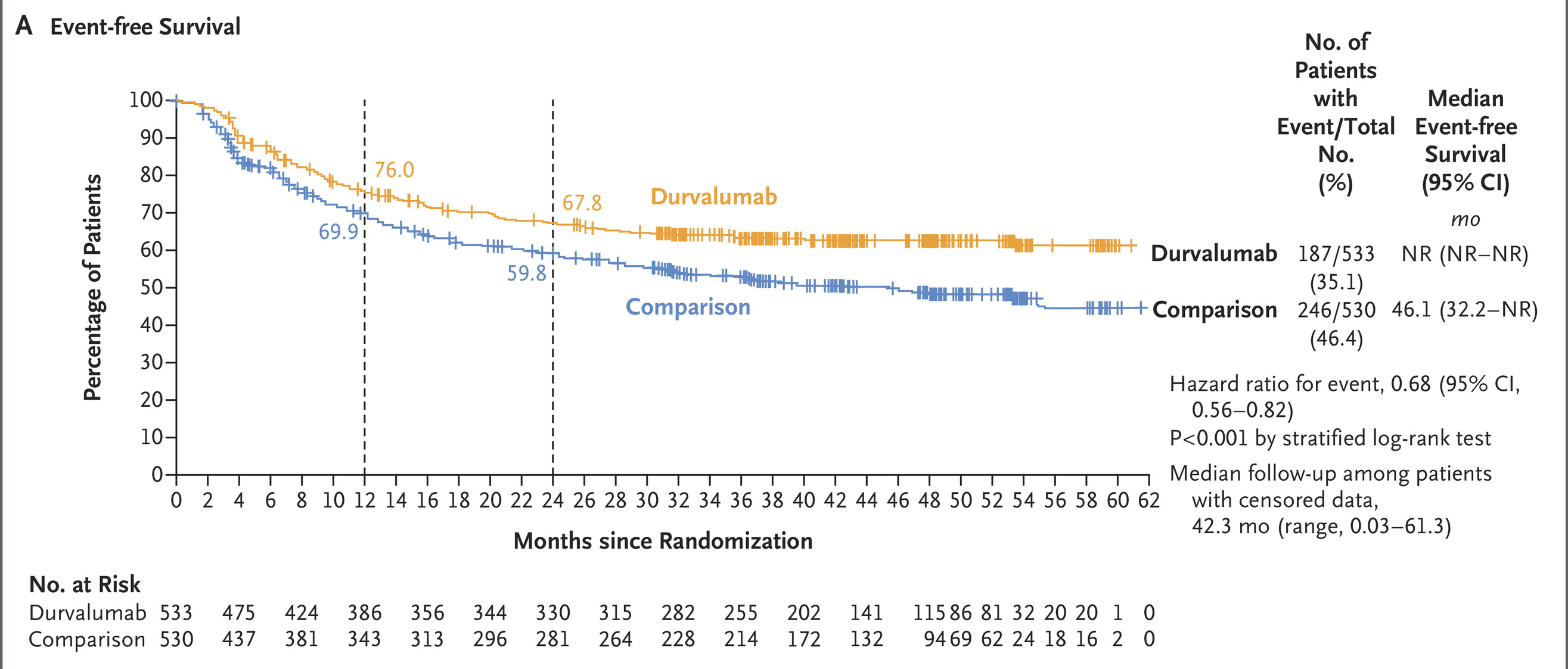
durvalumab 未达到无事件生存,化疗组为46.1个月。中位度伐利尤单抗组估计 24 个月无事件生存率为 67.8%,对照组为59.8%。
度伐利尤单抗组 24 个月时的估计总生存期为 82.2%,对照组为75.2%。
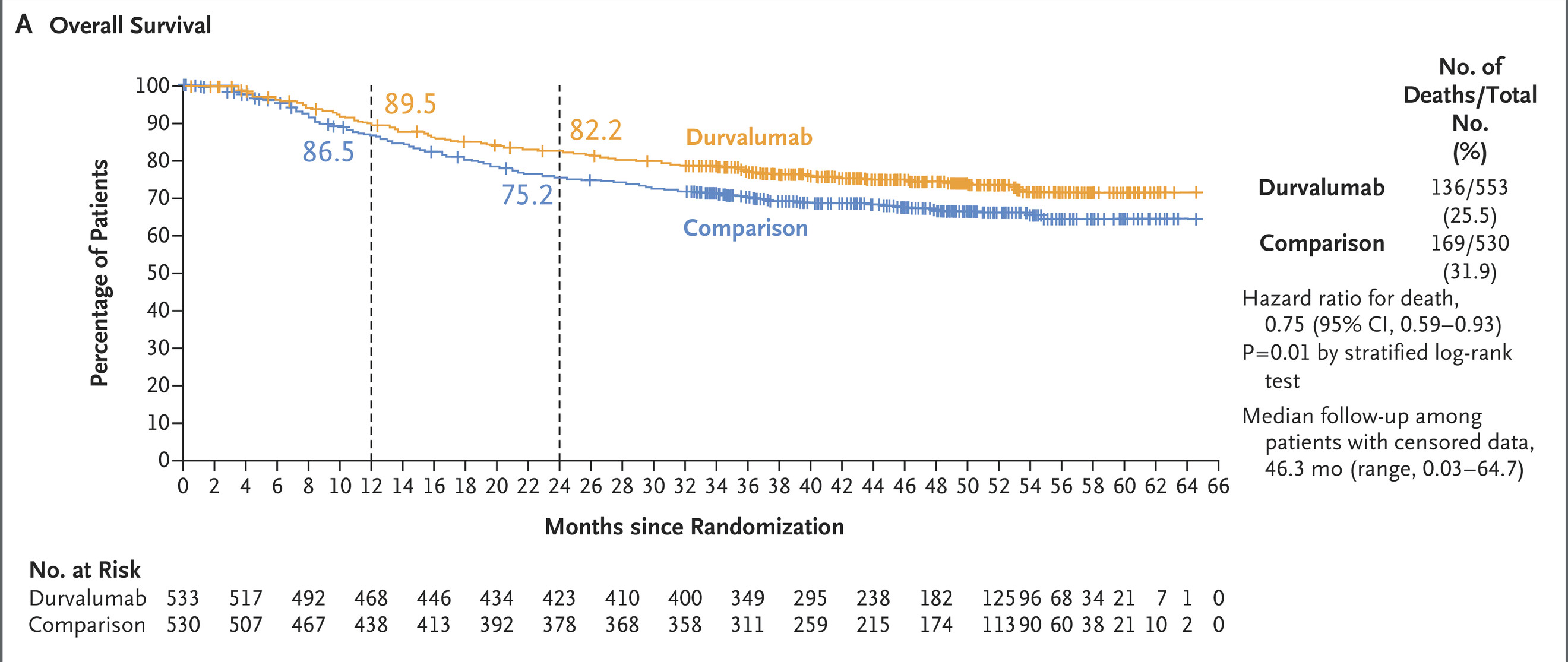
与单独使用新辅助化疗相比,围手术期 durvalumab 联合新辅助化疗导致无事件生存期和总生存期显著改善。
度伐利尤单抗是一种人源化的PD-L1单克隆抗体,能够阻断PD-L1与PD-1和CD80的结合,从而阻断肿瘤免疫逃逸并解除对免疫反应的抑制,重新激发T细胞识别杀伤肿瘤细胞,从而抑制肿瘤生长。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-durvalumab-muscle-invasive-bladder-cancer
2.https://www.nejm.org/doi/full/10.1056/NEJMoa2408154

相关推荐
随便看看
- 5周脑转移灶完全消退!第四代ALK抑制剂NVL-655获美FDA突破性疗法认定!客观缓解率达71%!
- ADC药物瑞康曲妥珠单抗联合治疗方案获美国FDA授予孤儿药资格认定
- 翰森制药阿美替尼联合化疗一线治疗EGFR突变晚期非小细胞肺癌患者的 III期AENEAS2研究达主要终点
- ADC药物ESG401治疗晚期HER2阴性乳腺癌患者脑转移的临床研究成果登上国际知名期刊
- 恩沃利单抗联合疗法在微卫星稳定/错配修复功能正常(MSS/pMMR)的结直肠癌患者中显示出积极效果
- IBI343治疗晚期胃或胃食管交界处腺癌(G/GEJ AC)的最新I期研究数据公布
- FDA 批准纳武利尤单抗联合伊匹木单抗治疗微卫星高度不稳定性(MSI-H)或错配修复缺陷(dMMR)结直肠癌
- ADC药物JSKN003临床试验申请获得美国FDA批准
- BRAF酶抑制剂备受关注---达拉非尼
- 新型BTK抑制剂奥布替尼和坦昔妥单抗的多项研究数据亮相2025 ESMO











