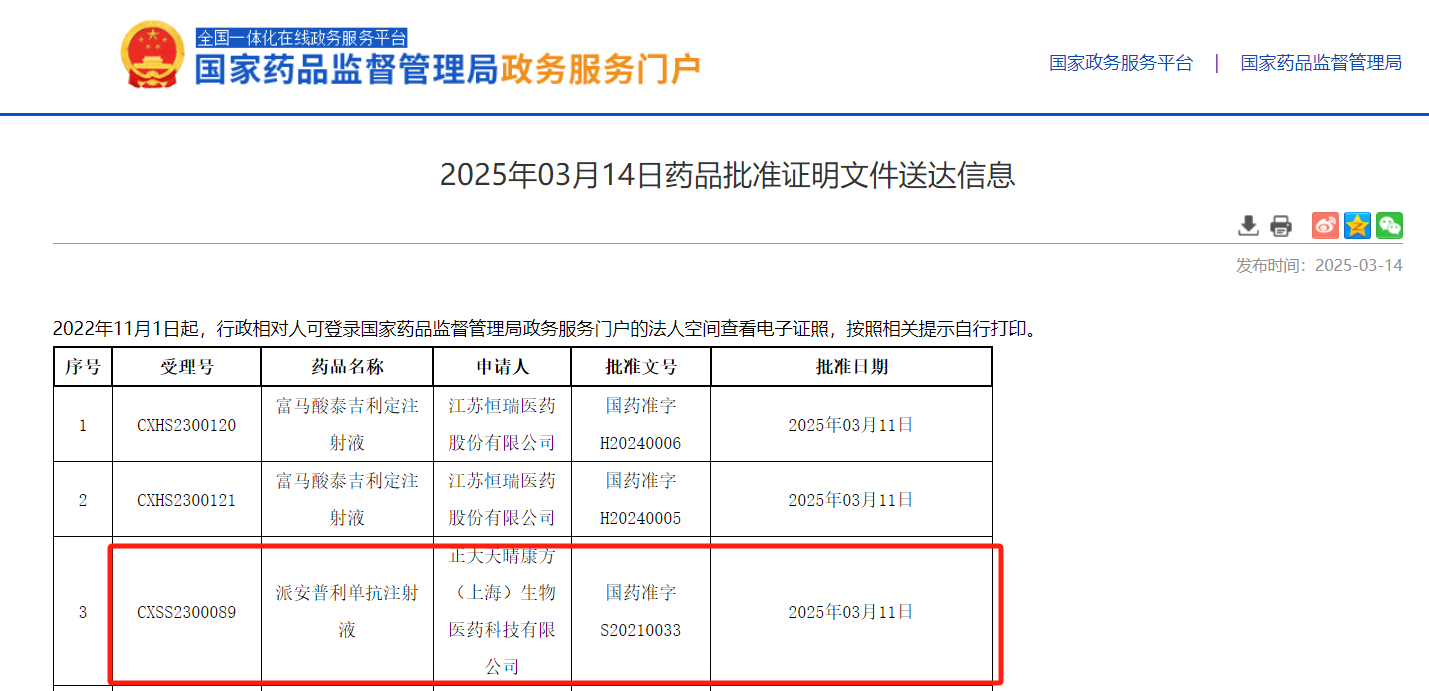
近日,国家药品监督管理局(NMPA)批准PD-1单抗药物派安普利单抗(商品名:安尼可)联合化疗一线治疗复发或转移性鼻咽癌(NPC)的新适应症。这是派安普利单抗的第4项适应症。
安尼可®是目前唯一采用 IgG1 亚型并进行Fc段改造的新型差异化PD-1 单抗,能够更有效增强免疫治疗疗效,且减少不良反应。
目前,安尼可®联合化疗一线治疗局部晚期或转移性鳞状非小细胞肺癌,安尼可®治疗至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤和安尼可®二线及以上治疗转移性鼻咽癌获批上市的适应症均已经获得批准,安尼可®联合方案一线治疗转移性鼻咽癌的上市申请已获得CDE和美国食品药品监督管理局(FDA)受理,单药用于三线及以上治疗转移性鼻咽癌的上市申请也获FDA受理。
2024年6月19日,《Signal Transductionand Targeted Therapy》发表了派安普利单抗治疗既往接受治疗的转移性鼻咽癌的II期研究结果。

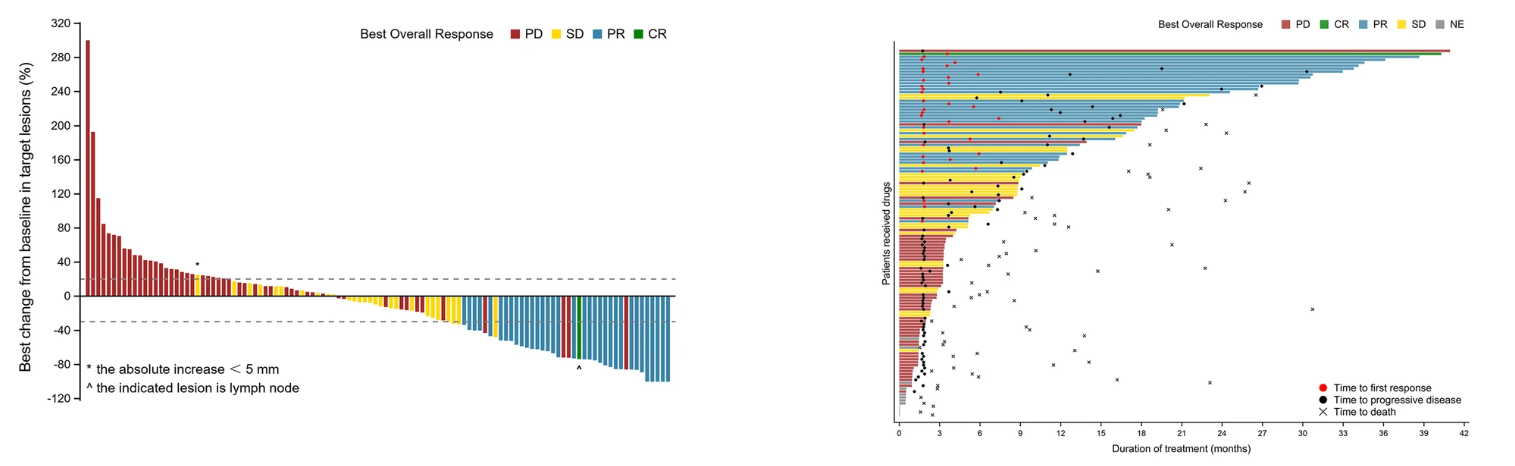
入组了 130 名患者,在根据IRRC的FAS中,1名患者达到完全缓解(CR),34名患者达到部分缓解(PR)。ORR为28.0%。中位反应时间为1.8个月,中位反应持续时间为14.8个月。在9个月时,66.8%的患者有反应。在数据截止时,10.4%的患者仍处于缓解期。此外,27名患者患有SD,51名患者患有PD。疾病控制率(DCR)为49.6%。
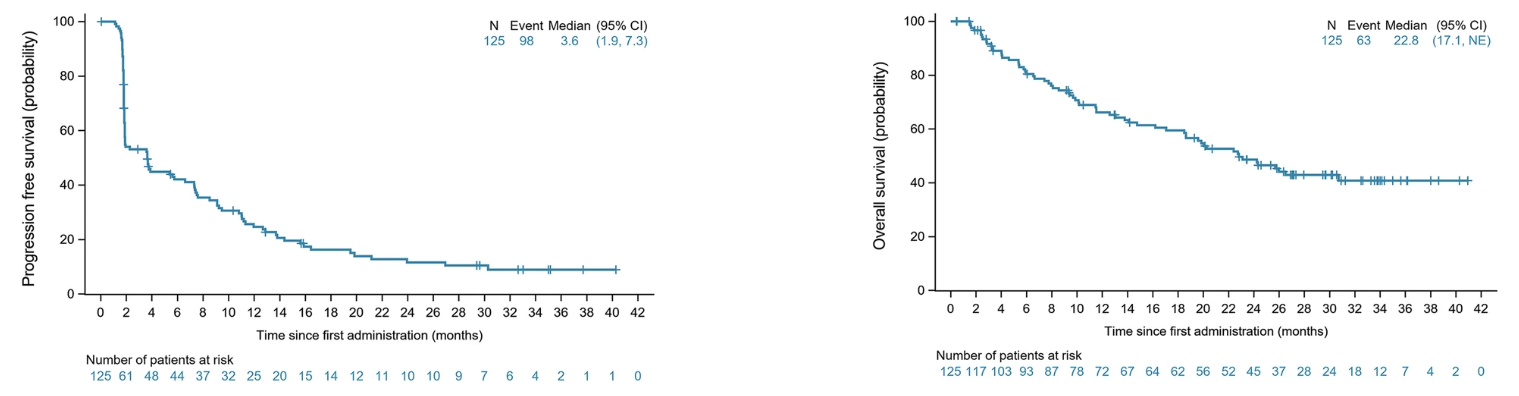
中位无进展生存时间为3.6个月。6个月和12个月的无进展生存率分别为42.1%和24.7%。中位OS为22.8个月。12个月和24个月OS率分别为66.1%和48.6%。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.nature.com/articles/s41392-024-01865-6

相关推荐
随便看看
- 新型BTK抑制剂奥布替尼和坦昔妥单抗的多项研究数据亮相2025 ESMO
- KRAS G12C抑制剂Glecirasib重创非小细胞肺癌、结直肠癌、胰腺癌等多种癌症!未来可期!
- JMKX001899片拟纳入突破性治疗
- SHR-A1921用于晚期小细胞肺癌(SCLC)的1期研究(NCT05154604)数据即将公布
- 劲方医药GFH375治疗KRAS G12D突变晚期实体瘤患者的I期临床数据亮相2025 ASCO
- IBI343治疗晚期胃或胃食管交界处腺癌(G/GEJ AC)的最新I期研究数据公布
- 度伐利尤单抗在美国获得可切除早期胃癌和胃食管交界处癌患者优先审评和突破性疗法认定
- 德曲妥珠单抗DESTINY-Breast05 Ⅲ期研究结果亮相2025 ESMO
- 芦康沙妥珠单抗第三项适应症获批上市
- Blenrep已获得欧盟批准,用于多发性骨髓瘤











