3月11日,罗氏宣布中国国家药品监督管理局(NMPA)批准了伊赫莱®(通用名:伊那利塞片)联合哌柏西利和氟维司群,适用于内分泌治疗耐药(包括在辅助内分泌治疗期间或之后出现复发)、PIK3CA突变、激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性乳腺癌成人患者。
这是中国首个获批的第三代高选择性PI3Kα抑制剂,凭借其独特的双重作用机制,填补了HR+/HER2-晚期乳腺癌患者精准治疗空白,为PIK3CA突变的HR+/HER2-乳腺癌患者带来精准、更高效能且安全性良好的治疗选择,助力患者实现更长生存。
伊那利塞是首个2通过高特异性选择和高效降解p110α亚基,实现对肿瘤信号通路的持续抑制。其联合CDK4/6抑制剂和内分泌治疗药物,同时抑制PI3K,CDK4/6和雌激素受体通路,通过协同作用加深应答并阻断耐药途径,联合作用机制为PIK3CA突变患者打开了一扇“生命之门”。
本次伊那利塞获批基于INAVO120研究,这是一项全球、多中心、双盲、随机对照的III期临床研究,旨在评估伊那利塞+哌柏西利+氟维司群在PIK3CA突变的HR+/HER2-局部晚期或转移性乳腺癌患者中一线治疗的疗效和安全性。
2024年10月,《新英格兰医学杂志》(New England Journal of Medicine)上发表了INAVO120数据。共纳入325例患者,其中 inavolisib 组 161 名患者,安慰剂组 164 名患者,结果显示:inavolisib 组 58.4% 的患者出现客观缓解,安慰剂组 25.0% 的患者出现客观缓解。中位缓解持续时间分别为 18.4 个月和 9.6 个月。
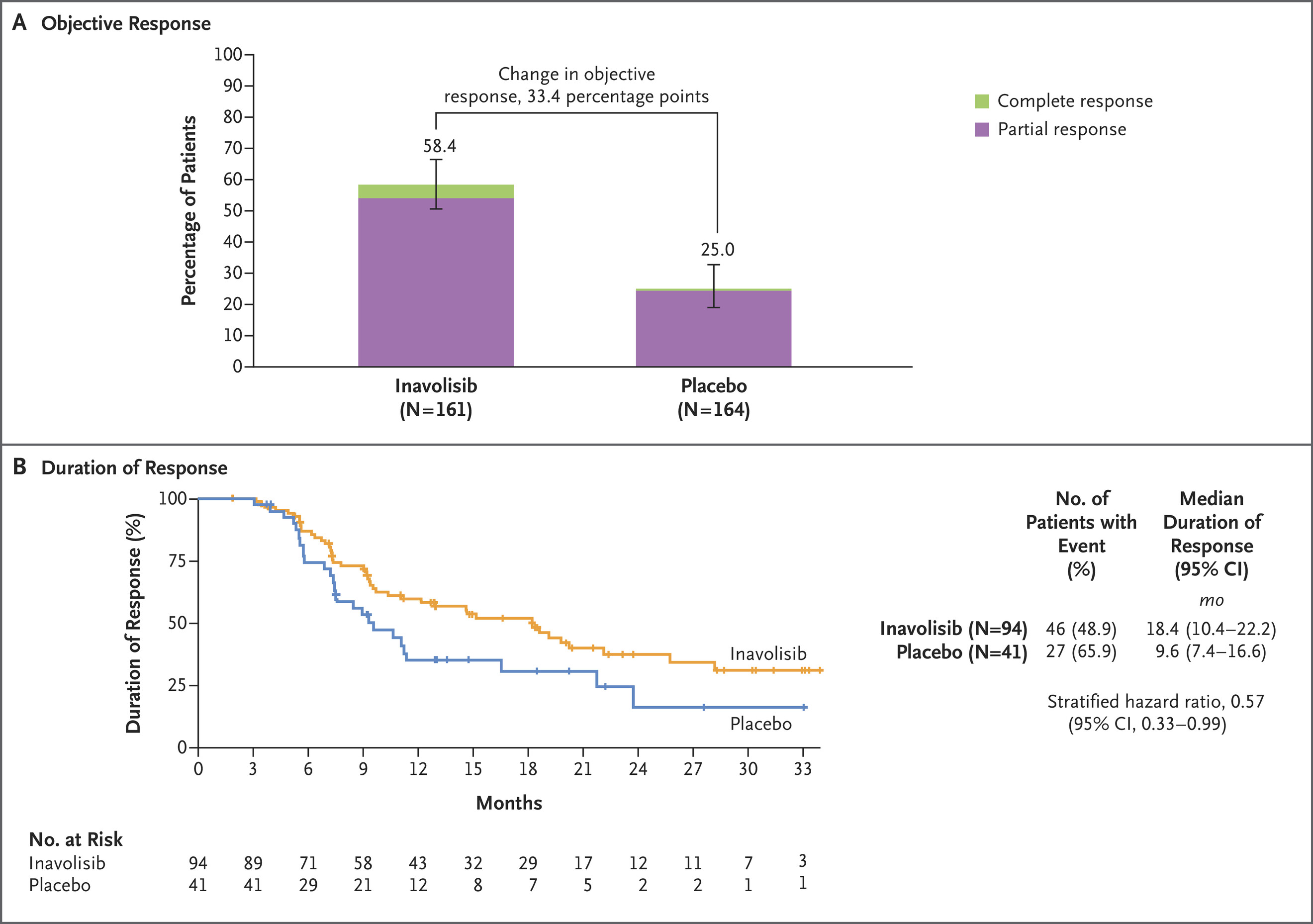
inavolisib 组中位无进展生存期为 15.0 个月,安慰剂组 为7.3 个月,navolisib 组 6 个月无进展生存概率为 82.9%,12 个月为 55.9%,18 个月为 46.2%,安慰剂组分别为 55.9%、32.6% 和 21.1%。
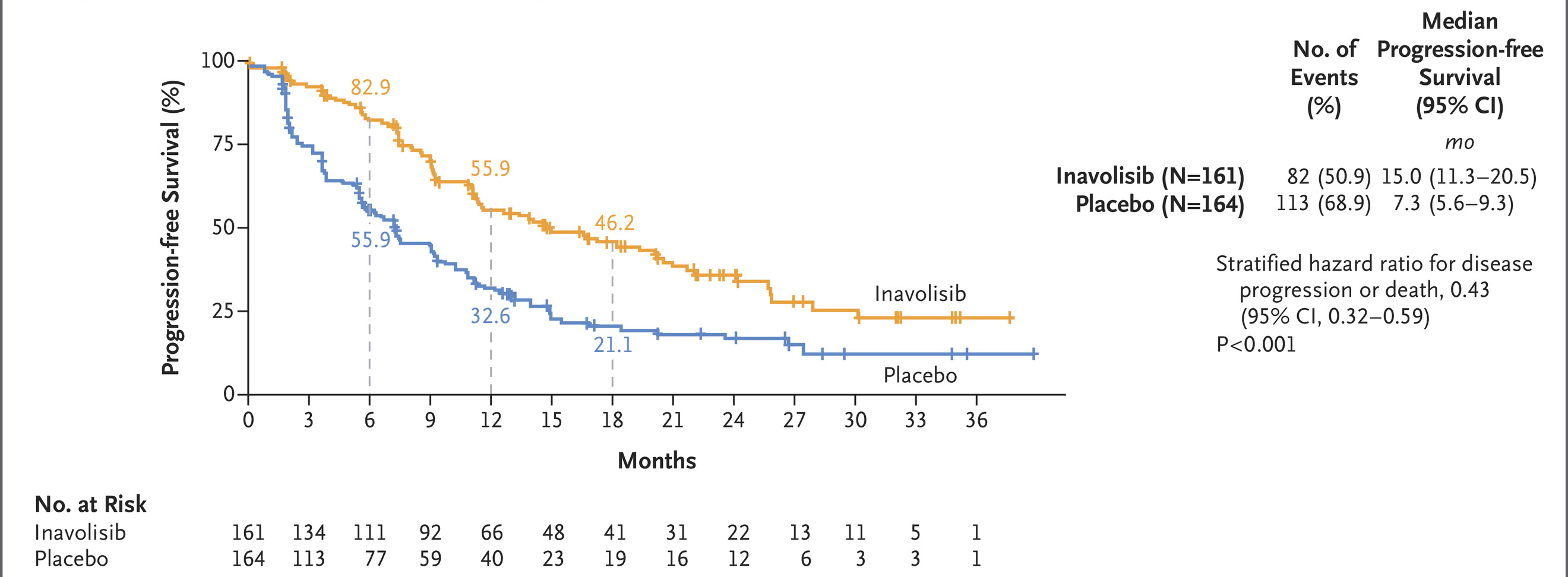
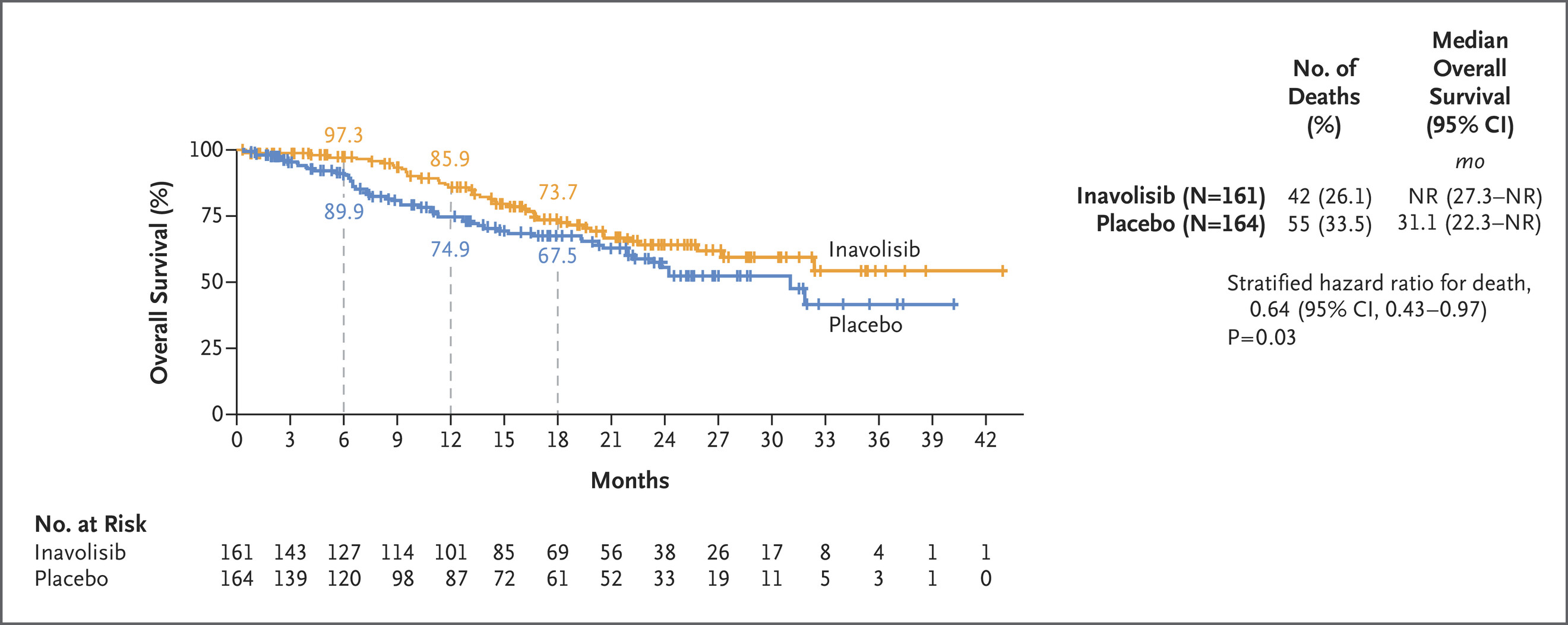
inavolisib 组 6 、 12 和 18 个月的生存概率分别为 97.3%、85.9% 和 73.7%,安慰剂组分别为 89.9%、74.9% 和 67.5%。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.nejm.org/doi/full/10.1056/NEJMoa2404625

相关推荐
随便看看
- 阿基仑赛注射液(Yescarta,奕凯达®,axicabtagene ciloleucel)
- HS-20093(B7-H3 ADC)用于复发或难治性肉瘤治疗的II期研究结果入选2025年欧洲肿瘤内科学会(ESMO)年会
- ADC药物SHR-A1921治疗铂耐药卵巢癌的首次人体I期研究数据亮相ESMO
- HLX07联合抗PD-1单抗H药(斯鲁利单抗)一线治疗EGFR高表达晚期鳞状非小细胞肺癌的II期研究更新数据公布
- 长期生存超过11年!第三代药出现耐药后怎么办?肺癌第4代靶向药震撼登场!
- ADC药物-YL201让晚期实体瘤患者“柳暗花明”,在多种癌症治疗中大放异彩
- 拜耳BAY 2927088治疗HER2突变非小细胞肺癌的数据结果亮相世界肺癌大会
- 6个月疾病控制率达79.5%!新一代广谱抗癌药Repotrectinib(瑞普替尼)有望于6月获批
- ADC药物芦康沙妥珠单抗用于EGFR突变非小细胞肺癌新适应症申请获受理
- 和誉医药宣布将在2025年ESMO GI 公布FGFR4抑制剂依帕戈替尼最新2期临床试验数据











