肝细胞癌(HCC)是全球最常见的癌症之一,它的死亡率在全球范围内呈上升趋势,2020年全球共有90.57万人诊断为肝癌,死亡患者达到83.02万。
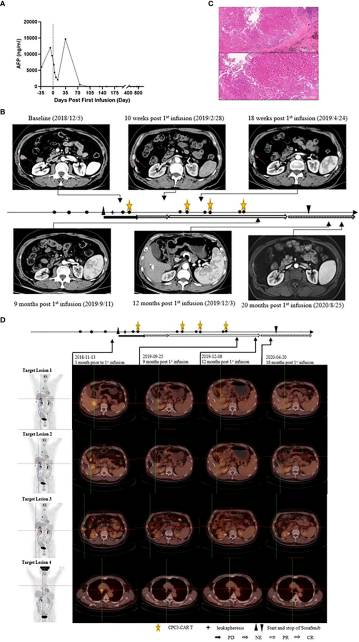
最后结果显示CT011联合索拉非尼治疗耐受性良好。患者从第3个月开始达到部分缓解(PR),并在第一个CT011输注周期后的第12个月达到完全缓解。肿瘤超过36个月没有进展,在第一次输注后保持完全缓解状态超过24个月。 项目名称:一项在GPC3阳性晚期肝细胞癌(HCC)受试者中评估Ori-C101的安全性、药代动力学和有效性的Ⅰb/Ⅱ期开放性、多中心临床研究