
8月13日,绿叶制药宣布mRNA治疗性疫苗LY01620的新药临床试验申请(IND)已获得国家药品监督管理局药品审评中心(CDE)批准,拟用于治疗HPV16相关的子宫颈高级别鳞状上皮内病变。

参考资料 1.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6439768/ 2.https://www.esmoiotech.org/article/S2590-0188(22)00198-8/fulltext 3.https://www.nature.com/articles/s41591-023-02612-0 4.https://s29.q4cdn.com/435878511/files/doc_events/2024/Jun/03/moderna-investor-oncology-event.pdf




相关推荐
随便看看
- 个性化癌症疫苗 EVX-01的 2 期试验的两年临床疗效数据即将亮相2025 ESMO
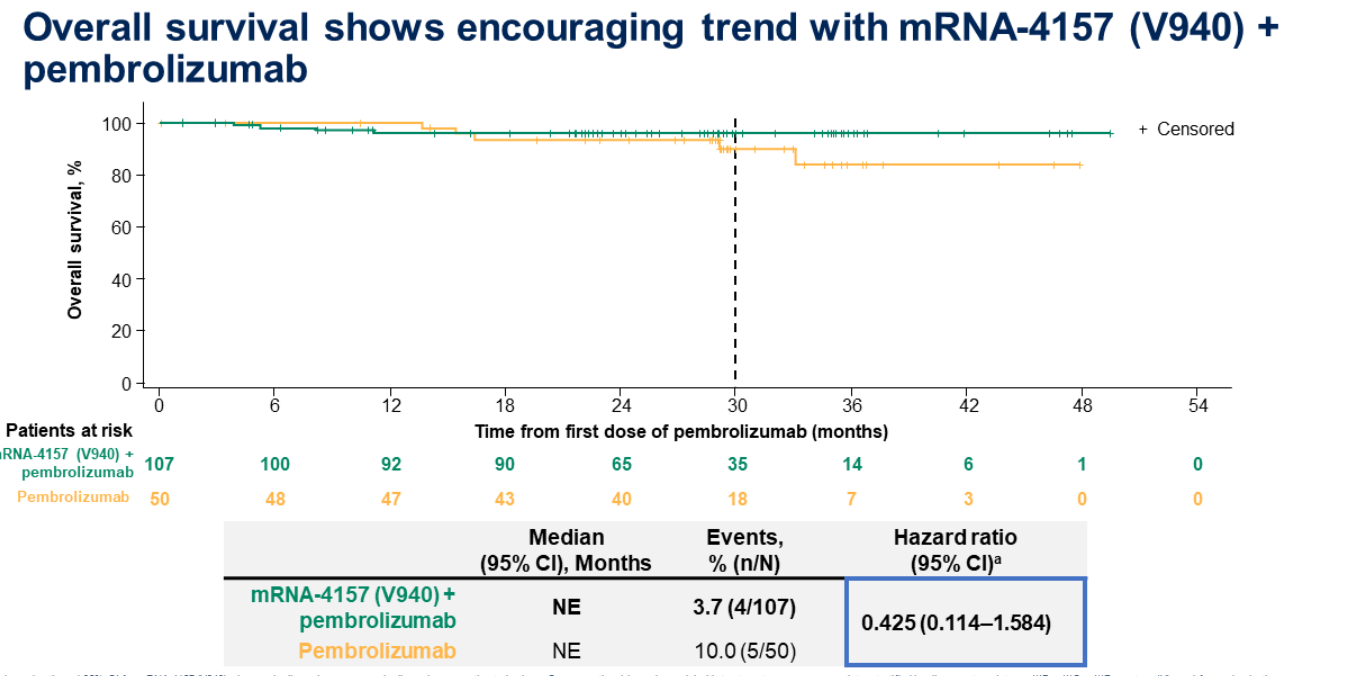
- mRNA疫苗加帕博利珠单抗在黑色素瘤中实现83%的缓解效果
- 个性化mRNA疫苗联合PD-1抑制剂治疗晚期食管鳞状细胞癌患者的病例
- 无进展生存期高达78.6%!国内首款自复制mRNA疫苗JCXH-211,癌症免疫治疗新时代的曙光
- 5年随访多名患者存活!癌症疫苗大放异彩,从“遥远梦想”到临床可能,开启癌症精准打击新篇章
- 肿瘤疫苗进入白热化阶段,突破晚期肺癌、胃癌治疗窘境!
- KSD-101注射液临床试验获得批准
- 2.5年生存率高达96.0%!癌症疫苗露锋芒:黑色素瘤、胃癌、胶质母细胞瘤、肺癌生存数据飙升
- 肿瘤消失25个月!新抗原癌症疫苗联合治疗方案对抗三大癌种
- 爆火!癌症疫苗“大杀四方”,或是胰腺癌、肺癌、头颈癌、间皮瘤、宫颈癌患者的“救命稻草”











