7月26日,皮尔法伯实验室宣布,欧洲药品管理局人用药品委员会 (CHMP) 通过了一项建议批准 BRAFTOVI®(康奈非尼)联合 MEKTOVI®(比美替尼)用于BRAF V600E突变晚期非小细胞肺癌 (NSCLC) 成人患者的对症治疗肯定意见。该肯定意见将提交至欧盟委员会 (EC) 审查,预计于今年晚些时候决定是否批准关于欧盟药品上市许可(MA) 的申请。

在PHAROS II 期研究中,康奈非尼(Encorafenib)联合比美替尼(Binimetinib)在从未接受治疗的患者 (n = 59) 中客观缓解率(ORR)实现75%。
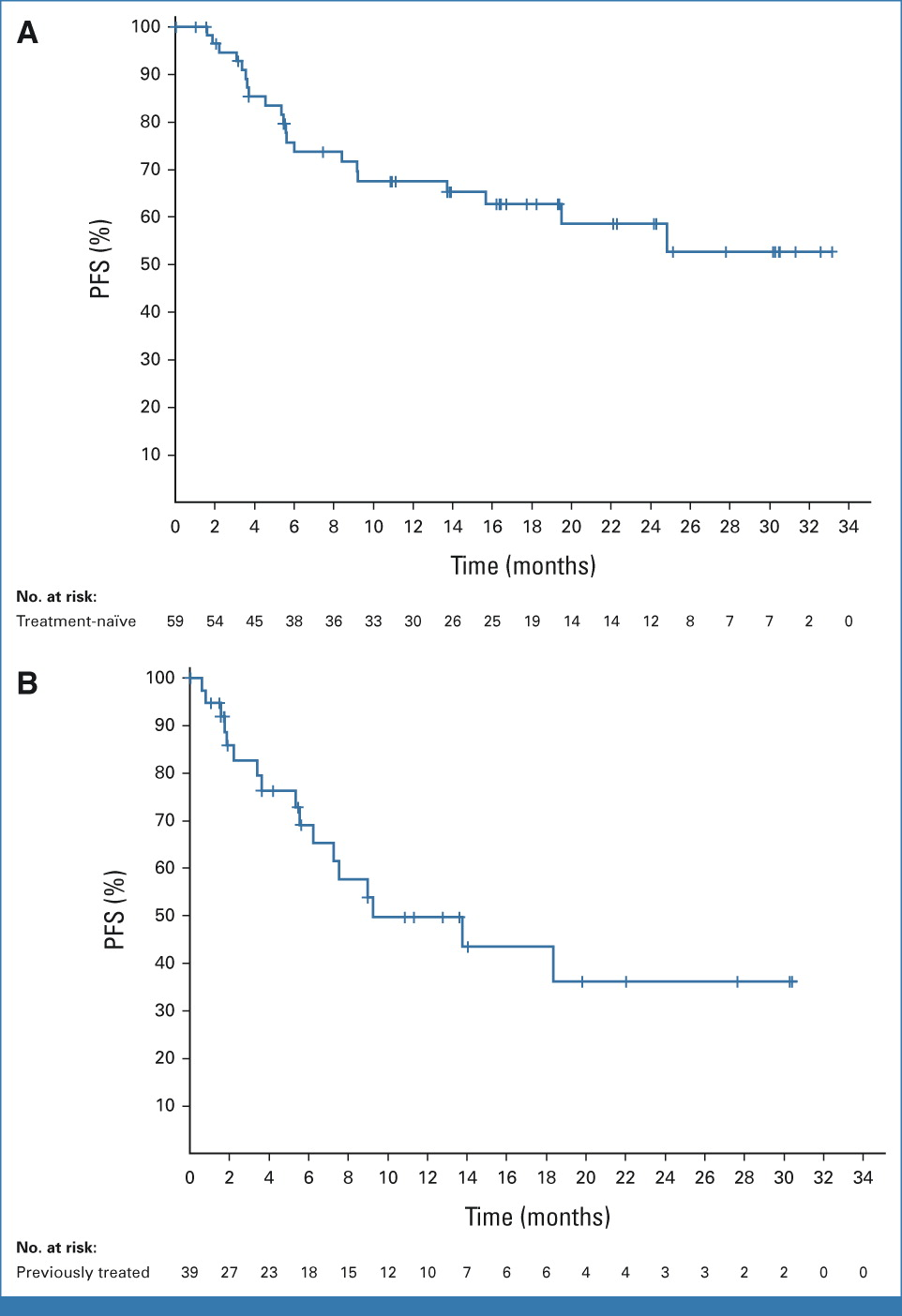
截至2022 年 6 月 2 日,共98例患者被纳入试验,其中59 名患者未接受过治疗,39 名患者既往接受过治疗。结果显示:在59例初治患者中,客观缓解率(ORR)实现75%,其中35例患者实现部分缓解(PR),9例患者实现完全缓解(CR)。在39例接受过治疗的患者中,ORR为46%,其中有14例患者实现部分缓解(PR),4例患者实现完全缓解(CR)。有 59%初治患者和33%的既往接受过治疗的患者至少在治疗的前 12 个月内得到缓解。24 周后,初治患者的 疾病控制率(DCR)为 64%,既往接受过治疗的患者为 41%。初治患者的中位无进展生存期为18.2个月,既往接受过治疗的患者为12.8个月。
目前康和源免疫之家有治疗BRAF V600E突变的晚期非小细胞肺癌临床试验正在寻找患者:
项目名称:妥拉美替尼联合维莫非尼治疗BRAF V600E突变的晚期非小细胞肺癌Ⅱ期临床研究
部分入选标准:
1.年龄18-75周岁;
2.预期生存期 > 3个月;
3.晚期非小细胞肺癌患者;
4.能够提供BRAF V600E突变的基因检测报告。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://mma.prnewswire.com/media/2469963/PIERRE_FABRE_PDF.pdf
2.https://ascopubs.org/doi/10.1200/JCO.23.00774












