作者:小编
更新时间:2024-07-31
点击数:
7月30日,美国食品药品监督管理局(FDA)批准达雷妥尤单抗注射液联合硼替佐米、来那度胺和地塞米松用于诱导和巩固治疗符合自体干细胞移植 (ASCT) 条件的新诊断多发性骨髓瘤患者。

此次批准主要基于PERSEUS(NCT03710603)临床试验,旨在评估达雷妥尤单抗联合硼替佐米、来那度胺和地塞米松 (VRd)诱导和巩固治疗以及来那度胺维持治疗治疗符合移植条件的新诊断多发性骨髓瘤患者的疗效和安全性。该试验共纳入709例患者,其中达雷妥尤单抗组有355例患者,结果显示:达雷妥尤单抗组无进展生存4年的患者有84.3%,对照组为67.7%。完全缓解率(CR)分别为87.9%和70.1%。
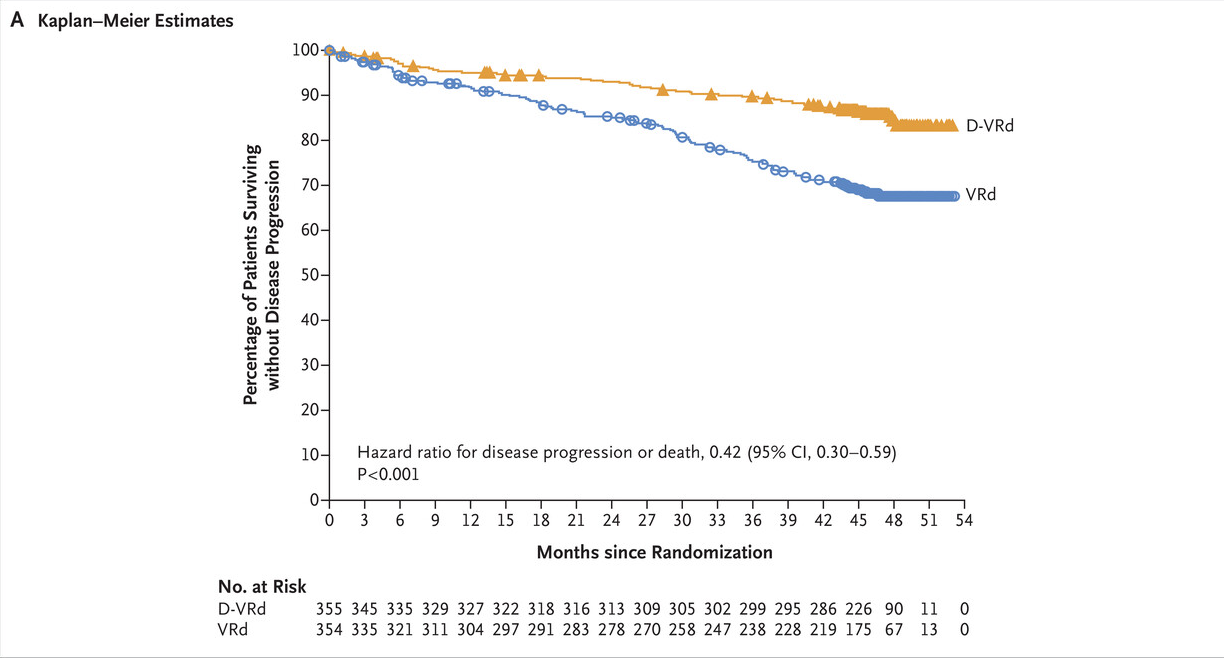
结果表明,在硼替佐米、来那度胺和地塞米松 (VRd)诱导和巩固治疗以及来那度胺维持治疗中加入皮下注射达雷妥尤单抗在符合移植条件的新诊断多发性骨髓瘤患者的无进展生存期方面具有显著优势。
目前康和源免疫之家有临床试验正在寻找多发性骨髓瘤患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
参考资料
https://www.nejm.org/doi/full/10.1056/NEJMoa2312054

相关推荐
随便看看
- 伯瑞替尼治疗携带 c-Met 改变的局部晚期或转移性非小细胞肺癌患者的II期KUNPENG 临床试验数据公布
- 瑞康曲妥珠单抗单药用于晚期非小细胞肺癌研究结果荣登《柳叶刀·肿瘤学》
- 复宏汉霖PD-L1 ADC HLX43首次人体I期临床研究的更新数据即将亮相2025 WCLC
- CT041治疗胰腺癌研究成果发表
- EGFR抑制剂佐利替尼获批上市
- 泽璟制药自主研发的新药Alveltamig、Nilvanstomig的临床研究数据及最新进展亮相2025 ESMO
- 抗癌“神药”拉罗替尼,成功通过谈判进入医保,让各类NTRK融合肿瘤患者病情缓解
- 小细胞肺癌新药获批上市!无进展生存率提升近4倍!小细胞肺癌治疗的重大进步!
- IMM2510联合化疗一线治疗非小细胞肺癌(NSCLC)患者的II期试验公布
- SHR-A1811拟纳入突破性治疗











