9月17日,美国食品药品监督管理局(FDA)批准ribociclib联合芳香化酶抑制剂用于辅助治疗激素受体阳性/人表皮生长因子受体 2 阴性 (HR+/HER2-) II 期和 III 期早期乳腺癌 (EBC)复发风险高的患者。

此次批准主要基于III 期NATALEE(NCT03701334)试验,该试验评估了ribociclib 与非甾体芳香酶抑制剂(NSAI)的疗效。该数据结果发表于《新英格兰医学杂志》上。
共有 5101 例患者接受治疗,其中2549例患者接受ribociclib联合芳香化酶抑制剂治疗,2552例患者接受芳香化酶抑制剂治疗,结果显示:联合治疗组3年无侵袭性疾病生存率(iDFS)为 90.4%,单独治疗组为 87.1%。
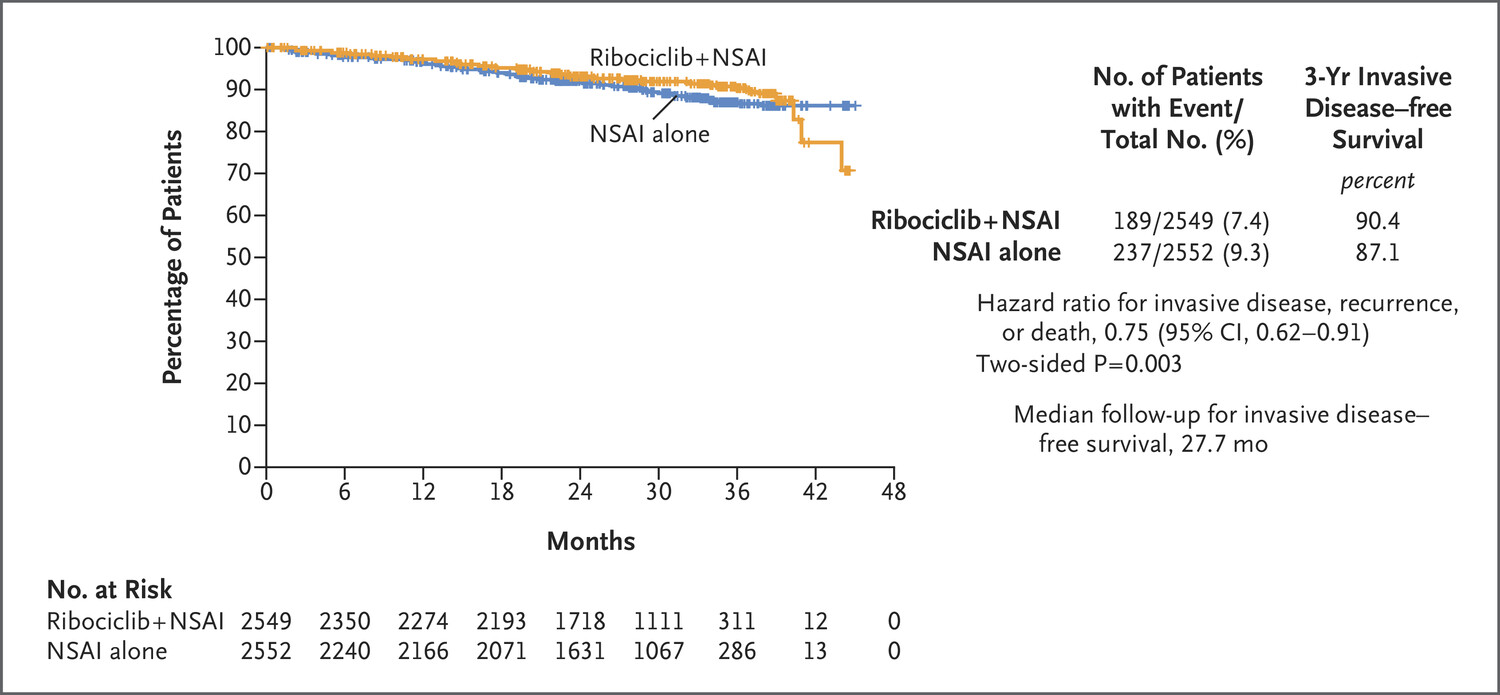
3年远处无病生存率(DFS)分别为 90.8%和88.6%,无复发生存率(RFS)分别为 91.7%和88.6%。

该数据表明,ribociclib联合芳香化酶抑制剂显著提高早期乳腺癌患者的无侵袭性疾病生存率。
关于ribociclib
瑞博西尼是一种细胞周期蛋白依赖性激酶(CDK4/CDK6)小分子抑制剂,一类通过抑制称为细胞周期蛋白依赖性激酶 4 和 6 (CDK4/6) 的两种蛋白质来帮助减缓癌症进展的药物。这些蛋白质在过度激活时,会使癌细胞生长和分裂得太快。以更高的精度靶向 CDK4/6 可能有助于确保癌细胞不会继续不受控制地复制。
目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-kisqali-aromatase-inhibitor-and-kisqali-femara-co-pack-early-high-risk-breast-cancer
2.https://www.novartis.com/news/media-releases/fda-approves-novartis-kisqali-reduce-risk-recurrence-people-hrher2-early-breast-cancer
3.https://www.nejm.org/doi/full/10.1056/NEJMoa2305488

相关推荐
随便看看
- 美国FDA授予靶向HER3的新一代ADC产品DB-1310快速通道资格认定
- 信达生物 PD-1 联合疗法申报上市
- 利厄替尼片获批上市,用于EGFR T790M 突变阳性非小细胞肺癌
- 依沃西单抗第二项肺癌适应症获批
- ADC药物Blenrep联合方案获批用于多发性骨髓瘤
- ADC药物Precem-TcT用于结直肠癌的I期试验结果登《自然医学》
- STING 激动剂 E7766 在晚期实体瘤中的 I 期临床数据公布
- 戈沙妥珠单抗获批新适应症,用于治疗转移性HR+/HER2-乳腺癌
- RMC-6236 在胰腺导管腺癌患者中的数据公布
- 德曲妥珠单抗DESTINY-Breast05 Ⅲ期研究结果亮相2025 ESMO











