9月14日,《新英格兰医学杂志》在线发表了Trastuzumab Deruxtecan (优赫得,德曲妥珠单抗,DS-8201,Enhertu,T-Dxd)治疗HR+、HER2 低表达(IHC 1+或IHC 2+/ISH-)或HER2-ultralow(定义为IHC 0伴有膜染色,即IHC >0且<1+)晚期或转移性乳腺癌患者的III期DESTINY-Breast06研究数据。

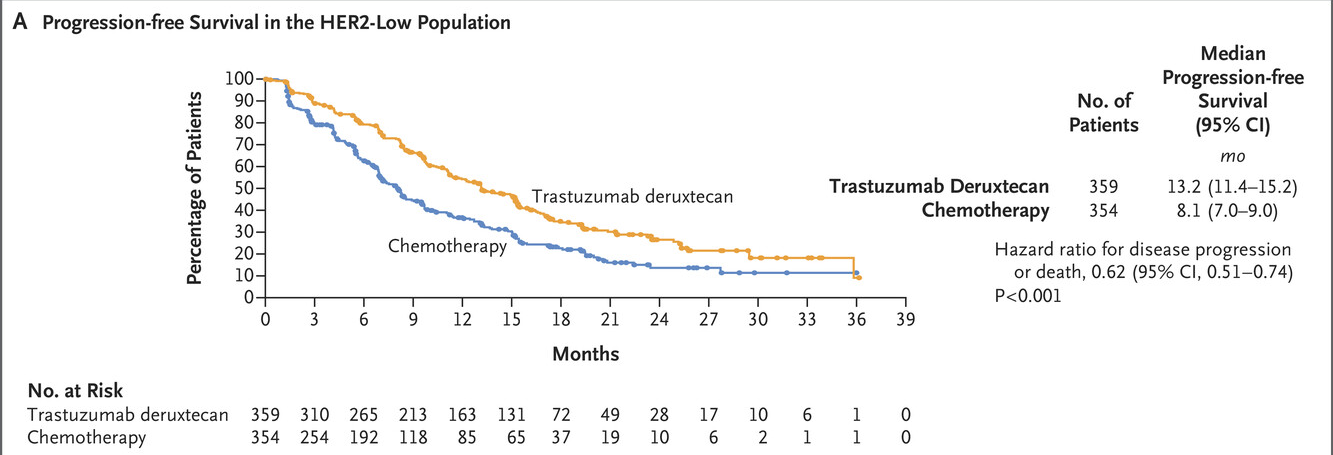
该试验共436例患者接受德曲妥珠单抗治疗,430 例患者接受化疗,结果显示:HER2 低人群中,德曲妥珠单抗组的中位无进展生存期(PFS)为13.2 个月,化疗组为 8.1 个月。德曲妥珠单抗组的1年总生存率为 87.6%,化疗组为 81.7%。客观缓解率(ORR)分别为56.5%和32.2% ,德曲妥珠单抗组有9例患者实现完全缓解(CR)。德曲妥珠单抗组中位缓解持续时间(DOR)为 14.1 个月,在化疗组中为 8.6 个月。
HER2 超低人群中德曲妥珠单抗组的中位无进展生存期(PFS)为13.2 个月,化疗组为8.3 个月。德曲妥珠单抗组的客观缓解率(ORR)为 61.8%,化疗组为 26.3%。

结果表明,在激素受体阳性、HER2低或HER2超低转移性乳腺癌患者中,德曲妥珠单抗显著延长无进展生存期。
关于德曲妥珠单抗
德曲妥珠单抗(T-Dxd,DS-8201)是一款靶向HER2的新型ADC药物,是ADC药物的杰出代表。
2023年2月24日,国家药监局(NMPA)官网最新公示,德曲妥珠单抗已在国内获批上市,用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。
2023年7月12日,德曲妥珠单抗(Enhertu)获得中国国家药品监督管理局批准用于治疗既往在转移性疾病阶段接受过至少一种系统治疗或在辅助化疗期间或完成辅助化疗之后6个月内复发、不可切除或转移性的HER2低表达(IHC 1+或IHC 2+/ISH-)成人乳腺癌患者。
目前德曲妥珠单抗正在全国范围内寻找HER2过表达的实体瘤患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以联系康和源免疫之家医学部(400-880-3716)。
部分入选标准:
1.年龄至少 18 岁;
2.晚期实体瘤患者;
3.ECOG体能状态评分为0~1。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可致电至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.nejm.org/doi/full/10.1056/NEJMoa2407086

相关推荐
随便看看
- ADC药物MRG003(注射用维贝柯妥塔单抗)获批上市,鼻咽癌患者获益
- Tucatinib联合曲妥珠单抗治疗HER2突变转移性乳腺癌患者的2期SGNTUC-019试验公布
- KRAS G12D抑制剂ABSK141新药临床试验申请获得美国FDA批准
- 盐酸特泊替尼被正式纳入国家医保目录
- DM005新药临床研究申请获国家药监局批准
- 贝伐珠单抗Bevacizumab
- 改写食管癌治疗格局!中国研究亮相ESTRO 2025
- 中国研究团队研究了信迪利单抗联合化疗对晚期食管鳞状细胞癌受试者的HRQoL方面的影响
- MEK抑制剂芦沃美替尼II期临床数据亮相国际神经纤维瘤病大会
- ADC药物Iza-Bren(BL-B01D1)亮相ESMO BC 2025











