近日,国家药品监督管理局(NMPA)批准戈沙妥珠单抗(Trodelvy,拓达维)用于治疗既往接受过内分泌治疗且在转移性疾病阶段接受过至少二种其他系统性治疗的不可切除局部晚期或转移性的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性(IHC 0、IHC1+或IHC 2+/ISH-)乳腺癌成人患者。

戈沙妥珠单抗是全球首个获批的靶向Trop-2的抗体偶联药物(ADC),由靶向TROP-2抗原的人源化IgG1抗体-hRS7与拓扑异构酶I抑制剂伊立替康的代谢活性产物SN-38通过可水解的Linker偶联而成。
2022年6月10日获得国家药监局批准用于既往至少接受过2种系统治疗(其中至少一种治疗针对转移性疾病)的不可切除的局部晚期或转移性三阴性乳腺癌成人患者。
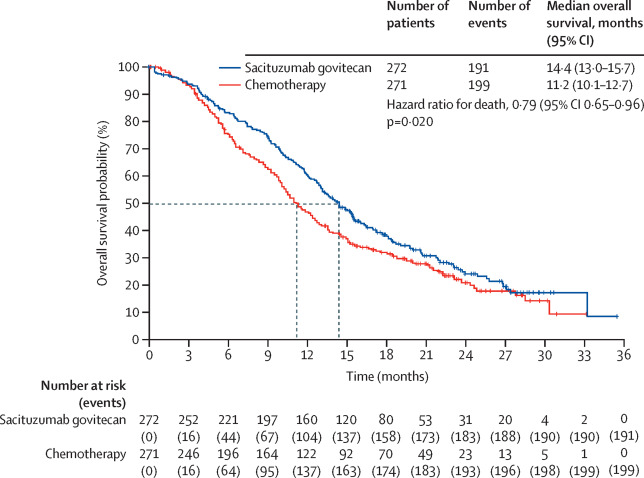
2023年8月,《柳叶刀》发表了戈沙妥珠单抗治疗激素受体阳性和人表皮生长因子受体 2 阴性转移性乳腺癌 (TROPiCS-02) 的3期TROPiCS-02 (NCT03901339)研究。该试验对 543 名不可切除的局部晚期或转移性 HR 阳性、HER2 阴性乳腺癌患者进行了疗效评估,结果显示:
戈沙妥珠单抗组有57例患者肿瘤缩小或消失,其中2例患者完全缓解(CR),55例患者部分缓解(PR),142例患者病情稳定(SD)。而化疗组271例患者中仅38例患者肿瘤缩小,106例患者病情稳定(SD)。中位缓解持续时间(DOR)分别为8.1个月,化疗组为5.6个月。
戈沙妥珠单抗组中位总生存期(OS)为14.4个月,化疗组为11.2个月,12 个月总生存率分别为61%和47%。
目前ADC药物有临床试验正在寻找胃癌、乳腺癌、头颈癌等患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(23)01245-X/fulltext

相关推荐
随便看看
- PD-1抑制剂帕博利珠单抗获批联合曲妥珠单抗和化疗治疗局部晚期不可切除或转移性HER2阳性胃或胃食管结合部腺癌
- ADC药物有哪些?
- EGFR抑制剂佐利替尼获批上市
- 替雷利珠单抗RATIONALE-315研究的最终分析结果和RATIONALE-303研究的长期随访数据亮相2025 WCLC
- 盐酸安罗替尼胶囊拟纳入优先审评
- 帕博利珠单抗在国内获批局部晚期宫颈癌适应症
- 针对EGFR20外显子插入的莫博赛替尼上市
- 抗CTLA-4安全抗体ADG126联合帕博利珠单抗的1b/2期临床研究最新数据即将亮相2025 ASCO
- 皮尔法伯实验室获得欧洲药品管理局人用药品委员会 (CHMP) 针对 BRAFTOVI®(康奈非尼)联合 MEKTOVI®(比美替尼)用于 BRAFV600E 突变晚期非小细胞肺癌 (NSCLC) 成人
- 疾病进展或死亡风险降低41%!FDA批准帕博利珠单抗联合放化疗治疗III-IVA期宫颈癌











