10月17日,康宁杰瑞宣布,HER2双特异性抗体KN026联合白蛋白结合型多西他赛HB1801的一项Ⅲ期临床研究申请已获得国家药品监督管理局药品审评中心(CDE)批准,用于HER2阳性早期或局部晚期乳腺癌的新辅助治疗。该试验旨在比较KN026联合HB1801与曲妥珠单抗联合帕妥珠单抗和多西他赛新辅助治疗早期和局部晚期HER2阳性乳腺癌患者的有效性和安全性。
2022年,《CLINICAL CANCER RESEARCH》报告了KN026作为单一疗法用于HER2阳性转移性乳腺癌(MBC)患者的I期试验KN026-CHN-001(NCT03619681)结果。

该试验共纳入63例患者,结果显示:43例患者观察到肿瘤缩小,1例患者实现完全缓解(CR),15例患者实现部分缓解(PR),28 例患者病情稳定(SD),疾病控制率(DCR)为 69.8%,中位无进展生存期(PFS)为 5.6 个月,未达到中位总生存期 (OS),1年生存率为 85.8%。
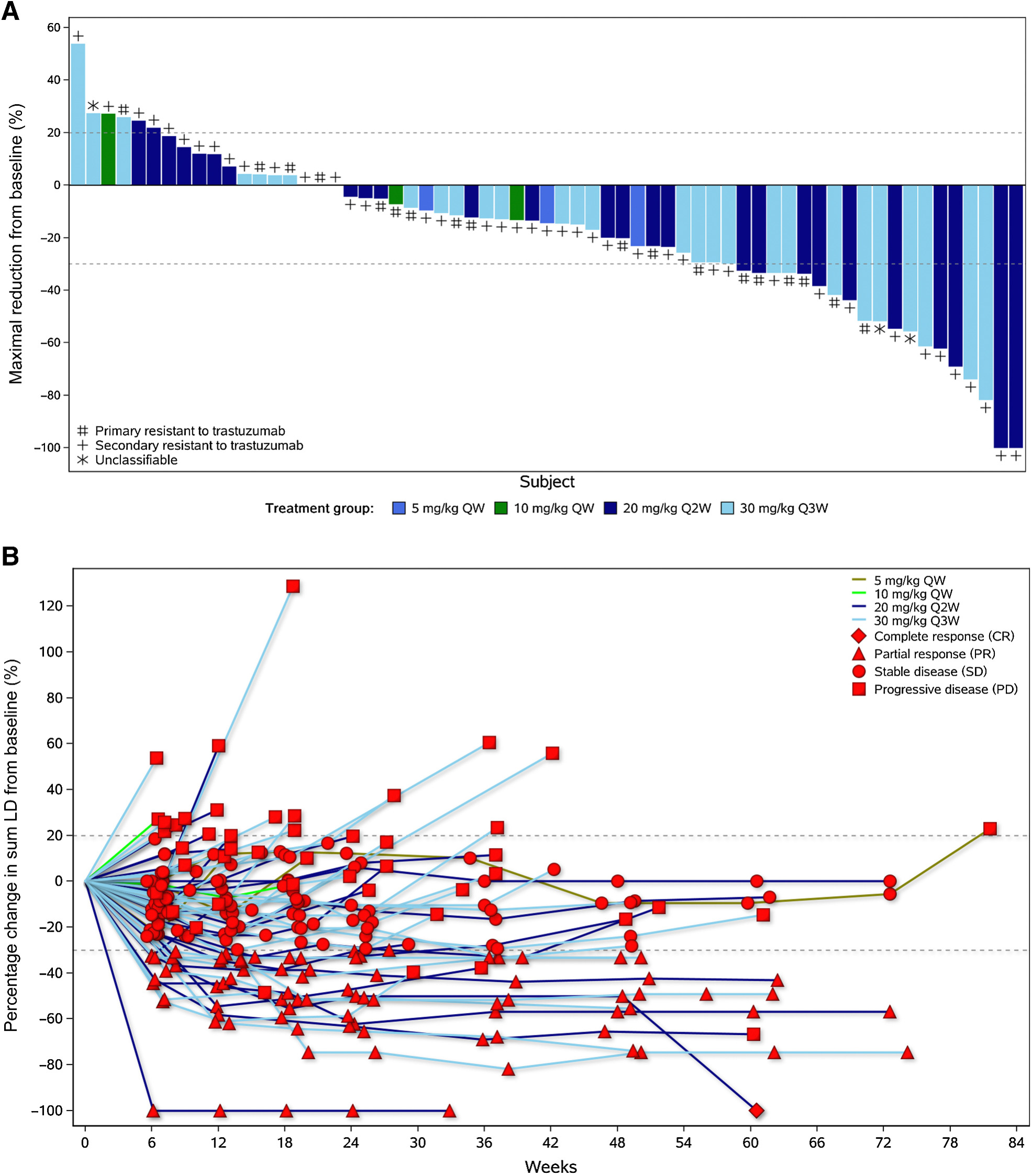
该试验表明,KN026耐受性良好。
KN026是康宁杰瑞自主研发的HER2双特异性抗体,2023年欧洲肿瘤内科协会(ESMO)上报告了KN026联合多西他赛一线治疗HER2阳性复发或转移乳腺癌的两年半随访数据KN026-201(NCT04165993)。
该试验共入组57例HER2阳性初治复发或转移性乳腺癌患者,55例患者可评估疗效,结果显示:客观缓解率(ORR)为76.4%,中位无进展生存期(mPFS)为27.7个月,中位总生存期(mOS)未达到。1年生存率为93%,24个月和30个月的生存率分别为84.1% 和78.5%。
该试验表明,KN026联合多西他赛作为一线方案治疗HER2阳性乳腺癌具有良好的耐受性和良好的临床获益。
目前有临床试验正在寻找乳腺癌患者,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可致电至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.annalsofoncology.org/article/S0923-7534(23)01431-X/fulltext
2.https://aacrjournals.org/clincancerres/article/28/4/618/678114/First-in-human-HER2-targeted-Bispecific-Antibody

相关推荐
随便看看
- 双特异性抗体Linvoseltamab治疗复发/难治性多发性骨髓瘤
- 新一代广谱抗癌药瑞普替尼(TPX-0005)获批上市!用于治疗ROS1融合阳性非小细胞肺癌!
- 聚焦2025 ASCO:ADC“生物导弹”集群爆发,横扫尿路上皮癌、肺癌、食管癌等
- 总生存率高达99%!纳武利尤单抗联合AVD化疗方案延长霍奇金淋巴瘤患者无进展生存期
- ABSK043联合戈来雷塞的临床研究申请获批
- ZUMA-3研究:接受Brexu-cel治疗长达4年的随访结果公布!中位总生存期为25.6个月
- CDK4/6抑制剂泰瑞西利胶囊III期临床研究成果亮相《JAMA Oncology》
- 第三代EGFR TKI 肺癌靶向药物利厄替尼片获批新适应症
- 美国前沿药LSTA1获美国FDA授予治疗骨肉瘤的孤儿药资格!
- FDA授予NT-I7治疗晚期胰腺癌的孤儿药资格!为患者带来一种新的治疗选择











