近日,康方生物宣布其独立自主研发的PD-1/VEGF双特异性抗体依沃西联合方案对比度伐利尤单抗(PD-L1)联合方案,一线治疗晚期胆道癌(BTC)的随机、对照、多中心注册性III期临床研究(HARMONi-GI-01/AK112-309)完成首例患者入组。
此前,依沃西联合化疗一线治疗晚期BTC的II期临床研究的优异结果已发表于2024年美国临床肿瘤学会(ASCO)年会。研究结果显示,依沃西方案具有显著的抗肿瘤活性和良好的安全性。
客观缓解率(ORR)为63.6%,其中胆囊癌患者的ORR为77.8%。疾病控制率(DCR)为100%。

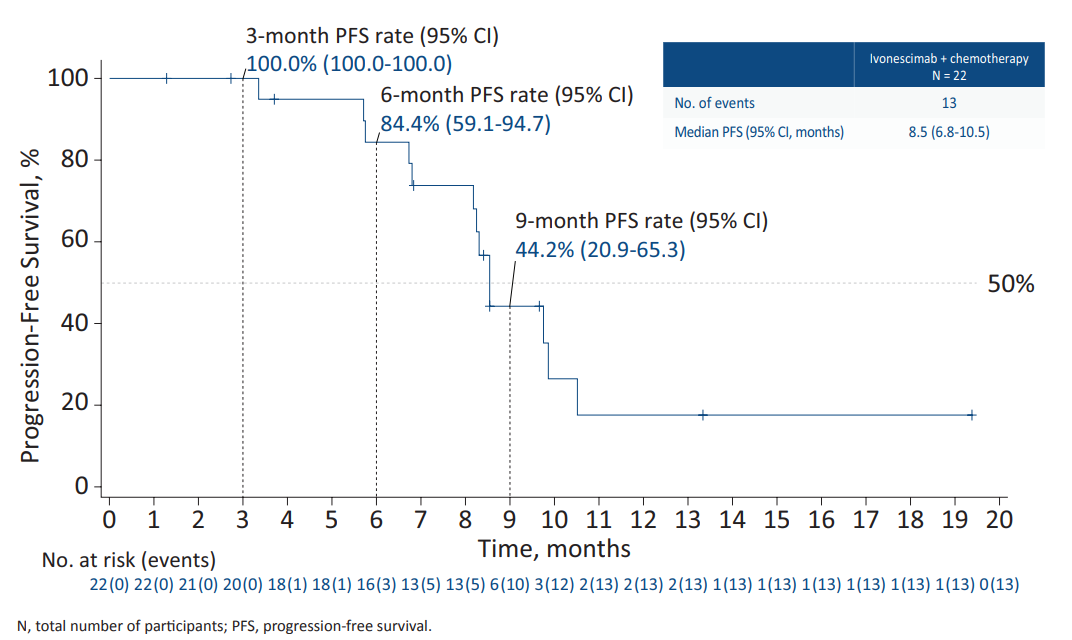
中位无进展生存期(PFS)为8.5个月,6个月PFS率为84.4%。
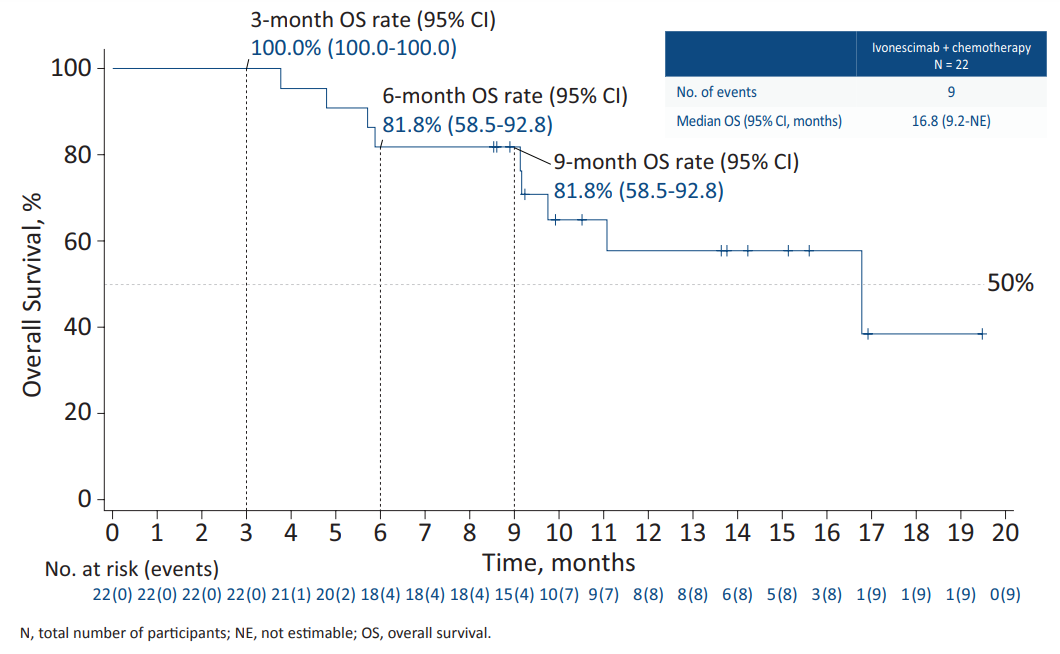
中位总生存期(OS)为16.8个月,9个月OS率为81.8%;其中胆囊癌患者的中位OS为16.8个月。
依达方®(依沃西单抗注射液)是康方生物自主研发的、全球首创PD-1/VEGF双特异性肿瘤免疫治疗药物。依达方®于2024年5月获得中国国家药品监督管理局批准上市,用于EGFR-TKI治疗进展的局部晚期或转移性nsq-NSCLC,成为全球首个获批上市的“肿瘤免疫+抗血管生成“协同抗肿瘤机制的双特异性抗体新药。
胆道恶性肿瘤是来源于胆管及胆囊的一组高度异质性恶性肿瘤,预后差,50%的胆道恶性肿瘤病人在确诊时已为进展期,生存期不足1年。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找胆管癌患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.akesobio.com/media/2270/final-asco-2024-btc-poster.pdf

相关推荐
随便看看
- IBI363关键注册研究完成首例受试者给药
- 震惊!“智能炸弹”抗体偶联药物实力霸屏,惊艳肺癌、乳腺癌、尿路上皮癌患者
- 卡瑞利珠单抗
- 埃万妥单抗联合化疗方案获批用于EGFR TKI经治后局部晚期或转移性非小细胞肺癌患者
- 君实生物创新产品选择性PI3K-α抑制剂JS105的I期临床研究结果亮相2025 ESMO
- 派安普利单抗联合方案一线治疗肝细胞癌的上市申请获受理
- 抗癌界“智能炸弹”ADC 药物来袭!横扫尿路上皮癌、宫颈癌、头颈癌、肺癌、淋巴瘤
- 肺癌、鼻咽癌、头颈鳞癌新希望!ADC药物MRG003上市,疗效数据惊艳,疾病控制率高达93.3%
- 中位生存期为21.4个月!Belzutifan亮相《新英格兰医学杂志》,肾癌患者新的治疗选择
- 依沃西联合方案一线治疗三阴性乳腺癌Ⅲ期临床完成首例患者入组











