
12月9日,第一三共宣布美国食品药品监督管理局(FDA)授予Datopotamab deruxtecan (Dato-DXd)突破性疗法认定,用于治疗接受EGFR 酪氨酸激酶抑制剂(TKI)和铂类化疗期间或之后出现疾病进展的局部晚期或转移性表皮生长因子受体突变(EGFR 突变)非小细胞肺癌(NSCLC)成人患者。

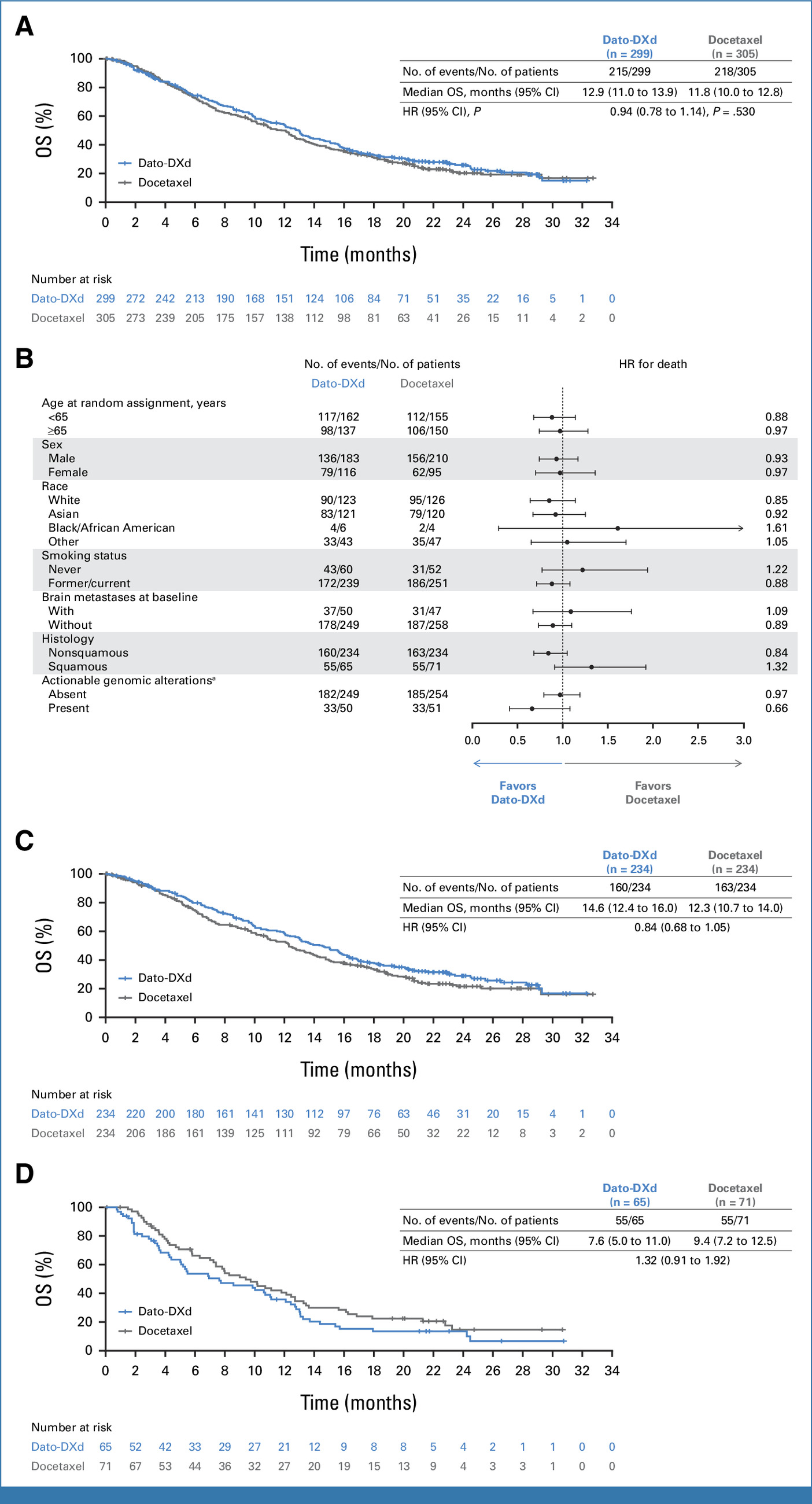
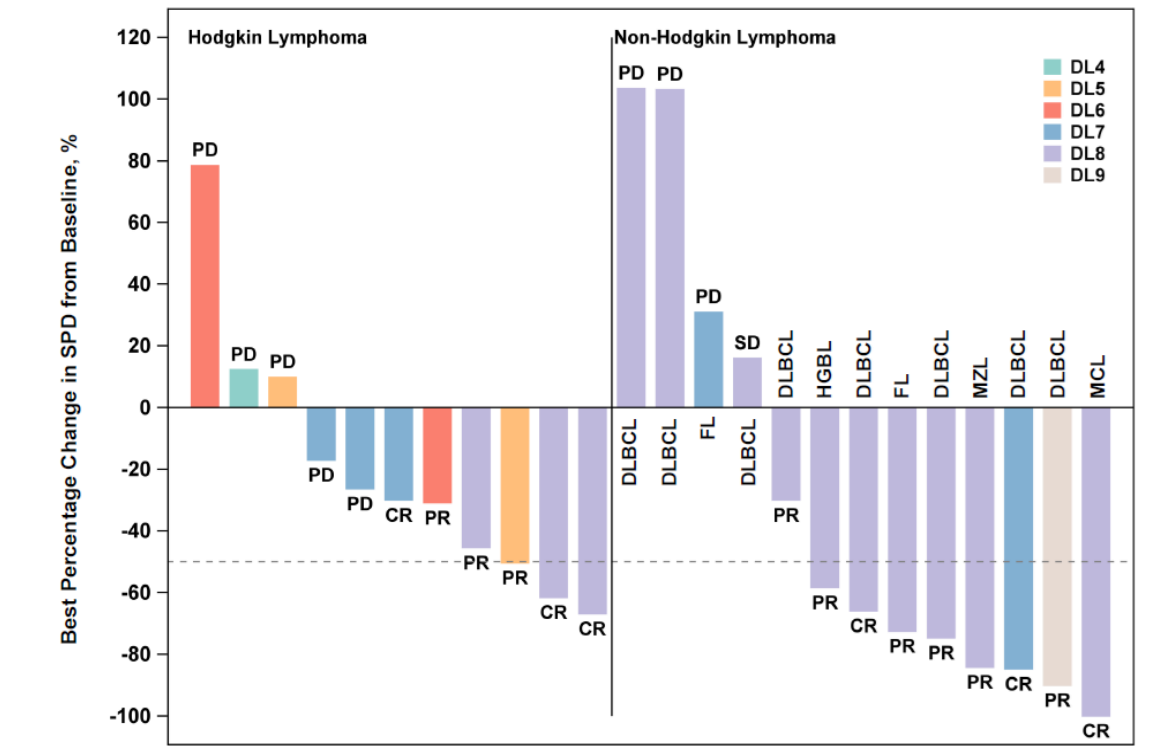
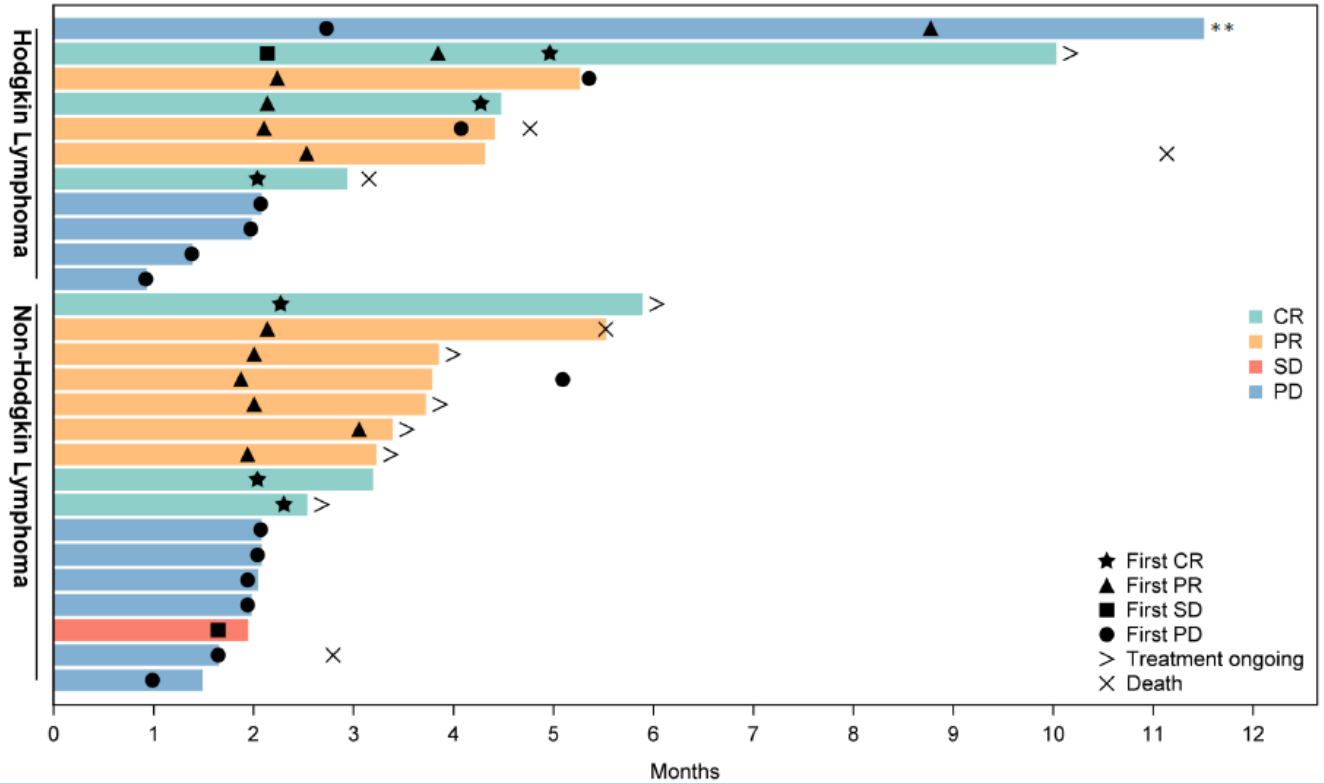
截图源于参考资料4
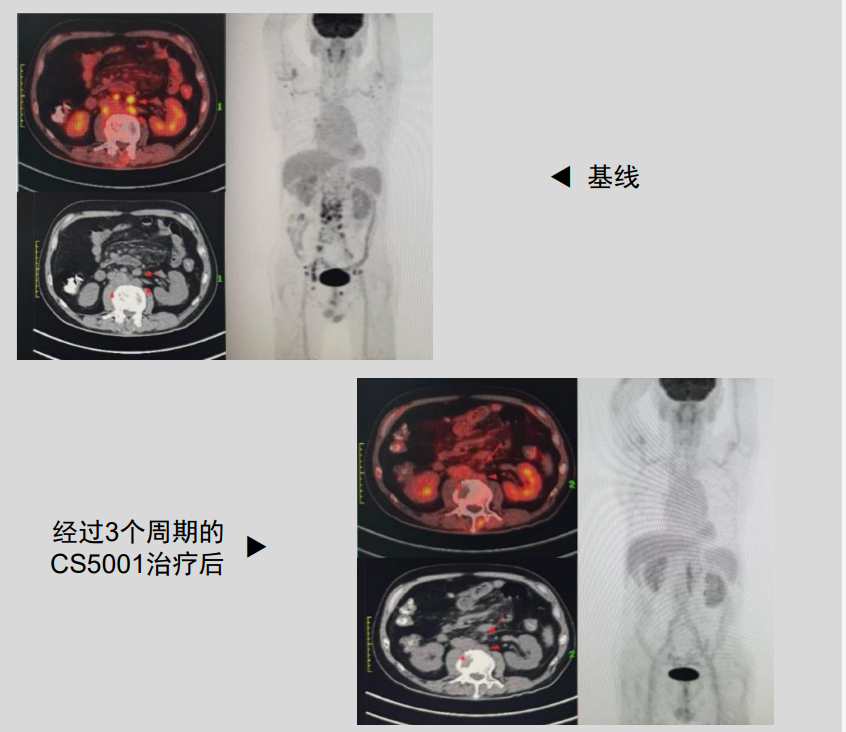
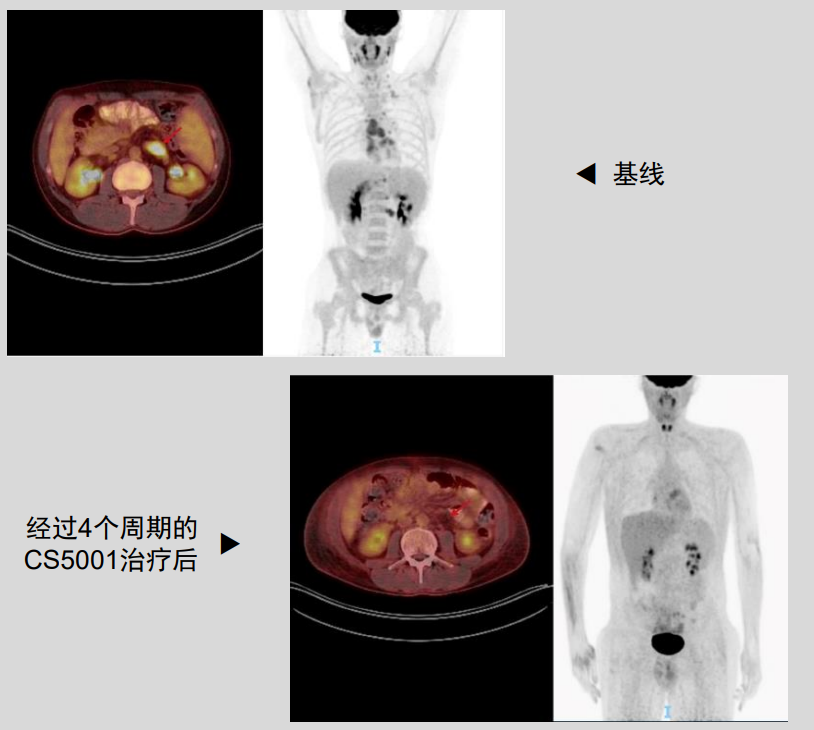
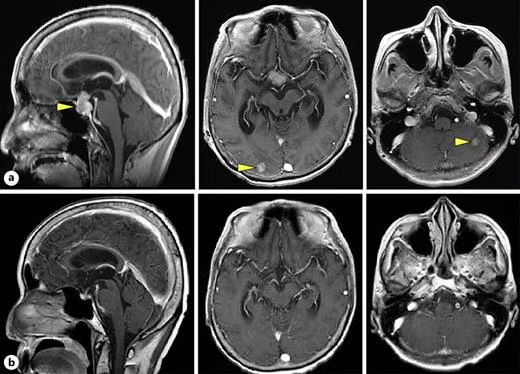
参考资料 1.https://daiichisankyo.us/press-releases/-/article/datopotamab-deruxtecan-granted-breakthrough-therapy-designation-in-u-s-for-patients-with-previously-treated-advanced-egfr-mutated-non-small-cell-lung- 2.https://ascopubs.org/doi/10.1200/JCO-24-01544 3.https://ash.confex.com/ash/2024/webprogram/Paper192979.html 4.https://www.cstonepharma.com/uploads/2024/12/173380023764077.pdf 5.https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.3028 6.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10730032/ 7.https://karger.com/cro/article/16/1/497/853868/Dramatic-Recovery-of-Vision-after-Trastuzumab
相关推荐
随便看看
- 抗体偶联药物强势来袭,实体瘤治疗大突破,ADC药物成头颈癌、肺癌、尿路上皮癌、胰腺癌“香饽饽”
- 美国FDA授予ADRX-0706快速通道资格,用于鳞状细胞宫颈癌
- PD-L1贝莫苏拜单抗联合安罗替尼为肾癌、肉瘤、子宫内膜癌带来新治疗选择
- 疾病控制率高达100%!EGFR×HER3双抗ADC药物BL-B01D1狙击多实体瘤
- 瑞康曲妥珠单抗(SHR-A1811)治疗晚期HER2突变非小细胞肺癌研究结果公布于AACR
- 安达替尼上市申请获受理
- 卡瑞利珠单抗
- 日本上市佐妥昔单抗(Zolbetuximab),claudin (CLDN)18.2阳性胃癌患者迎来新药
- KN026
- 安罗替尼在国内的第九个适应症获批











