2月17日,国家药品监督管理局药品审评中心(CDE)显示:翰森生物的注射用HS-20093拟纳入突破性治疗,用于治疗经至少二线治疗后进展的骨肉瘤患者。

HS-20093是一种靶向B7-H3的新型抗体-药物偶联物(ADC),由全人源抗B7-H3单抗与拓扑异构酶抑制剂(TOPOi)有效载荷共价连接而成。
2024年美国肿瘤学会(ASCO)上口头报告了HS-20093治疗骨肉瘤患者II期ARTEMIS-002 试验数据结果。ARTEMIS-002研究是一项开放标签、双臂、Ⅱ期临床研究,纳入经标准全身系统治疗后进展的R/R骨肉瘤(N=42)或其他肉瘤(N=20)患者。
共纳入42例R/R骨肉瘤患者接受HS-20093治疗,38例可评估疗效患者中,12.0 mg/kg HS-20093治疗组患者的ORR为17.4%;8 mg/kg组和12.0 mg/kg组患者的疾病控制率分别为66.7%和87.0%。
对于纳入的20例接受12.0 mg/kg剂量的其他肉瘤患者均可评估疗效,ORR为25.0%,在2例尤文肉瘤、1例骨未分化多形性肉瘤、1例滑膜肉瘤和1例其他未分类的软组织肉瘤观察到了疾病部分缓解(PR),中位PFS期为7.1个月。
安全性上,常见≥3级的不良事件(发生率≧10%)为中性粒细胞计数降低、白细胞计数降低、淋巴细胞计数降低、血小板计数降低和贫血。
初步数据显示,HS-20093在既往充分治疗的复发或难治性骨与软组织肉瘤患者中表现出了较强的抗肿瘤活性,优于临床现有标准治疗历史数据,且安全耐受性良好。
典型病例如下:
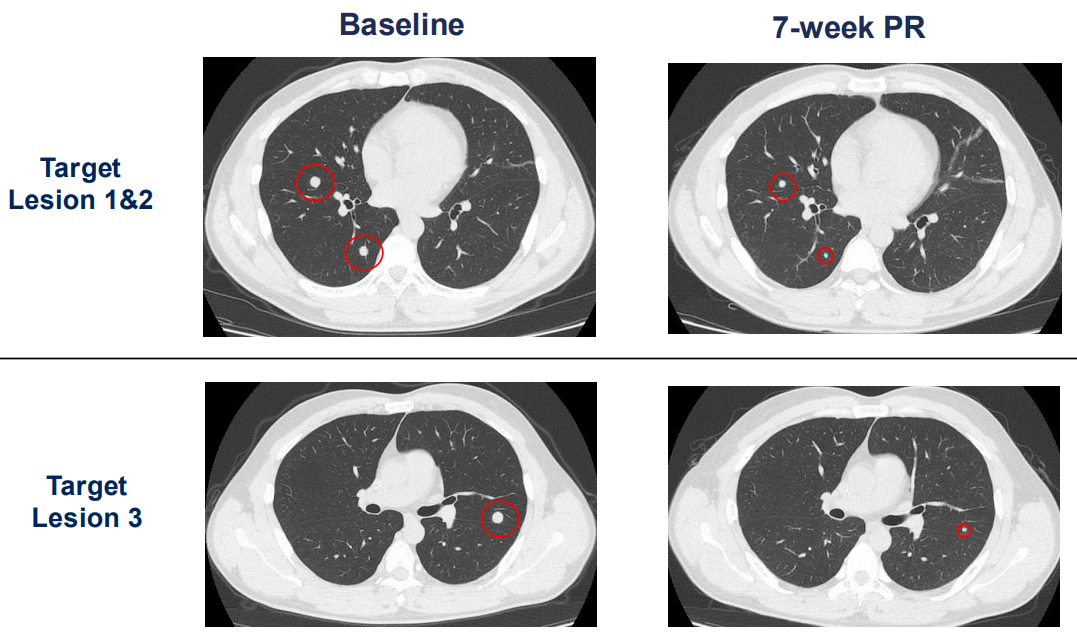
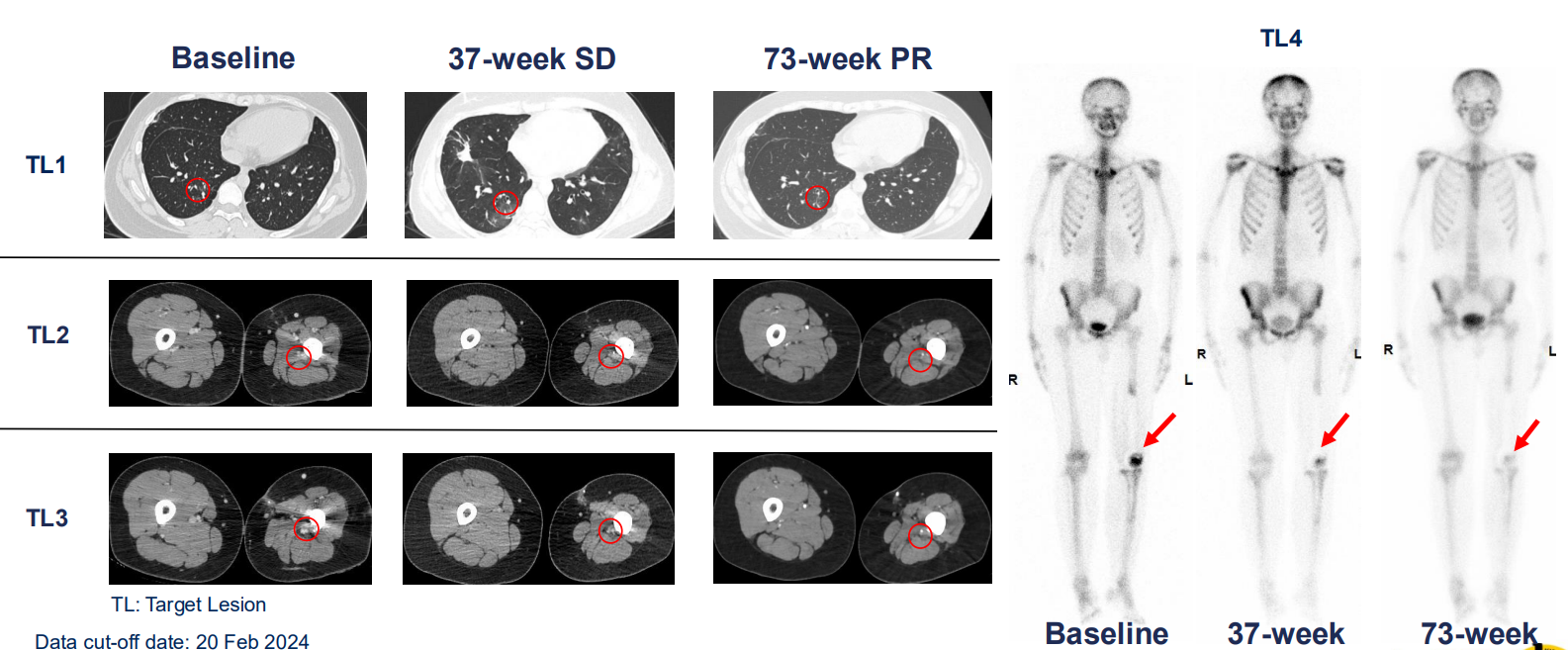
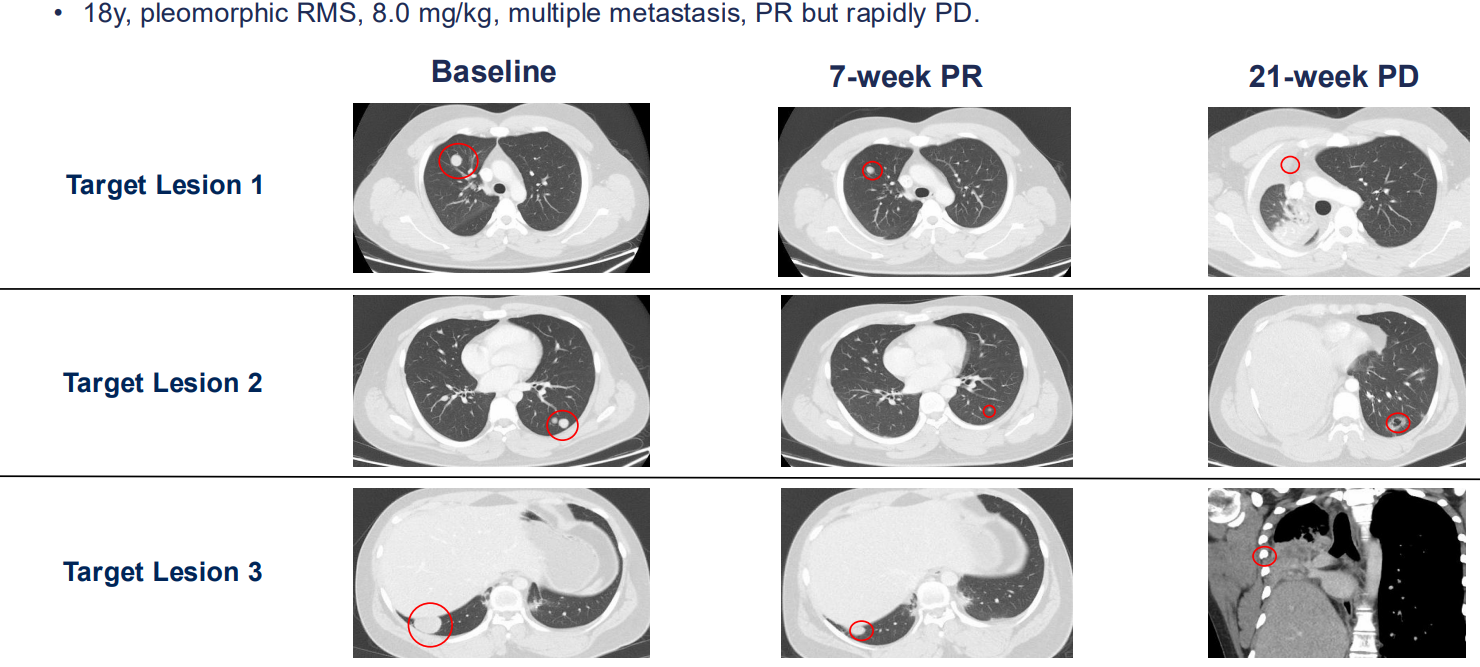
目前国内多家权威三甲医院已开展临床试验,正在寻找适合的患者。临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.11507
2.https://cdn.prod.website-files.com/5fa31a4ab3ea0180b3d65627/66bbca73e738a70465819474_F24%20Clinical%20Trials%20panel%20-%20XIE.pdf

相关推荐
随便看看
- “不完美心动”——干细胞叫嚣“心衰”
- ZUMA-3研究:接受Brexu-cel治疗长达4年的随访结果公布!中位总生存期为25.6个月
- 美国FDA批准CSF1R抑制剂Romvimza用于腱鞘巨细胞瘤
- RC148注射液拟纳入突破性治疗
- 依沃西单药对比帕博利珠单抗单药一线治疗非小细胞肺癌的III期HARMONi-2研究亮相WCLC
- 实现了100%的临床完全缓解率!多塔利单抗在 dMMR 直肠癌有希望的结果
- 美国FDA批准telisotuzumab vedotin用于c-Met蛋白高表达的局部晚期或转移性非鳞状非小细胞肺癌成人患者
- ADC药物瑞康曲妥珠单抗(艾维达,SHR-A1811)上市
- 艾伯维向美国FDA提交Teliso-V生物制剂许可申请用于非鳞状非小细胞肺癌
- ADC药物Iza-Bren(BL-B01D1)亮相ESMO BC 2025











