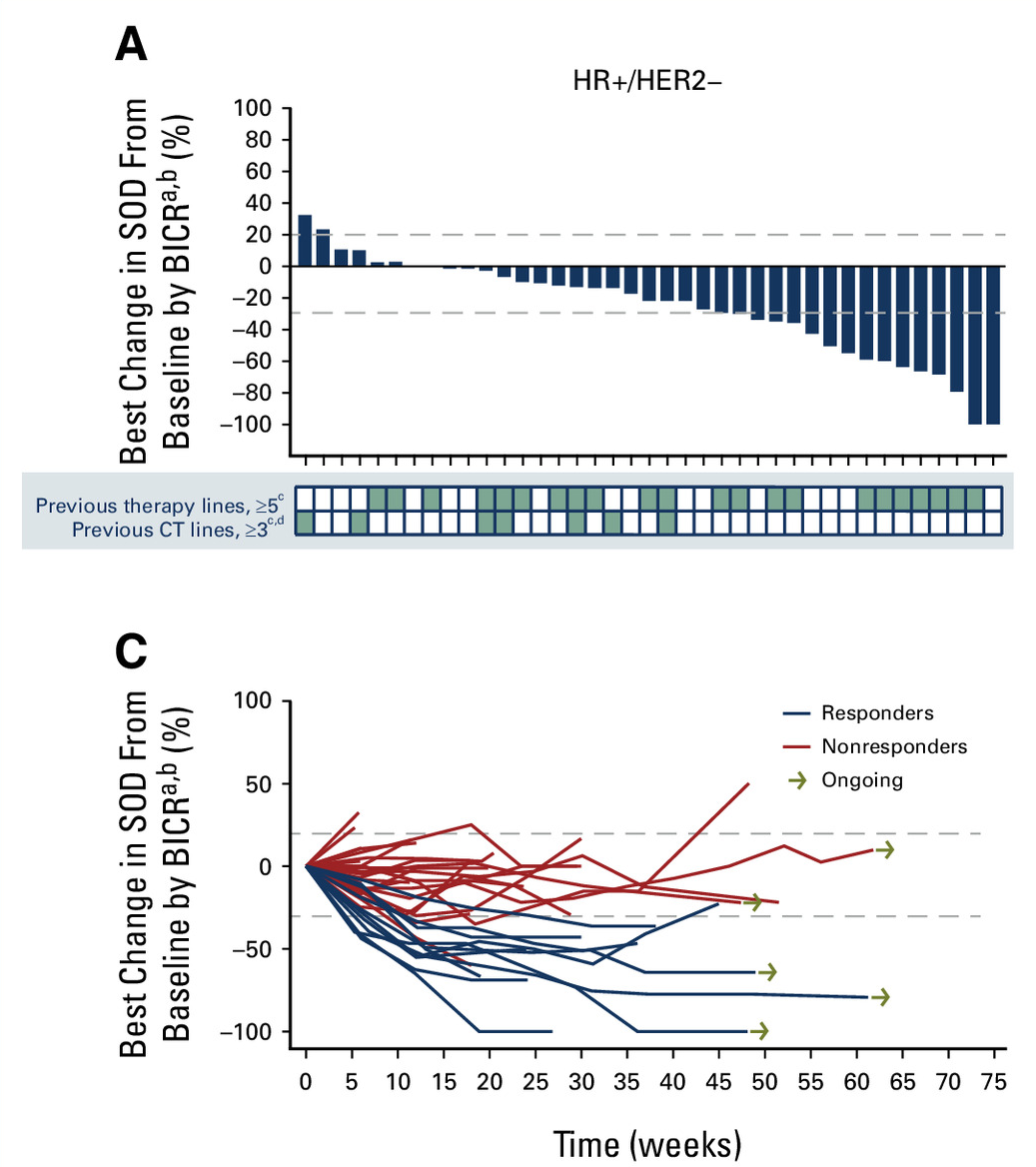
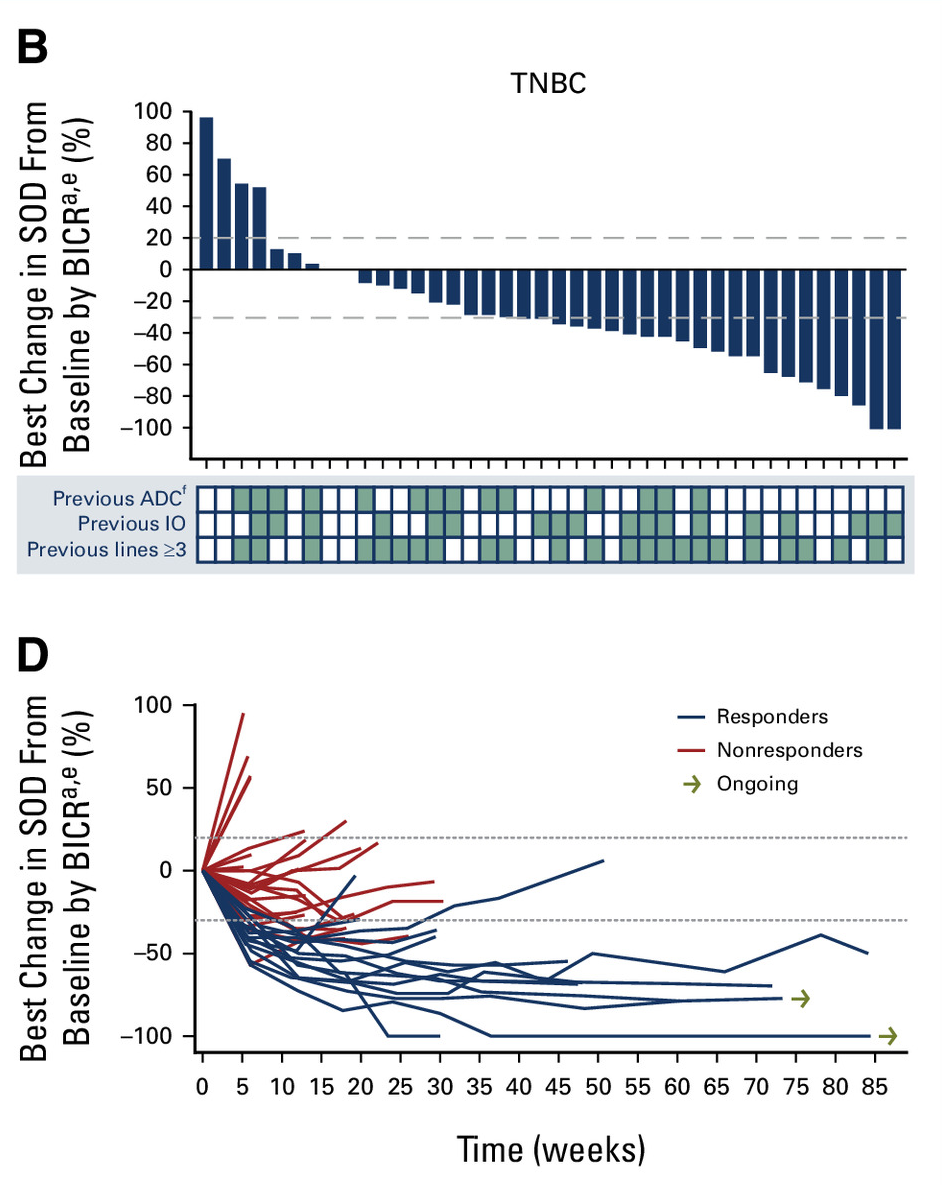
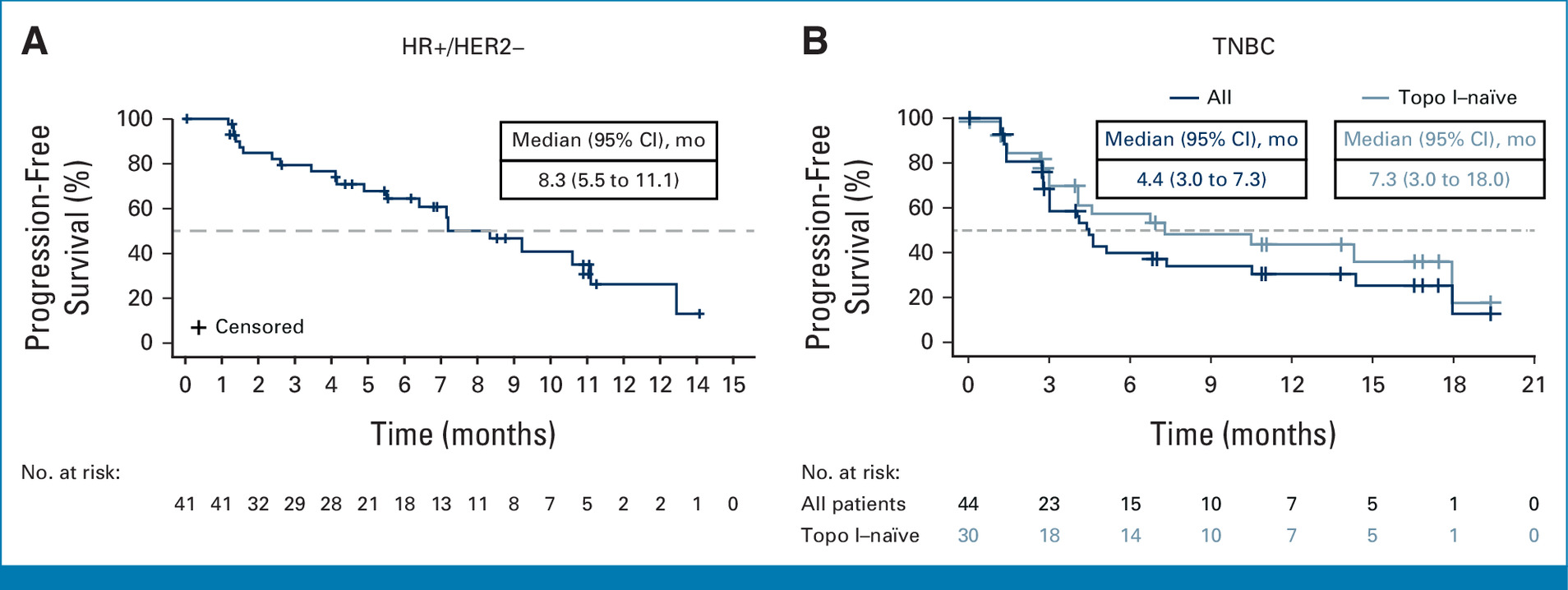
2025年1月6日,《Journal of Clinical Oncology》发表了Datopotamab deruxtecan治疗既往经治的伴可靶向基因组变异(AGA)的晚期或转移性非小细胞肺癌的II期TROPION-Lung05 研究结果。 截图源于参考资料1
共有 137 名患者接受了Dato-DXd治疗。结果显示:4名患者完全缓解(CR),45名患者部分缓解(PR),56例病情稳定(SD),疾病控制率(DCR)为 78.8%,中位缓解持续时间(DOR)为7.0 个月,中位无进展生存期(PFS)为5.4 个月,中位总生存期(OS)为13.6 个月。78 例EGFR突变患者中43.6%的患者肿瘤缩小或消失,4例患者达到完全缓解(CR),30例患者部分缓解(PR),27例患者病情稳定(SD),疾病控制率(DCR)为 82.1%;34例携带ALK重排的患者中,8例患者达到部分缓解(PR),17例患者病情稳定(SD),疾病控制率(DCR)为73.5%。
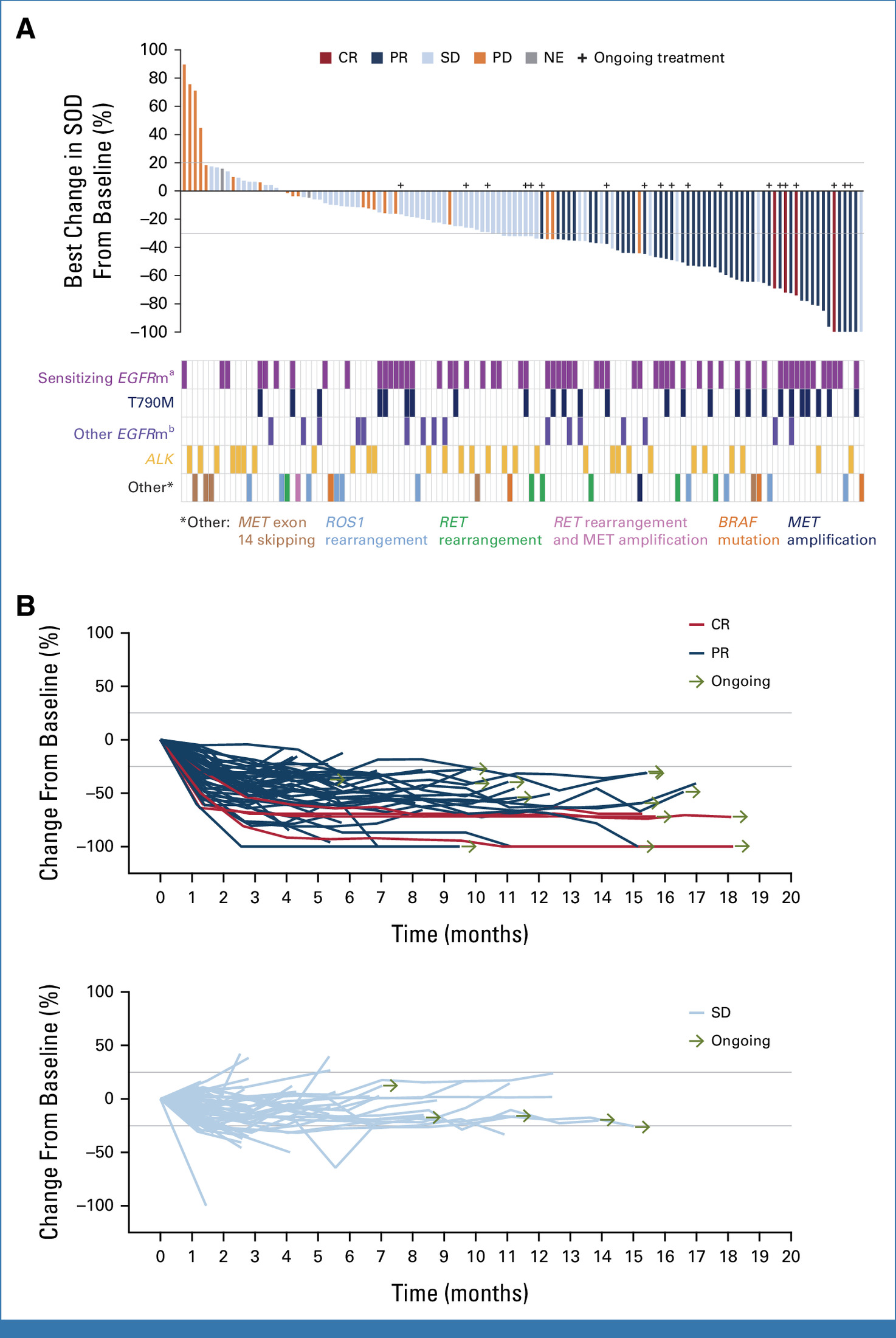
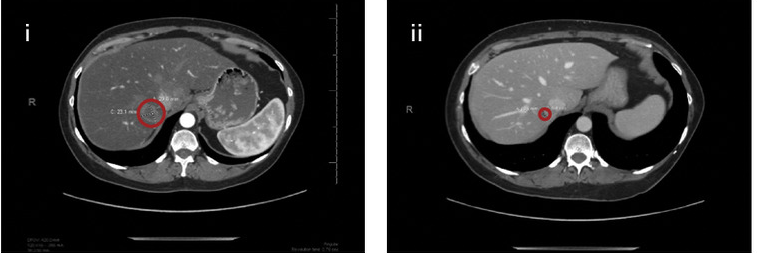
截图源于参考资料1
所有患者中位缓解持续时间(DOR)为7.0个月,中位无进展生存期(PFS)为5.4个月,中位总生存期(OS)为13.6个月。EGFR突变患者中位缓解持续时间(DOR)为7.0个月,中位无进展生存期(PFS)为5.8 个月,中位总生存期(OS)为18.3个月;携带ALK重排的患者中位无进展生存期(PFS)为4.3个月,中位总生存期(OS)为9.3个月。
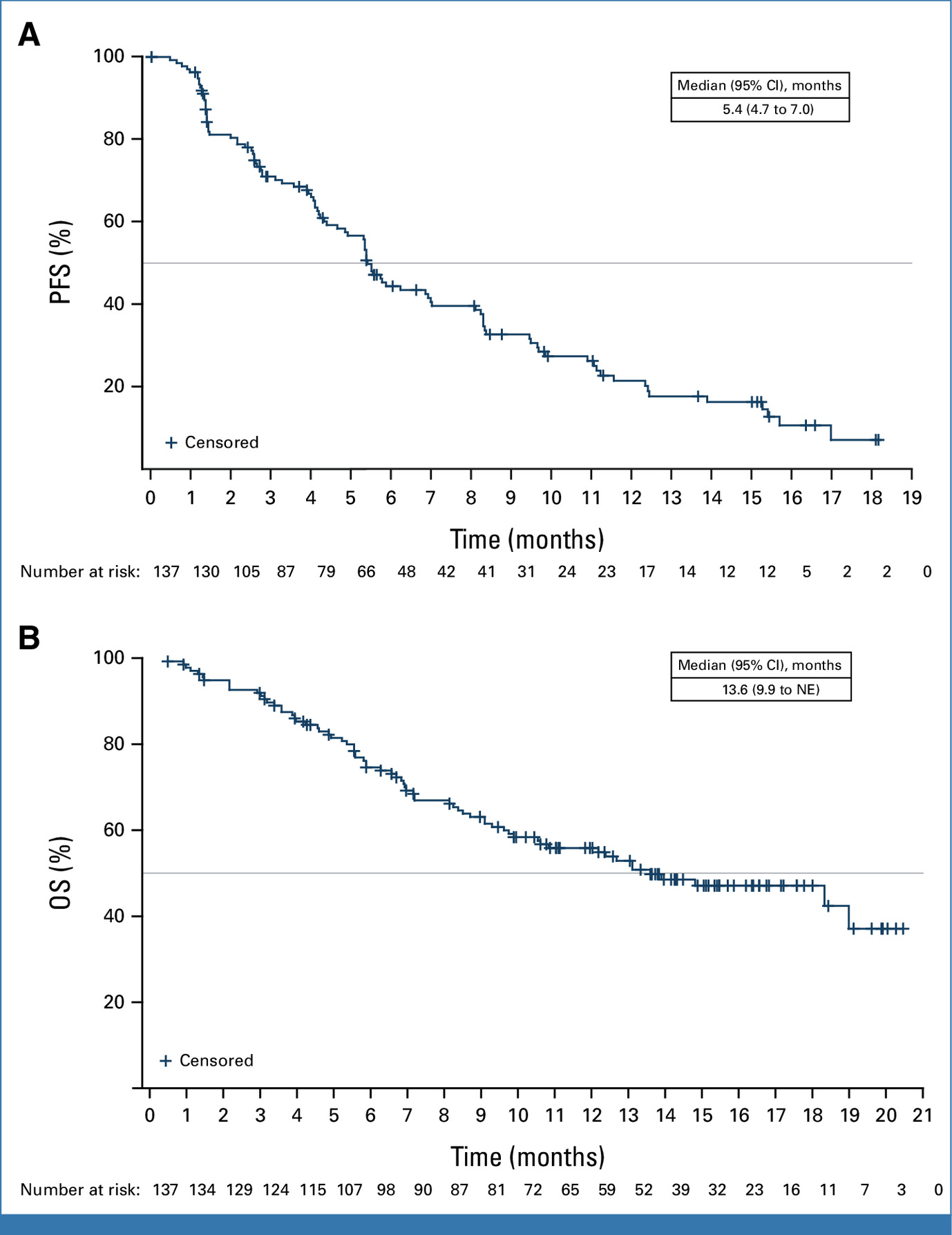
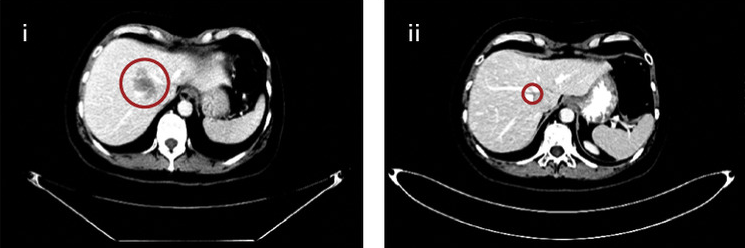
截图源于参考资料1
该试验中,Dato-DXd 在经过大量预处理的晚期/转移性非小细胞肺癌患者中观察到令人鼓舞且持久的抗肿瘤活性。
Datopotamab deruxtecan(Dato-DXd)是一款由人源化、靶向Trop2的单克隆抗体与创新DNA拓扑异构酶I抑制剂(DXd),通过可裂解的四肽连接子偶联生成的抗体偶联药物 (ADC)。2024年11月,第一三共和阿斯利康已向美国食品药品监督管理局(FDA)提交生物制品许可申请,用于治疗既往接受过全身治疗的局部晚期或转移性表皮生长因子受体突变(EGFR 突变)非小细胞肺癌 (NSCLC) 成年患者。 目前ADC药物正在全国范围内寻找HER2过表达的实体瘤患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以联系康和源免疫之家医学部(400-880-3716)。 部分入选标准: 1.年龄至少18岁; 2.晚期实体瘤患者; 3.ECOG体能状态评分为0~1。 临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可致电至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。

参考资料 1.https://ascopubs.org/doi/10.1200/JCO-24-01349 2.https://daiichisankyo.us/press-releases/-/article/datopotamab-deruxtecan-new-bla-submitted-for-accelerated-approval-in-the-u-s-for-patients-with-previously-treated-advanced-egfr-mutated-non-small-cell 3.https://ascopubs.org/doi/10.1200/JCO.24.00920 4.https://ascopubs.org/doi/10.1200/JCO.23.01909 5.https://ascopubs.org/doi/10.1200/JCO.2025.43.5_suppl.663