
8月1日,全球首个TCR-T细胞疗法Tecelra(Afami-cel)获批上市!这一里程碑事件为癌症治疗领域带来了新突破。而这一产品标价72.7万美元,折合人民币约522万,是迄今为止已上市细胞疗法中最为昂贵的细胞产品。由此引发了关于其高昂价格与TCR-T细胞治疗效果的广泛讨论。
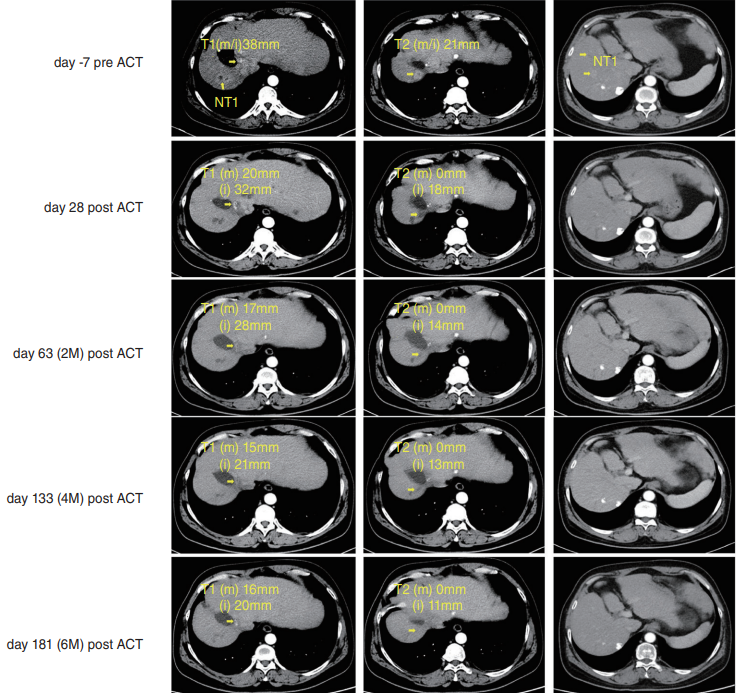
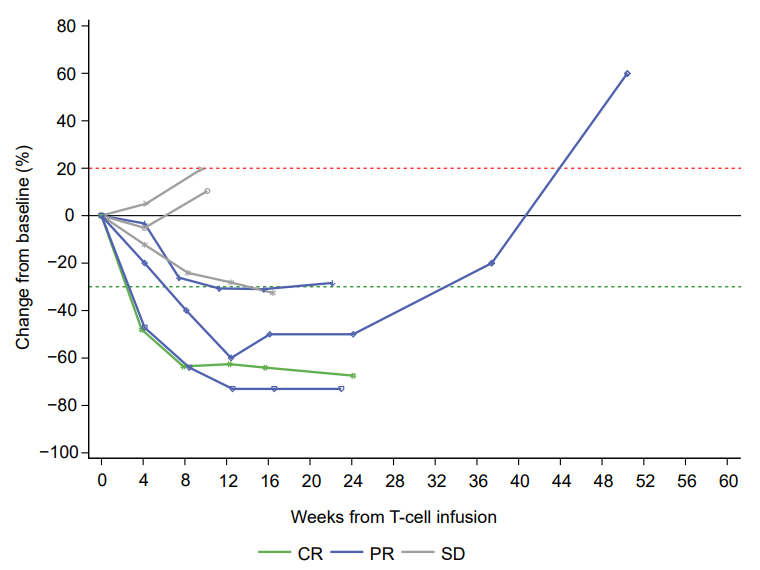
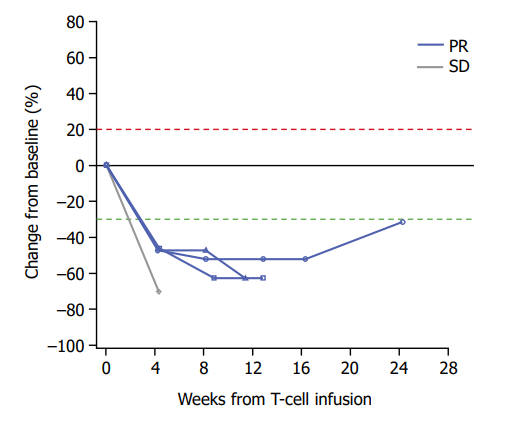
关于TCR-T细胞疗法 截图源于参考资料5 截图源于参考资料6 结语 参考资料 1.https://www.adaptimmune.com/investors-and-media/news-center/press-releases/detail/271/adaptimmune-receives-u-s-fda-accelerated-approval-of 2.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-afamitresgene-autoleucel-unresectable-or-metastatic-synovial-sarcoma 3.Autologous T cell therapy for MAGE-A4+ solid cancers in HLA-A*02+ patients: a phase 1 trial - PMC (nih.gov) 4.https://e-cmh.org/journal/view.php?doi=10.3350/cmh.2024.0058 5.https://d1io3yog0oux5.cloudfront.net/_beb82ef7ec4487e56ee720d898252492/adaptimmune/files/documents/Ho_MHNCS24_.pdf 6.https://d1io3yog0oux5.cloudfront.net/_5eca70337ca8afadc2c36fb95cd990e9/adaptimmune/db/249/3296/pdf/Hong+ESMO+2021+SURPASS+poster_UPLOADED2.pdf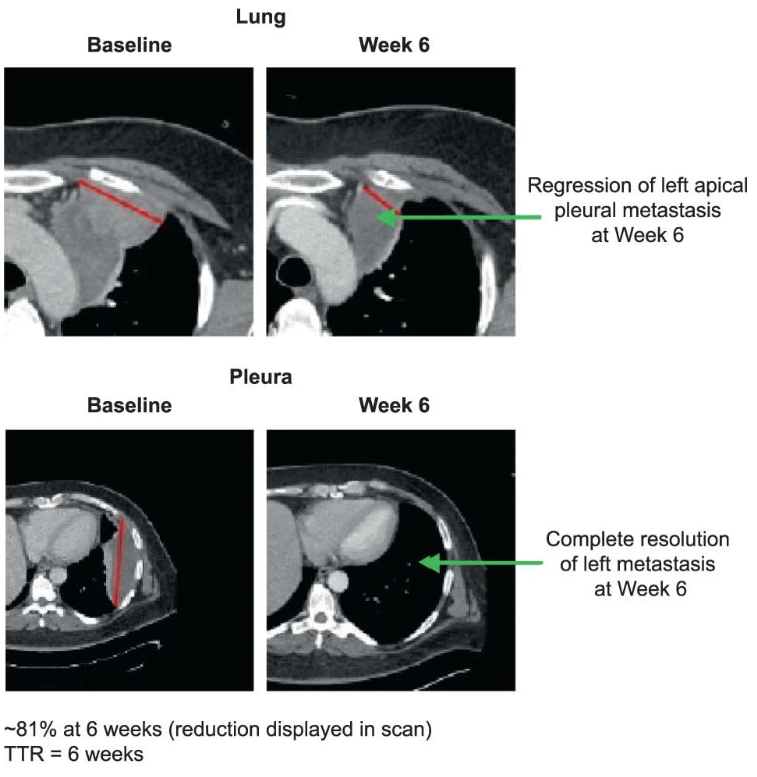


相关推荐
随便看看
- 无复发超过1年!TCR-T疗法新增两款血液肿瘤产品:TSC-100和TSC-101,效果惊艳
- TCR-T狙击手已到位,狙击宫颈癌,肝癌等多款实体瘤!
- 6个月肿瘤缩小了72%!靶向KRAS突变的TCR-T细胞疗法带来新希望
- 黑色素瘤患者肿瘤缩小78.3%!靶向PRAME抗原的TCR-T疗法IMA203持久缓解超1年!
- TCR-T细胞产品lete-cel治疗肉瘤的研究数据登上《Journal of Clinical Oncology》
- TCR-T细胞产品Lete-cel获得突破性疗法认定
- 来恩生物TCR-T细胞产品Liocyx-M004获得美国FDA批准启动2期临床试验
- 星汉德生物SCG101一期临床亮相AASLD
- FDA加速批准!TCR-T疗法让胰腺癌患者半年时间肿瘤缩小72%,94%患者病毒暴跌
- 87% 患者肿瘤缩小!TCR-T疗法IMA203用以治疗经治转移性黑色素瘤患者的最新数据公布











