多发性骨髓瘤(Multiple myeloma, MM)是一种浆细胞恶性肿瘤,其特征是恶性浆细胞在骨髓中克隆性增殖,伴有单克隆免疫球蛋白(m蛋白)的过量产生,并伴有终末器官损伤,约占血液系统恶性肿瘤的10%。随着对MM发病机制的认识不断加深和新型治疗药物的应用,如蛋白酶体抑制剂(bortezomib, ixazomib, carfilzomib),免疫调节药物(thalidomide, lenalidomide, pomalidomide),单克隆抗体(daratumumab, isatuximab, elotuzumab),以及选择性核输出抑制剂(selinexor), MM患者的生存结果得到了极大的改善。然而,几乎所有MM患者最终都会复发。尤其是复发或难治性(R/R)患者合并髓外疾病(EMD)或高危细胞遗传学异常,如t(4;14)、t(14;16)、t(14;20)、gain (1q)、del(17p)、TP53突变以及双/三重命中,通常预后较差。此外,在治疗的选择压力下,MM细胞的克隆进化经常发生,这可能导致疾病进展和对常规治疗的耐药性。因此,迫切需要新的治疗方法来治疗R/R MM。
近年来,嵌合抗原受体T (CAR-T)细胞疗法作为一种极具发展前景的免疫疗法,深刻地改变了血液系统恶性肿瘤的治疗格局。为了产生能够特异性识别肿瘤表面抗原的CAR-T细胞,来自患者或健康供体的T细胞经过基因修饰,带有一种特定的肿瘤靶向受体,这种受体被称为嵌合抗原受体(CAR)。CAR结构包含一个单链可变片段(scFv),它可以特异性识别肿瘤表面抗原,而不需要mhc限制性抗原呈递。与效应T细胞类似,CAR-T细胞也可以通过多种方式介导肿瘤杀伤,包括分泌含有穿孔素和颗粒酶的细胞毒性颗粒,产生IFN-γ和TNF-α等促炎细胞因子,激活Fas/Fas配体(Fas/FasL)通路。目前,B细胞成熟抗原(BCMA)是CAR-T细胞治疗MM最成功的靶点,抗BCMA CAR-T细胞治疗在R/R MM患者中取得了前所未有的疗效,为这些R/R MM患者带来了新的希望。此外,EMD的R/R MM患者也可以从抗BCMA CAR-T细胞治疗中获益,但与非EMD患者相比,这些患者通常具有更短的无进展生存期(PFS)和总生存期(OS)。迄今为止,两种抗BCMA CAR-T细胞产品,idecabtagene vicleucel (ide-cel)和ciltacabtagene autoleuel (cilta-cel),已被美国食品和药物管理局(FDA)批准用于治疗R/R MM。近年来,随着越来越多的CAR-T细胞临床试验的开展,CAR-T相关的不良事件逐渐被认识到,并且通常是可控的,如细胞因子释放综合征、CAR-T细胞相关脑病综合征、细胞减少症、感染等。特别是,由于MM患者的体液免疫缺陷以及随后淋巴细胞消耗化疗和抗BCMA CAR-T细胞治疗介导的B细胞发育不全,这些患者非常容易感染,尤其是细菌感染。因此,补充免疫球蛋白和预防性抗感染治疗对这些免疫功能低下的患者是非常必要的。然而,仍然存在一些实质性的挑战,如抗BCMA CAR-T细胞治疗的耐药性,以及CAR-T细胞治疗的可及性有限。因此,许多研究工作正在进行中,以探索有效的策略。
尽管抗BCMA CAR-T细胞治疗R/R MM的结果令人鼓舞,但它通常表现为短期疗效,许多MM患者仍然经历疾病复发或进展。其耐药机制与抗BCMA CAR-T细胞与肿瘤细胞以及复杂的肿瘤微环境相互作用密切相关,涉及抗原逃逸和CAR-T细胞衰竭。有几种潜在的策略可以克服对CAR-T细胞治疗的耐药性,包括利用双靶向CAR-T细胞和装甲CAR-T细胞,通过小分子药物和基因修饰抑制细胞内衰竭相关信号,采用桥接疗法,以及选择在疾病早期收集的T细胞进行CAR-T细胞制造。
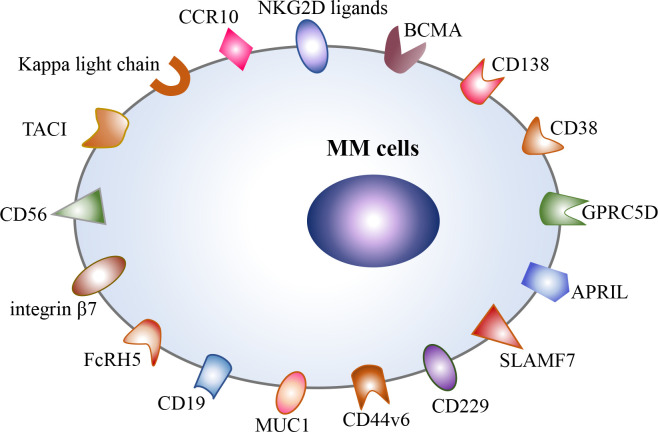
目前,BCMA是治疗MM研究最深入的靶点,包括抗BCMA CAR-T细胞疗法和靶向BCMA和CD3的双特异性抗体,如teclistamab。然而,大多数MM患者在接受抗BCMA CAR-T细胞治疗后仍会出现复发。其主要机制之一是在治疗压力下抗原下调或抗原丢失。因此,靶向不同的表面抗原是防止抗原负逃逸的有效策略,目前正在不断发现多种替代靶点,包括CD138、CD38、CD19、GPRC5D、SLAMF7(CS1)、APRIL、TACI、CD229、CD56、MUC1、NKG2D配体、整合素β7、Kappa轻链、FcRH5、CCR10、CD44v6(图1)。上述靶点大部分仍处于临床前阶段(18-23),只有少数靶点在临床试验中进行了探索,如CD138、CD38、CD19, GPRC5D, SLAMF7和整合素β7 (NCT03778346)。其中,GPRC5D是目前CAR-T细胞治疗R/R MM患者最有潜力的靶点。最近,两项i期试验报道了抗GPRC5D CAR-T细胞疗法令人鼓舞的疗效。在一项1期剂量递增研究中,17名R/R MM患者接受了四种剂量水平的抗GPRC5D CAR-T细胞输注,其中71%的患者获得了临床反应。在另一项单中心一期试验中,10名R/R MM患者接受抗GPRC5D CAR-T细胞(OriCAR-017)治疗,100%的患者表现出临床反应,60%的患者达到严格的完全缓解(sCR)。更重要的是,这些抗GPRC5D CAR-T细胞在既往抗BCMA CAR-T细胞治疗难治性R/R MM患者中也有效。然而,由于中位随访时间相对较短,抗GPRC5D CAR-T细胞治疗R/R MM的疗效和安全性仍需在大规模多中心研究中进行评估。此外,在2022年美国血液学会(ASH)年会上,公布了一项针对GPRC5D靶向CAR-T细胞产品BMS-986393在R/R MM患者中的I期临床试验的初步结果(NCT04674813)。在该临床试验中,10例既往未接受抗BCMA治疗的患者均获得缓解,7例既往抗BCMA治疗失败的患者也可从抗GPRC5D CAR-T细胞治疗中获益。
在一项I期临床试验中,23例R/R MM患者接受BCMA/CD38双特异性CAR-T细胞治疗,87%的患者获得临床缓解,52%的患者获得完全缓解(CR),中位随访时间为9.0个月。在另一项临床试验中,16例R/R MM患者接受BCMA/CD38双特异性CAR-T细胞治疗,在中位随访11.5个月后,14例患者有临床反应,13例患者达到CR。除了BCMA/CD38双特异性CAR-T细胞外,还进行了抗CD38和抗BCMA CAR-T细胞联合治疗。在一项2期单臂单中心临床试验中,22例R/R MM患者接受了人源化抗BCMA细胞和小鼠抗cd38 CAR-T细胞联合输注,91%的患者有临床反应,55%的患者达到CR。在另一项单臂II期试验中,21例患者接受了抗BCMA和抗CD19 CAR-T细胞联合输注治疗,其中20例获得临床缓解,3例达到CR,中位随访179天。随着随访时间的延长,该试验纳入的患者数量增加,62例R/R MM患者接受了抗BCMA和抗CD19 CAR-T细胞联合输注。在这项临床试验中,92%的患者有临床反应,60%的患者达到CR,中位随访时间为21.3个月。一项研究探讨了抗CD19和抗BCMA CAR-T细胞联合治疗10例新诊断的具有高危因素的MM患者的疗效和安全性,所有患者均获得了临床缓解。
在临床前研究中,BCMA/GPRC5D和BCMA/CS1双特异性CAR-T细胞对MM细胞表现出较强的抗肿瘤活性,并能克服BCMA阴性抗原逃逸。同样,BCMA/CS1双特异性CAR-T细胞在R/R MM患者中也有效,并且能够防止BCMA阴性复发。有趣的是,一些天然配体能够结合MM细胞上的两种或多种表面抗原,因此这些由这些配体衍生的抗原识别结构域制造的CAR-T细胞能够识别恶性细胞上的几种靶抗原,并实现双抗原或多抗原靶向。
近年来,抗BCMA CAR-T细胞疗法在治疗R/R MM方面取得了令人瞩目的效果,其副作用总体可控,但仍有一些挑战需要解决。目前,研究人员正在探索潜在的机制和治疗策略,如寻找新的治疗靶点、优化CAR结构和基因修饰方法、应用双靶向CAR-T细胞治疗以及CAR-T细胞治疗与其他方法的联合治疗等。然而,由于CAR-T细胞治疗的耐药和持续存在的高危因素,后续的抗骨髓瘤治疗也具有重要的临床意义。
目前免疫管家已开通微信公众号,健康界,知乎,今日头条等多自媒体网站并且同名[免疫管家]
扫描下方二维码,或者直接电话咨询免疫管家医学部(400-880-3716),为癌友患者们分享更多信息。

免责声明:免疫管家为免疫科普平台,文本参考来源于网络,版权归原作者所有。该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!











